STRIBILD®
GADOR
STRIBILD® es una combinación de dosis fija de los medicamentos antivirales elvitegravir (reforzado con el inhibidor de la CYP3A cobicistat) emtricitabina y tenofovir disoproxil fumarato (tenofovir DF).
Composición.
Cada comprimido recubierto de STRIBILD® contiene: Elvitegravir 150 mg, Cobicistat 150 mg, Emtricitabina 200 mg, Tenofovir disoproxil fumarato 300 mg. Excipientes: Hidroxipropilcelulosa, Laurilsulfato de sodio, Dióxido de silicio, Lactosa monohidrato, Celulosa microcristalina, Croscarmelosa sódica, Estearato de magnesio, Opadry II verde 85F91215 c.s.
Farmacología.
Descripción: STRIBILD® es un comprimido de combinación de dosis fija que contiene elvitegravir, cobicistat, emtricitabina y tenofovir DF para administración oral. Elvitegravir es un inhibidor de transferencia de cadenas de integrasa del VIH-1. Cobicistat es un inhibidor basado en un mecanismo de enzimas de citocromo P450 (CYP) de la familia CYP3A. Emtricitabina es un análogo de nucleósido sintético de la citidina. Tenofovir DF se convierte in vivo a tenofovir, un fosfonato nucleósido acíclico (nucleótido) análogo de 5' adenosinmonofosfato. Cada comprimido contiene 150 mg de elvitegravir, 150 mg de cobicistat, 200 mg de emtricitabina y 300 mg de tenofovir DF (equivalente a 245 mg de disoproxilo de tenofovir). Los comprimidos incluyen los siguientes ingredientes inactivos: monohidrato de lactosa, celulosa microcristalina, dióxido de silicio, croscaramelosa sódica, hidroxipropilcelulosa, laurilsulfato de sodio y estearato de magnesio. Los comprimidos están recubiertos con una película de material de revestimiento que contiene laca de aluminio carmín índigo (FD&C Azul No 2), polietilenglicol, alcohol polivinílico, talco, dióxido de titanio y óxido de hierro amarillo. Elvitegravir: El nombre químico de elvitegravir es 6-(3-Cloro-2-fluorobenzilo)-1-[(2S)-1-hidroxi-3-metilbutano-2-il]-7-metoxi-4-oxo-1,4-ácido dihidroquinolina-3-carboxílico. Tiene una fórmula molecular de C23H23ClFNO5 y un peso molecular de 447,9. Posee la siguiente fórmula estructural:
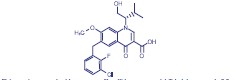
Elvitegravir es un polvo blanco a amarillo pálido con una solubilidad de menos de 0,3 microgramos por mL en agua a 20 °C. Cobicistat: El nombre químico de cobicistat es 1,3-tiazol-5-ilmetil [(2R,5R)5-{[(2S)-2-[(metil{[2-(propano-2-il)-1,3-tiazol-4-il]metil}carbamoil)amino]-4(morfolin-4-il)butanoil]amino}-1,6-difenilhexano-2-il]carbamato. Tiene una fórmula molecular de C40H53N7O5S2 y un peso molecular de 776,0. Posee la siguiente fórmula estructural:
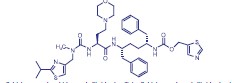
Cobicistat es absorbido en el dióxido de silicio. Cobicistat sobre el dióxido de silicio es un sólido blanco a amarillo pálido con una solubilidad de 0,1 mg por mL en agua a 20°C. Emtricitabina: El nombre químico de emtricitabina es 5-fluoro-1-[(2R,5S)-2(hidroximetil)-1,3-oxatiolan-5-il]citosina. Emtricitabina es el enantiómero (-) de un tiol análogo de citidina, que difiere de los otros análogos de la citidina en que tiene un flúor en la posición 5. Tiene una fórmula molecular de C8H10FN3O3S y un peso molecular de 247,24. Posee la siguiente fórmula estructural:
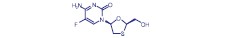
Emtricitabina es un polvo cristalino de blanco a blanco crema con una solubilidad de aproximadamente 112 mg por mL en agua a 25 °C. Tenofovir DF: Tenofovir DF es una sal de ácido fumárico del éster bis-isopropoxicarboniloximetilo de tenofovir. El nombre químico de tenofovir DF es fumarato de 9-[(R)-2-[[bis[[(isopropoxicarbonil)oxi]-metoxi]fosfinil]metoxi]propil]adenina (1:1). Tiene una fórmula molecular de C19H30N5O10P < 195 > C4H4O4 y un peso molecular de 635,52. Posee la siguiente fórmula estructural:
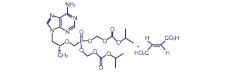
Tenofovir DF es un polvo cristalino de blanco a blanco crema con una solubilidad de 13,4 mg por mL en agua a 25 °C. Todas las dosis están expresadas en términos de tenofovir DF excepto donde se menciona lo contrario. Acción Farmacológica - Farmacología Clínica: Mecanismo de acción: STRIBILD® es una combinación de dosis fija de medicamentos antirretrovirales elvitegravir (reforzado con el inhibidor de la CYP3A cobicistat), emtricitabina y tenofovir DF [Consulte Microbiología]. Farmacodinamia: Efectos en el electrocardiograma: Se han realizado estudios completos de QT para elvitegravir y cobicistat. No se conoce el efecto de los otros dos componentes, tenofovir y emtricitabina, o el régimen de combinación de STRIBILD® en el intervalo QT. Elvitegravir: En un estudio exhaustivo del intervalo QT/QTc efectuado en 126 sujetos sanos, el elvitegravir (coadministrado con 100 mg de ritonavir) en dosis de 125 mg y 250 mg (0,83 y 1,67 veces la dosis incluida en STRIBILD®) no afectó el intervalo QT/QTc ni prolongó el intervalo PR. Cobicistat: En un estudio exhaustivo del intervalo QT/QTc efectuado en 48 sujetos sanos, el intervalo QT/QTc no se vio afectado al administrar una dosis única de 250 mg y 400 mg de cobicistat (1,67 y 2,67 veces la dosis incluida en STRIBILD®). Se observó prolongación del intervalo PR en los sujetos que recibieron cobicistat. La diferencia media máxima (límite superior de confianza del 95 %) en el intervalo PR respecto del placebo después de la corrección según el valor basal fue de 9,5 (12,1) ms para la dosis de 250 mg de cobicistat y de 20,2 (22,8) para la dosis de 400 mg de cobicistat. Dado que la dosis de 150 mg de cobicistat incluida en el comprimido de dosis fijas combinadas de STRIBILD® es menor que la dosis más baja evaluada en el estudio exhaustivo del intervalo QT, es poco probable que el tratamiento con STRIBILD® provoque una prolongación del intervalo PR que sea clínicamente relevante. Efectos en la creatinina sérica El efecto del cobicistat en la creatinina sérica se investigó en un estudio de fase 1 efectuado en sujetos con una TFGe de al menos 80 ml por minuto (N=18) y con una TFGe de 50 a 79 ml por minuto (N=12). Se observó un cambio estadísticamente significativo en la TFGeCG respecto del valor basal después de 7 días de tratamiento con 150 mg de cobicistat entre los sujetos con una TFGe de al menos 80 ml por minuto (9,9 ± 13,1 ml/min) y los sujetos con una TFGe de 50 a 79 ml por minuto (11,9 ± 7,0 ml por minuto). Estas reducciones en la TFGeCG se revirtieron luego de suspender el tratamiento con cobicistat. No se observó ninguna modificación respecto del valor basal en la tasa de filtración glomerular real, determinada según el aclaramiento del fármaco sonda iohexol, luego del tratamiento con cobicistat entre los sujetos con una TFGe de al menos 50 ml por minuto, lo que indica que el cobicistat inhibe la secreción tubular de creatinina, que se manifiesta como una reducción en la TFGeCG, sin afectar la tasa de filtración glomerular real. Farmacocinética: En la tabla 1, se informan las propiedades farmacocinéticas de los componentes de STRIBILD®. En la tabla 2, se presentan los parámetros farmacocinéticos de las dosis múltiples de elvitegravir, cobicistat, emtricitabina y tenofovir.
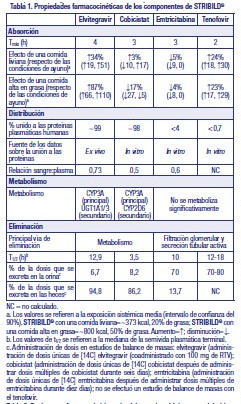
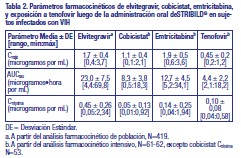
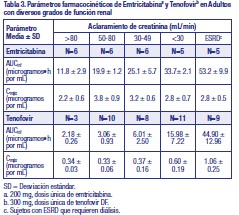
Poblaciones específicas: Pacientes Geriátricos: No se ha evaluado completamente la farmacocinética de elvitegravir, cobicistat, emtricitabina y tenofovir en pacientes geriátricos (65 años y mayores) [Consulte Uso en Poblaciones Específicas]. Pacientes Pediátricos: Las exposiciones (ABC) al elvitegravir y al tenofovir en 14 sujetos pediátricos de edad entre 12 y menos de 18 años que recibieron STRIBILD® en el estudio 112 se incrementaron un 30 % y 37 %, respectivamente, en comparación con las exposiciones alcanzadas en los adultos luego de la administración de STRIBILD®; no obstante, dichas exposiciones se consideraron aceptables de acuerdo con el perfil general de seguridad de estos fármacos y las evaluaciones de seguridad en función de la exposición. Los demás componentes de STRIBILD® generaron exposiciones similares en los adolescentes en comparación con los adultos [ver Uso en poblaciones específicas]. Se ha estudiado la emtricitabina en sujetos pediátricos a partir de 3 meses hasta 17 años de edad. Se ha estudiado el tenofovir DF en sujetos pediátricos a partir de 2 años hasta menos de 18 años de edad. No se ha establecido la farmacocinética de elvitegravir o cobicistat en sujetos pediátricos menores de 12 años de edad [Consulte Uso en Poblaciones Específicas]. Raza, Sexo: No se identificaron diferencias clínicamente significativas en la farmacocinética de STRIBILD® en base a la raza o el sexo. Pacientes con insuficiencia renal Elvitegravir y cobicistat: Se realizó un estudio de farmacocinética del cobicistat + elvitegravir en sujetos sanos y sujetos con insuficiencia renal severa (aclaramiento estimado de creatinina menor a 30 mL por minuto). No se observaron diferencias clínicamente relevantes en la farmacocinética de elvitegravir o cobicistat entre los sujetos sanos y los sujetos con insuficiencia renal severa. Emtricitabina y tenofovir DF: La farmacocinética de emtricitabina y tenofovir se altera en sujetos con aclaramiento estimado de creatinina por debajo de 50 mL por minuto o con enfermedad renal en etapa terminal que requiere diálisis. (ESRD) (Tabla 3) [Consulte Advertencias y Uso en Poblaciones Específicas].
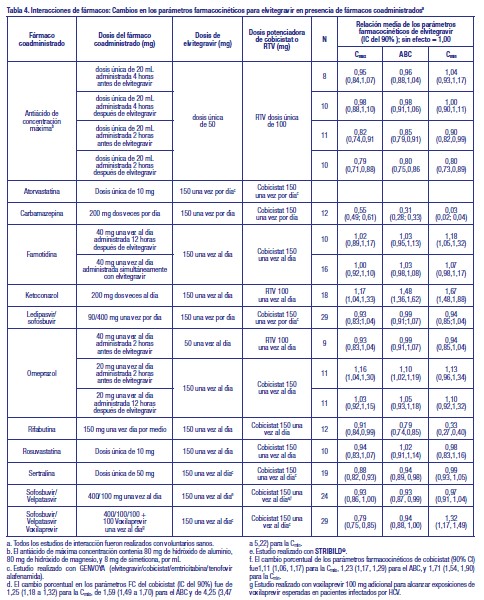
Pacientes con insuficiencia hepática: Elvitegravir y cobicistat: Se realizó un estudio de farmacocinética del cobicistat + elvitegravir en sujetos sanos y sujetos con insuficiencia hepática moderada (Clase B de Child-Pugh). No se observaron diferencias clínicamente relevantes en la farmacocinética de elvitegravir o cobicistat entre los sujetos sanos y los sujetos con insuficiencia hepática moderada. No se ha estudiado el efecto de la insuficiencia hepática severa (Clase C de Child-Pugh) en la farmacocinética de elvitegravir o cobicistat [Consulte Uso en Poblaciones Específicas]. Emtricitabina: No se ha estudiado la farmacocinética de emtricitabina en pacientes con insuficiencia hepática; sin embargo, las enzimas hepáticas no metabolizan significativamente la emtricitabina, por lo que el impacto de la insuficiencia hepática debería ser limitado. Tenofovir DF: Se ha estudiado la farmacocinética de tenofovir después de una dosis de 300 mg de VIREAD (tenofovir DF) en sujetos sanos con insuficiencia hepática moderada a severa (Clase C de Child-Pugh). No se observaron diferencias clínicamente relevantes en la farmacocinética de tenofovir entre los sujetos sanos y los sujetos con insuficiencia hepática. Coinfección con los Virus de Hepatitis B y/o Hepatitis C: Elvitegravir: Los limitados datos del análisis farmacocinético poblacional (N=24) indicaron que la infección por el virus de hepatitis B y/o C no tuvo efecto clínicamente relevante sobre la exposición de elvitegravir reforzado con cobicistat. Cobicistat: Se recolectaron insuficientes datos de farmacocinética en los estudios clínicos para determinar el efecto de la infección por el virus de hepatitis B y/o C en la farmacocinética de cobicistat. Emtricitabina y Tenofovir: La farmacocinética de emtricitabina y tenofovir DF no ha sido completamente evaluada en sujetos coinfectados con el virus de hepatitis B y/o C. Evaluación de interacciones de fármacos: [Ver Contraindicaciones e Interacciones de fármacos]. Se realizaron estudios sobre la interacción fármaco-fármaco, descriptos en las Tablas 3 y 4, con STRIBILD®, elvitegravir (coadministrado con cobicistat o ritonavir), o cobicistat administrado solo. Como STRIBILD® está indicado para uso como régimen completo para tratar la infección por VIH-1 y no se debería administrar con otros medicamentos antirretrovirales, no se provee información sobre las interacciones fármaco-fármaco con otros agentes antirretrovirales. Los efectos de fármacos coadministrados sobre la exposición de elvitegravir, emtricitabina y tenofovir se muestran en la Tabla 4, la Tabla 5 y la Tabla 6, respectivamente. Los efectos de elvitegravir más cobicistat, o cobicistat, o emtricitabina sobre la exposición de fármacos coadministrados se muestra en la Tabla 7. Para obtener información con respecto a recomendaciones clínicas, consulte [Interacciones de Fármacos]. (Ver Tabla 4, Tabla 5, Tabla 6 y Tabla 7.).



Microbiología: Mecanismo de Acción: Elvitegravir: Elvitegravir inhibe la actividad de transferencia de cadenas de la integrasa del VIH-1 (inhibidor de transferencia de cadena de la integrasa; ITCI), una enzima codificada por el VIH-1 que se requiere para la replicación viral. La inhibición de la integrasa evita la integración del ADN del VIH-1 en el ADN genómico del hospedero, bloqueando la formación del provirus del VIH-1 y la propagación de la infección viral. Elvitegravir no inhibe las topoisomerasas humanas I o II. Cobicistat: Cobicistat es un inhibidor selectivo, basado en el mecanismo de citocromos P450 de la subfamilia CYP3A. La inhibición del metabolismo mediado por CYP3A por cobicistat mejora la exposición sistémica de los sustratos de CYP3A, como elvitegravir, donde la biodisponibilidad está limitada y la vida media es acortada por el metabolismo dependiente de CYP3A. Emtricitabina: Emtricitabina, un análogo nucleósido sintético de citidina, es fosforilado por las enzimas celulares para formar emtricitabina 5'-trifosfato. La emtricitabina 5'-trifosfato inhibe la actividad de la transcriptasa reversa (TR) del VIH-1 por competencia con el sustrato natural desoxicitidina 5'-trifosfato y se incorpora en el ADN viral naciente, con laconsecuente terminación de la cadena. Emtricitabina 5'-trifosfato es un inhibidor débil de polimerasas del ADN de mamíferos,,, y polimerasa del ADN mitocondrial. Tenofovir DF: Tenofovir DF es un análogo del diéster de fosfonato nucleósido acíclico de adenosinmonofosfato. Tenofovir DF requiere hidrólisis diéster inicial para la conversión a tenofovir y subsiguientes fosforilaciones por medio de enzimas celulares para formar difosfato de tenofovir. El tenofovir difosfato inhibe la actividad de la TR del VIH-1 por competencia con el sustrato natural desoxiadenosina 5'-trifosfato y, tras su incorporación en el ADN, por terminación de la cadena de ADN. El difosfato de tenofovir es un inhibidor débil de las polimerasas del ADN de mamíferos,, y polimerasa del ADN mitocondrial. Actividad antiviral en cultivo celular: Elvitegravir, cobicistat, emtricitabina y tenofovir DF: La triple combinación de elvitegravir, emtricitabina y tenofovir no fue antagonística en las pruebas de actividad antiviral en combinación en cultivo celular y no estuvo afectada por el agregado de cobicistat. Elvitegravir: La actividad antiviral de elvitegravir contra las cepas clínicas y de laboratorio de VIH-1 fue evaluada en líneas celulares linfoblastoide T, células monocito/macrofágicas y linfocitos sanguíneos periféricos principales. El 50% de concentraciones efectivas (CE50) varió de 0,02 a 1,7 nM. Elvitegravir mostró actividad antiviral en cultivo celular contra clados A, B, C, D, E, F, G y O de VIH-1 (valores de CE50 que oscilaron entre 0,1 a 1,3 nM) y actividad contra VIH-2 (valor de CE50 de 0,53 nM). El elvitegravir no mostró inhibición de la replicación del VHB o VHC en cultivo celular. Cobicistat: Cobicistat no tiene actividad antiviral detectable en cultivo celular contra VIH-1, virus de la hepatitis B crónica(VHB) o virus de la hepatitis C(VHC) y no antagoniza la actividad antiviral de elvitegravir, emtricitabina, o tenofovir. Emtricitabina: La actividad antiviral de emtricitabina contra las cepas clínicas y de laboratorio de VIH-1 fue evaluada en líneas celulares linfoblastoide T, líneas de células MAGI-CCR5 y células mononucleares sanguíneas periféricas principales. Los valores de CE50 para emtricitabina estuvieron en el rango de 0,0013-0,64 micromolar. Emtricitabina mostró actividad antiviral en cultivo celular contra clados A, B, C, D, E, F y G deVIH-1(valores de CE50 que oscilaron entre 0,007-0,075 micromolar) y mostró actividad específica de cepa contra VIH-2 (valores de EC50 entre 0,007-1,5 micromolar). Tenofovir DF: La actividad antiviral de tenofovir contra las cepas clínicas y de laboratorio del VIH-1 fue evaluada en líneas celulares linfoblastoides T, células principales monocito/macrofágicas y linfocitos sanguíneos periféricos. Los valores de CE50 para tenofovir estuvieron en el rango de 0,04-8,5 micromolar. Tenofovir mostró actividad antiviral en cultivo celular contra clados A, B, C, D, E, F, G y O de VIH-1 (valores de CE50 que oscilaron entre 0,5-2,2 micromolar) y mostró actividad específica de cepa contra VIH-2 (valores deCE50 entre 1,65,5 micromolar). Resistencia: En Cultivo Celular: Elvitegravir: Las cepas de VIH-1 con susceptibilidad reducida para elvitegravir se seleccionaron en el cultivo celular. La susceptibilidad reducida para elvitegravir fue asociada con las sustituciones principales de integrasa T66A/I, E92G/Q, S147G y Q148R. Las sustituciones de integrasa adicionales observadas en la selección de cultivo celular incluían D10E, S17N, H51Y, F121Y, S153F/Y, E157Q, D232N, R263K y V281M. Emtricitabina y Tenofovir DF: Las cepas de VIH-1 con susceptibilidad reducida para emtricitabina o tenofovir se seleccionaron en el cultivo celular. La susceptibilidad reducida para emtricitabina fue asociada con sustituciones M184V/I en la TR del VIH-1. Las cepas de VIH-1 seleccionadas por tenofovir expresaron una sustitución K65R en la TR del VIH-1 y mostraron una reducción de 2-4 veces en la susceptibilidad para tenofovir. En estudios clínicos: Elvitegravir: El desarrollo de sustituciones T66A/I/K, E92G/Q, T97A, S147G, Q148H/K/R y N155H en la proteína de la integrasa del VIH-1 estuvo asociado principalmente con la resistencia al elvitegravir. Además de estas sustituciones primarias asociadas con la resistencia al elvitegravir, también se observaron ocasionalmente sustituciones E92A, F121C/Y, P145S, Q146I/L/R y N155S, y se demostró que reducen la susceptibilidad al elvitegravir. En los aislamientos virales que albergaban las sustituciones primarias observadas en asociación con la resistencia al elvitegravir, se detectaron sustituciones adicionales en la integrasa, que incluyeron H51Y, L68I/V, G70R, V72A/N, I73V, Q95K/R, S119R, E138A/K, G140A/C/S, E157Q, K160N, E170A, S230R y D232N. Emtricitabina y tenofovir DF: Se han seleccionado aislamientos de VIH-1 con susceptibilidad reducida a la emtricitabina o al tenofovir obtenidos de sujetos que presentaron fracaso virológico en los estudios clínicos. El análisis genotípico de estos aislamientos identificó sustituciones de los aminoácidos M184V/I y K65R en la TR viral, respectivamente. Elvitegravir, cobicistat, emtricitabina y tenofovir DF: En los estudios clínicos efectuados en sujetos infectados por el VIH-1 sin antecedentes de tratamiento antirretroviral [en los estudios 102 y 103, ver Estudios clínicos (8)], al cabo de 144 semanas, se observó el desarrollo de una o más sustituciones primarias asociadas con la resistencia al elvitegravir, a la emtricitabina y/o al tenofovir en los virus obtenidos del 51% (18/35) de los sujetos que tuvieron un fracaso terapéutico con STRIBILD®, que contaban con datos de resistencia genotípica evaluables, que habían recibido al menos 8 semanas de STRIBILD® y que tenían un valor de ARN del VIH-1 superior o igual a 400 copias por ml en la confirmación del fracaso virológico, al final de cada año del estudio o en el momento de la suspensión prematura del fármaco del estudio. Las sustituciones que surgieron más comúnmente fueron M184V/I (N=17) en la TR del VIH-1 y las sustituciones primarias asociadas con la resistencia al elvitegravir, E92Q (N=9), N155H (N=5), Q148R (N=3), T66I (N=2) y T97A (N=1) en la integrasa; también se detectó la sustitución K65R en la TR (N=5). En los aislamientos virales que albergaban las sustituciones primarias observadas en asociación con la resistencia al elvitegravir, se detectaron sustituciones adicionales en la integrasa, que incluyeron H51Y, L68I/V, G70R, I73V, G140C, S153A, E157Q y G163R. El virus presente en todos los sujetos con datos evaluables para la TR y la integrasa, y cuyo virus desarrolló sustituciones en la integrasa asociadas con la resistencia al elvitegravir (N=14) también desarrolló las sustituciones M184I/V en la TI, y se redujo la susceptibilidad tanto al elvitegravir como a la emtricitabina. En los análisis fenotípicos, los aislamientos del VIH-1 que expresaban las sustituciones M184V/I en la TR mostraron una susceptibilidad reducida a la emtricitabina (entre 42 y más de 152 veces); los que expresaban las sustituciones primarias en la integrasa asociadas con la resistencia al elvitegravir mostraron una susceptibilidad reducida al elvitegravir (entre 4 y más de 198 veces); y aquellos que expresaban la sustitución K65R en la TR mostraron una susceptibilidad reducida al tenofovir (de 0,8 a 1,6 veces), en comparación con el VIH-1 silvestre de referencia. La cantidad de fracasos virológicos con datos evaluables (N=1) en los estudios clínicos realizados con sujetos infectados por el VIH-1, con supresión virológica y sin antecedentes de fracaso virológico, los estudios 115 y 121 [ver Estudios clínicos] fue insuficiente para establecer conclusiones acerca del desarrollo de resistencia. Resistencia cruzada: Los aislamientos de sujetos con fracaso en el tratamiento con STRIBILD® mostraron grados variables de resistencia cruzada dentro de las clases de fármacos de ITCI e INTRdependiendo de las sustituciones específicas observadas. Estos aislamientos permanecieron susceptibles a todos los INNTR e inhibidores de proteasa. Elvitegravir: Se ha observado resistencia cruzada entre los ITCI. Los virus resistentes al elvitegravir mostraron diversos grados de resistencia cruzada al raltegravir en cultivo celular según el tipo y la cantidad de sustituciones en la integrasa del VIH-1. De las sustituciones primarias asociadas con la resistencia al elvitegravir que se evaluaron (T66A/I/K, E92G/Q, T97A, S147G, Q148H/K/R y N155H), todas salvo tres (T66I, E92G y S147G) redujeron más de 1,5 veces la susceptibilidad al raltegravir (por encima del corte biológico para el raltegravir) cuando se introdujeron individualmente en el virus inhibición por emtricitabina. Tenofovir DF: Se ha observado resistencia cruzada entre los INTR. La sustitución K65R en la TR del VIH-1 seleccionada por tenofovir también es seleccionada en algunos pacientes infectados con VIH-1 tratados con abacavir o didanosina. Los aislamientos de VIH-1 con sustitución K65R también mostraron susceptibilidad reducida para emtricitabina y lamivudina. Por ello, la resistencia cruzada entre estos INTR puede producirse en pacientes cuyos virus albergan la sustitución K65R. La sustitución K70E seleccionada clínicamente por el tenofovir DF reduce la susceptibilidad al abacavir, la didanosina, la emtricitabina, la lamivudina y el tenofovir. Los aislamientos de VIH-1 de pacientes (N=20) cuyo VIH-1 expresó una media de 3 sustituciones de aminoácidos de la TR asociadas con zidovudina (M41L, D67N, K70R, L210W, T215Y/F, o K219Q/E/N) mostraron una disminución de 3,1 veces en la susceptibilidad para tenofovir. Los sujetos cuyo virus expresó una sustitución L74V en la TR sin sustituciones asociadas a resistencia a zidovudina (N=8) habían reducido la respuesta al tenofovir DF. Se dispone de datos limitados para pacientes cuyos virus expresaron la sustitución Y115F (N=3), la sustitución Q151M (N=2), o la inserción T69 (N=4) en la TR del VIH-1, quienes tuvieron, todos ellos, una respuesta reducida en los estudios clínicos.
Indicaciones.
STRIBILD® está indicado como un régimen completo para el tratamiento de la infección por VIH-1 en adultos y en pacientes pediátricos de 12 años o más que pesan al menos 35 kg y que no tienen antecedentes de haber recibido tratamiento antirretroviral, o para reemplazar el régimen antirretroviral actual en aquellos pacientes con supresión virológica (ARN del VIH-1 inferior a 50 copias/ml) que hayan estado bajo un régimen antirretroviral estable durante al menos 6 meses sin antecedentes de fracaso terapéutico ni sustituciones conocidas asociadas con la resistencia a los componentes individuales de STRIBILD® [ver Estudios Clínicos].
Dosificación.
Pruebas antes de iniciar el tratamiento con STRIBILD® y durante su administración: Antes de iniciar el tratamiento con STRIBILD®,los pacientes deben realizarse análisis para determinar la presencia de infección por el virus de la hepatitis B [ver Advertencias]. Antes de iniciar el tratamiento y durante el uso de STRIBILD®, con un esquema clínico apropiado, evaluar la creatinina sérica, el aclaramiento de creatinina estimado, la glucosuria y la proteinuria en todos los pacientes. En los pacientes con enfermedad renal crónica evaluar también el fósforo sérico [ver Advertencias]. Posología recomendada: STRIBILD® es un producto que combina cuatro fármacos en dosis fijas: 150 mg de elvitegravir, 150 mg de cobicistat, 200 mg de emtricitabina y 300 mg de tenofovir DF. La posología recomendada de STRIBILD® es un comprimido tomado oralmente una vez al día con la comida en adultos y en pacientes pediátricos de 12 años o más con un peso corporal de al menos 35 kg (al menos 77 lb) y cuyo aclaramiento de creatinina es superior o igual a 70 ml por minuto [Consulte Acción Farmacológica Farmacología Clínica]. Ajuste posológico en pacientes con disfunción renal: No se recomienda iniciar el tratamiento con STRIBILD® en pacientes con aclaramiento estimado de creatinina por debajo de 70 mL por minuto. Como STRIBILD® es un comprimido de combinación de dosis fija, STRIBILD® debe interrumpirse si el aclaramiento estimado de creatinina declina por debajo de 50 mL por minuto durante el tratamiento con STRIBILD®, ya que no se puede alcanzar el ajuste de intervalo de dosis requerido para emtricitabina y tenofovir tenofovir DF [Consulte Advertencias, Reacciones Adversas, Uso en Población Específica, Acción Farmacológica Farmacología Clínica, y Estudios Clínicos]. No hay datos disponibles que determinen recomendaciones posológicas para pacientes pediátricos con disfunción renal. No recomendado para pacientes con disfunción hepática grave: No se recomienda utilizar STRIBILD® en pacientes que padecen insuficiencia hepática grave [Consulte Uso en Población Específica y Acción Farmacológica Farmacología Clínica]. No recomendado durante el embarazo: No se recomienda el uso de STRIBILD® durante el embarazo debido a exposiciones sustancialmente más bajas de cobicistat y elvitegravir durante el segundo y el tercer trimestres [ver Uso en Poblaciones Específicas]. No se debería iniciar el tratamiento con STRIBILD® en mujeres embarazadas. Se recomienda un régimen alternativo para las mujeres que quedan embarazadas durante el tratamiento con STRIBILD® [ver Uso en Poblaciones Específicas]. Forma farmacéutica y concentración: Cada comprimido recubierto de STRIBILD® contiene 150 mg de elvitegravir, 150 mg de cobicistat, 200 mg de emtricitabina y 300 mg de tenofovir disoproxil fumarato (tenofovir DF, equivalente a 245 mg de tenofovir disoproxil).
Contraindicaciones.
Está contraindicada la coadministración de STRIBILD® con fármacos que son altamente dependientes de CYP3A para aclaramiento y para los que las concentraciones elevadas en plasma están asociadas con eventos serios y/o potencialmente mortales. Estos fármacos y otros contraindicados (que pueden llevar a la eficiencia reducida de STRIBILD® y posible resistencia) están enumerados a continuación [Consulte Interacciones de Medicamentos, Acción Farmacológica Farmacología Clínica]. Antagonista adrenoreceptor Alfa-1: alfuzosina. Anticonvulsivos: carbamazepina, fenobarbital, fenitoína. Antimicobacterianos: rifampina. Antipsicóticos: lurasidona, pimozida. Derivados del ergot: dihidroergotamina, ergotamina, metilergonovina. Agente de motilidad GI: cisaprida. Productos herbales: Hierba de San Juan (Hypericum perforatum) Agentes modificadores de los lípidos: lomitapida, lovastatina, simvastatina. Inhibidor de la fosfodiesterasa-5 (PDE-5): sildenafil cuando es administrado como REVATIO® para el tratamiento de la hipertensión pulmonar arterial. Sedantes/hipnóticos: triazolam, midazolam administrado oralmente.
Reacciones adversas.
Se trataron las siguientes reacciones adversas a los fármacos en otras secciones del prospecto: Severas exacerbaciones agudas de hepatitis Ben pacientes coinfectados por el VIH-1 y el VHB [Consulte Advertencias]. Nuevo inicio o empeoramiento de insuficiencia renal [Consulte Advertencias]. Acidosis láctica/Severa hepatomegalia con esteatosis [Consulte Advertencias]. Pérdida de masa ósea y defectos de mineralización [Consulte Advertencias]. Síndrome de Reconstitución Inmune [Consulte Advertencias]. Experiencia en Estudios Clínicos: Dado que los estudios clínicos se llevan a cabo en condiciones muy variables, las tasas de reacciones adversas observadas en los estudios clínicos de un determinado fármaco no pueden compararse de manera directa con las tasas obtenidas en los estudios clínicos de otro fármaco y es posible que no reflejen las tasas observadas en la práctica. Estudios clínicos en sujetos adultos infectados por el VIH-1 sin antecedentes de tratamiento antirretroviral: La evaluación de seguridad de STRIBILD® se basó en datos agrupados obtenidos en la semana 144 correspondientes a 1408 sujetos en dos aleatorizados, doble ciego, controlados con principio activo (el estudio 102 y estudio 103), realizados en sujetos adultos infectados con VIH-1 sin tratamiento antirretroviral previo [Ver Estudios Clínicos]. Un total de 701 sujetos recibieron STRIBILD® una vez por día en estos dos estudios. La proporción de los sujetos que interrumpieron el tratamiento con STRIBILD®, ATRIPLA (efavirenz 600 mg/emtricitabina 200 mg/tenofovir DF 300 mg) o ATV+RTV+TRUVADA® (emtricitabina 200 mg/tenofovir DF 300 mg) debido a eventos adversos, sin tener en cuenta la gravedad, fue del 6,0%, 7,4% y 8,5%, respectivamente. La Tabla 12 muestra la frecuencia de reacciones adversas al fármaco mayor o igual al 5%de los sujetos en cualquier grupo de tratamiento.
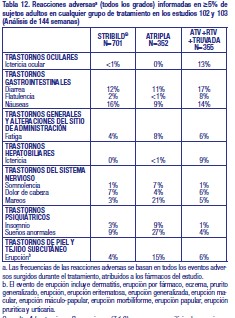
Consulte Advertencias, para ver un análisis de reacciones adversas renales producidas a partir de la experiencia en estudios clínicos con STRIBILD®. Las reacciones adversas adicionales que se observaron al administrar STRIBILD® incluyeron ideación suicida e intento de suicidio (0,3 %); todos los casos se produjeron en sujetos con antecedentes preexistentes de depresión o enfermedad psiquiátrica. Estudios clínicos en sujetos adultos infectados por el VIH-1 con supresión virológica: No se identificaron nuevas reacciones adversas a STRIBILD® hasta la semana 48 en los 584 sujetos adultos virológicamente estables que cambiaron a STRIBILD® desde un régimen que contenía un inhibidor de la proteasa (IP) reforzado con RTV o un inhibidor no nucleósido de la transcriptasa inversa (INNTR). En un análisis combinado de los estudios 115 y 121, la frecuencia de reacciones adversas (todos los grados) fue del 24 % en los sujetos que cambiaron a STRIBILD®, en comparación con el 6 % de los sujetos de cualquiera de los dos grupos que continuaron con su régimen antirretroviral basal, IP reforzado con RTV+TRUVADA (emtricitabina y tenofovir DF), o con INNTR+TRUVADA (emtricitabina y tenofovir DF). Las reacciones adversas frecuentes que se produjeron en el 2 % o más de los sujetos que cambiaron a STRIBILD® fueron náuseas (4 %), flatulencia (2 %) y cefalea (2 %). La proporción de sujetos que suspendieron el tratamiento con STRIBILD®, el IP reforzado con RTV o el INNTR debido a eventos adversos fue del 2 %, 3 % y 1 %, respectivamente. Estudios clínicos efectuados con los componentes de STRIBILD® en sujetos adultos: Emtricitabina y tenofovir DF: Además de las reacciones adversas observadas con STRIBILD®, se produjeron las siguientes reacciones adversas en al menos el 5 % de los sujetos con o sin tratamiento previo que recibieron emtricitabina o tenofovir DF con otros antirretrovirales en otros estudios clínicos: depresión, dolor abdominal, dispepsia, vómitos, fiebre, dolor, nasofaringitis, neumonía, sinusitis, infección en las vías respiratorias superiores, artralgia, dolor de espalda, mialgia, parestesia, neuropatía periférica (que incluye neuritis y neuropatía periféricas), ansiedad, aumento de la tos y rinitis. Se han notificado casos de alteración del color de la piel con una frecuencia mayor entre los sujetos tratados con emtricitabina; se manifestó como hiperpigmentación en las palmas de las manos y/o las plantas de los pies y, en general, fue una reacción leve y asintomática. Se desconocen su mecanismo y significación clínica. Anomalías de laboratorio La Tabla 13 presenta la frecuencia de anomalías de laboratorio (Grados 3-4) que se produjeron en al menos el 2% de los sujetos que recibieron STRIBILD® en los estudios 102 y 103.
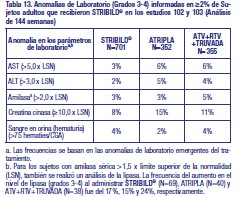
En el estudio 103, se evaluó la DMO mediante densitometría (DEXA) en un subconjunto no aleatorio de 120 sujetos [grupo de STRIBILD®, N=54; grupo de ATV+RTV+TRUVADA (emtricitabina y tenofovir DF), N=66]. El porcentaje medio de disminuciones en la DMO desde la situación basal hasta la semana 144 en el grupo de STRIBILD® fue similar al del grupo de ATV+RTV+TRUVADA (emtricitabina y tenofovir DF) en la columna lumbar (-1,43 % frente a -3,68 %, respectivamente) y en la cadera (-2,83 % frente a -3,77 %, respectivamente). En los estudios 102 y 103, se produjeron fracturas óseas en 27 sujetos (3,9 %) del grupo de STRIBILD®, en 8 sujetos (2,3 %) del grupo de ATRIPLA (efavirenz, emtricitabina y tenofovir DF) y en 19 sujetos (5,4 %) del grupo de ATV+RTV+TRUVADA (emtricitabina y tenofovir DF). Estos hallazgos concordaron con los datos obtenidos de un estudio anterior de 144 semanas de duración en el que participaron sujetos sin tratamiento previo que recibieron tenofovir DF+lamivudina+efavirenz. Se observaron casos de proteinuria (todos los grados) en el 52 % de los sujetos que recibieron STRIBILD®, el 41 % de los sujetos que recibieron ATRIPLA (efavirenz, emtricitabina and tenofovir DF) y el 42 % de los sujetos que recibieron ATV+RTV+TRUVADA (emtricitabina y tenofovir DF). Se ha demostrado que el componente cobicistat de STRIBILD® incrementó la creatinina sérica y disminuyó el aclaramiento de creatinina estimado debido a la inhibición de secreción tubular de creatinina sin afectar la función glomerular renal.En los estudios 102 y 103, se produjeron aumentos en la creatinina sérica y disminuciones en el aclaramiento de creatinina estimado al iniciar el tratamiento con STRIBILD®, que más adelante se estabilizaron. En la tabla 14 se muestran los cambios medios en los niveles de creatinina sérica y la tasa de filtración glomerular estimada (TFGe) en la semana 144, junto con el porcentaje de sujetos con elevaciones en la creatinina sérica (todos los grados).
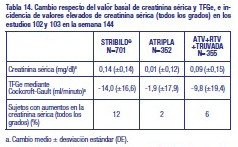
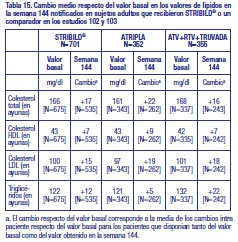
Emtricitabina o Tenofovir DF: Además de las anomalías de laboratorio observadas con STRIBILD®, se han informado las siguientes anomalías de laboratorio en sujetos tratados con emtricitabina o tenofovir DF con otros agentes antirretrovirales en otros estudios clínicos: Anomalías de laboratorio de Grado 3 o 4 de ALT (hombres: mayor de 215 U/L; mujeres: mayor de 170 U/L), fosfatasa alcalina (mayor a 550 U/L), bilirrubina (mayor a 2,5 x LSN), glucosa sérica (menor de 40 o mayor de 250 mg por dL), glucosuria (mayor de o igual a 3+), neutrófilos (menos de 750 por mm3), colesterol en ayunas (mayor de 240 mg/dL), y triglicéridos en ayunas (mayor de 750 mg/dL). Lípidos séricos: En los estudios clínicos de STRIBILD®, el porcentaje de sujetos que recibía hipolipemiantes en la situación basal fue similar entre los sujetos que recibieron STRIBILD®, ATRIPLA (efavirenz, emtricitabina y tenofovir DF) y ATV+RTV+TRUVADA (emtricitabina y tenofovir DF)(12 %, 12 % y 13 %, respectivamente). Durante la administración del fármaco del estudio hasta la semana 144, otro 11 % de los sujetos tratados con STRIBILD® comenzó a utilizar hipolipemiantes, en comparación con el 13 % de los sujetos tratados con ATRIPLA (efavirenz, emtricitabina y tenofovir DF) y el 12 % de los sujetos tratados con ATV+RTV+TRUVADA (emtricitabina y tenofovir DF). Los cambios con respecto al valor inicial en el colesterol total, colesterol HDL, colesterol LDL y triglicéridos se muestran en la Tabla 15.
Estudios clínicos en sujetos pediátricos: Se evaluó la seguridad de STRIBILD® en 50 sujetos pediátricos infectados por el VIH-1 sin tratamiento previo, de edad entre 12 y menos de 18 años, que pesaban al menos 35 kg (77 lb) durante el transcurso de 48 semanas en un estudio clínico abierto (estudio 112) [ver Estudios clínicos]. En este estudio, el perfil de seguridad de STRIBILD® fue similar al de los adultos. Veintidós sujetos (44 %) presentaron proteinuria emergente durante el tratamiento (grados 1-2). Un sujeto reunió los criterios de laboratorio correspondientes a tubulopatía renal proximal, que se evidenció por niveles sostenidos de proteinuria y glucosuria normoglucémica a partir de la semana 32. El sujeto continuó recibiendo STRIBILD® y, finalmente, se perdió durante el seguimiento. Entre los 50 sujetos pediátricos que recibieron STRIBILD® durante 48 semanas, la DMO media se incrementó desde la situación basal hasta la semana 48: +0,68 % en la columna lumbar y +0,77 % en el cuerpo entero menos la cabeza. Los cambios medios en las puntuaciones Z de la DMO (ajustadas en función de la estatura-edad) desde la situación basal hasta la semana 48 fueron -0,09 para la columna lumbar y -0,12 para el cuerpo entero menos la cabeza. En la semana 48, 7 sujetos tratados con STRIBILD® presentaron una pérdida significativa (superior o igual al 4 %) de la DMO en la columna lumbar, y 2 sujetos presentaron una pérdida significativa de la DMO en el cuerpo entero menos la cabeza. Experiencia posterior a la comercialización: Se han identificado las siguientes reacciones adversas durante el uso de tenofovir DF con posterioridad a su aprobación. Debido a que las reacciones que aparecen en el período poscomercialización son notificadas voluntariamente por una población de tamaño indeterminado, no siempre es posible calcular su frecuencia de manera confiable ni establecer una relación causal con la exposición al fármaco. No se han identificado reacciones adversas adicionales específicas posteriores a la comercialización de emtricitabina. Trastornos en el sistema inmune: Reacción alérgica, incluyendo angioedema Trastornos del metabolismo y de la nutrición: Acidosis láctica, hipocalemia, hipofosfatemia Trastornos respiratorios, torácicos y mediastínicos Disnea Trastornos gastrointestinales: Pancreatitis, aumento de amilasa, dolor abdominal Trastornos hepatobiliares: Esteatosis hepática, hepatitis, aume
nto de enzimas en el hígado (más comúnmente AST, ALT, gamma GT) Trastornos de piel y tejido subcutáneo: Erupción. Trastornos musculoesqueléticos y del tejido conjuntivo: Rabdomiólisis, osteomalacia (manifestada como dolor óseo y que rara vez puede contribuir a fracturas), debilidad muscular, miopatía. Trastornos renales y urinarios: Insuficiencia renal aguda, insuficiencia renal, necrosis tubular aguda, síndrome de Fanconi, tubulopatía proximal renal, nefritis intersticial (incluidos casos agudos), diabetes insípida nefrogénica, insuficiencia renal, aumento de creatinina, proteinuria, poliuria. Trastornos generales y alteraciones del sitio de administración: Astenia. Las siguientes reacciones adversas, listadas bajo los encabezados del sistema orgánico, pueden acontecer como consecuencia de tubulopatía renal proximal: rabdomiólisis, osteomalacia, hipopotasemia, debilidad muscular, miopatía, hipofosfatemia.
Advertencias.
Generales: Exacerbación aguda grave de la hepatitis B en pacientes coinfectados con VIH-1 y VHB: Todos los pacientes con VIH-1 deben realizarse análisis para detectar la pre-silvestre mediante mutagénesis dirigida al sitio. De las sustituciones primarias asociadas con la resistencia al raltegravir (Y143C/H/R, Q148H/K/R y N155H), todas salvo Y143C/H redujeron más de 2,5 veces la susceptibilidad al elvitegravir (por encima del corte biológico para el elvitegravir). Emtricitabina: Se ha observado resistencia cruzada entre los INTR. Los aislamientos resistentes a emtricitabina que albergan una sustitución M184V/I en la TR del VIH-1 tuvieron resistencia cruzada para lamivudina. Los aislamientos de VIH-1 que contenían la sustitución K65R en la TR, seleccionadas in vivo por abacavir, didanosina, y tenofovir, demostraron susceptibilidad reducida a la sencia del virus de la hepatitis B (VHB) antes de iniciar la terapia antirretroviral [ver Dosificación]. STRIBILD® no está aprobado para el tratamiento de la infección crónica por el VHB y no se ha establecido la seguridad y la eficiencia de STRIBILD® en pacientes coinfectados con VIH-1y VHB. Se han informado exacerbaciones agudas graves de hepatitis B (p. ej., hepatopatía descompensada e insuficiencia hepática) en pacientes que están coinfectados con VIH-1 y VHB y han interrumpido emtricitabina o tenofovir DF, dos de los componentes de STRIBILD®. Debe realizarse un estricto control clínico y de laboratorio de los pacientes coinfectados con VIH-1 y VHB durante al menos varios meses después de la interrupción del tratamiento con los comprimidos de STRIBILD®. Si fuese adecuado, puede estar justificado el inicio de una terapia de tratamiento contra la hepatitis B, especialmente en pacientes con hepatopatía avanzada o cirrosis, ya que la exacerbación de la hepatitis después del tratamiento puede causar descompensación e insuficiencia hepática. Nueva aparición o empeoramiento de la disfunción renal: Se ha informado disfunción renal, incluyendo casos de falla renal aguda y síndrome de Fanconi (lesión tubular renal con hipofosfatemia grave) con el uso de tenofovir DF, un componente de STRIBILD®, y con el uso de STRIBILD® [Consulte Reacciones Adversas]. En los estudios clínicos de 144 semanas de duración con STRIBILD®, 13 (1,9 %) sujetos en el grupo de STRIBILD® (N=701), 8 (2,3 %) sujetos en el grupo de atazanavir (ATV)+ritonavir (RTV)+TRUVADA (emtricitabina y tenofovir DF) (N=355) y ningún sujeto en el grupo de ATRIPLA (efavirenz, emtricitabina y tenofovir DF) (N=352) suspendieron el uso del fármaco del estudio a causa de una reacción adversa renal. De estas suspensiones del tratamiento, 8 en el grupo de STRIBILD® y 1 en el grupo de ATV+RTV+TRUVADA (emtricitabina y tenofovir DF) se produjeron durante las primeras 48 semanas. Cuatro (0,6 %) sujetos que recibieron STRIBILD® presentaron hallazgos de laboratorio que concordaban con disfunción tubular renal proximal y que provocaron la suspensión del uso de STRIBILD® durante las primeras 48 semanas de tratamiento. Dos de los cuatro sujetos tenían disfunción renal (es decir, aclaramiento de creatinina estimado inferior a 70 ml por minuto) en la situación basal. Los hallazgos de laboratorio en estos 4 sujetos mejoraron al suspender el uso de STRIBILD®, pero no se resolvieron completamente en todos los sujetos. No se requirió tratamiento de reemplazo renal para estos sujetos. En un (0,3 %) sujeto que recibió ATV+RTV+TRUVADA (emtricitabina y tenofovir DF) se observaron hallazgos de laboratorio que concordaban con disfunción tubular renal proximal y que provocaron la suspensión del tratamiento con ATV+RTV+TRUVADA (emtricitabina y tenofovir DF) después de la semana 96. Debe evitarse administrar STRIBILD® con el uso reciente o concomitante de un fármaco nefrotóxico (p. ej., dosis altas de antiinflamatorios no esteroideos [AINE] o múltiples AINE) [ver Interacciones medicamentosas]. Se han notificado casos de insuficiencia renal aguda después de iniciar el uso de dosis altas de AINE o de múltiples AINE en pacientes infectados por el VIH con factores de riesgo de disfunción renal que se encontraban estables mientras recibían tenofovir DF. Algunos pacientes debieron ser hospitalizados y requirieron tratamiento de reemplazo renal. De ser necesario, deben considerarse alternativas a los AINE en los pacientes con riesgo de disfunción renal. La persistencia o el empeoramiento del dolor óseo, el dolor en las extremidades, las fracturas y/o el dolor o la debilidad muscular pueden ser manifestaciones de tubulopatía renal proximal y requieren una evaluación de la función renal en los pacientes de riesgo. Antes de iniciar el tratamiento y durante el uso de STRIBILD®, con un esquema clínico apropiado, evaluar la creatinina sérica, el aclaramiento estimado de creatinina, glucosa en orina y proteínas en orina en todos los pacientes. En los pacientes con enfermedad renal crónica, evaluar también el fósforo sérico. Suspender la administración de STRIBILD® en pacientes que desarrollan una disminución clínicamente significativa de la función renal o síndrome de Fanconi. No se recomienda iniciar el tratamiento con STRIBILD® en pacientes con aclaramiento estimado de creatinina por debajo de 70 mL por minuto [ver Dosificación)]. Aunque el cobicistat (un componente de STRIBILD®) puede causar ligeros aumentos en la creatinina sérica y leve disminución en el aclaramiento estimado de creatinina sin afectar la función glomerular renal [Consulte Reacciones Adversas (9.1)], los pacientes que experimentan un aumento confirmado de creatinina sérica mayor a 0,4 mg por dL respecto al inicio del tratamiento deben ser minuciosamente monitorizados por seguridad renal. Los componentes emtricitabina y tenofovir DF de STRIBILD® se excretan principalmente por el riñón. Se debe interrumpir STRIBILD® si el aclaramiento estimado de creatinina declina por debajo de 50 mL por minuto, ya que el ajuste del intervalo de dosis requerido para emtricitabina y tenofovir DF no se puede alcanzar con el comprimido de combinación de dosis fija [ver Uso en poblaciones específicas]. Acidosis láctica/Hepatomegalia severa con esteatosis: Se han informado casos de acidosis láctica y hepatomegalia grave con esteatosis, incluso casos mortales, con el uso de análogos de nucleósidos, incluido el tenofovir DF y emtricitabina, componentes de STRIBILD®, solos o en combinación con otros antirretrovirales. El tratamiento con STRIBILD® deberá ser suspendido en caso de que algún paciente desarrolle manifestaciones clínicas y/o parametros de laboratorio sugestivos de acidosis láctica o hepatotoxicidad pronunciada (que pueden incluir hepatomegalia y esteatosis incluso en ausencia de elevación de transaminasas). Riesgo de reacciones adversas o pérdida de la respuesta virológica debido a interacciones medicamentosas: El uso concomitante de STRIBILD® y otros fármacos puede ocasionar interacciones medicamentosas conocidas o posiblemente significativas, algunas de las cuales pueden provocar lo siguiente [ver Contraindicaciones, e Interacciones medicamentosas]: Pérdida del efecto terapéutico de STRIBILD® y posible desarrollo de resistencia. Reacciones adversas clínicamente significativas, que pueden conducir a eventos graves, potencialmente mortales o fatales, debido a una mayor exposición a fármacos concomitantes metabolizados por CYP3A. Pérdida del efecto terapéutico de los fármacos concomitantes que utilizan CYP3A para formar metabolitos activos. Consulte en la tabla 8 los pasos a seguir para prevenir o tratar estas interacciones medicamentosas significativas posibles y conocidas, incluidas las recomendaciones sobre la administración de las dosis [ver Interacciones medicamentosas]. Tenga en cuenta las posibles interacciones medicamentosas antes y durante el tratamiento con STRIBILD®; revise los medicamentos concomitantes durante el tratamiento con STRIBILD®; y monitoree la aparición de reacciones adversas asociadas con los fármacos concomitantes 7.1.5 Pérdida de masa ósea y defectos de mineralización: Densidad mineral ósea: En estudios clínicos realizados en adultos infectados por el VIH-1,el tenofovir DF (un componente de STRIBILD®) ha sido asociado con disminuciones ligeramente mayores en la densidad mineral ósea (DMO) y aumentos en marcadores bioquímicos de metabolismo óseo lo que sugiere mayor recambio óseo con respecto a los comparadores. Los niveles séricos de hormona paratiroidea y los niveles de vitamina D 1,25 también fueron mayores en los sujetos que recibieron tenofovir DF. Para obtener información adicional [ver Reacciones Adversas] consulte la información para prescribir de tenofovir DF. Se llevaron a cabo estudios clínicos en los que se evaluó el tenofovir DF en sujetos pediátricos y adolescentes. En circunstancias normales, la DMO aumenta rápidamente en los pacientes pediátricos. En los sujetos infectados por el VIH-1 de edad entre 2 y menos de 18 años, los efectos óseos fueron similares a los observados en los sujetos adultos y sugieren un mayor recambio óseo. La ganancia en la DMO del cuerpo entero fue menor en los sujetos pediátricos infectados por el VIH-1 que recibieron tratamiento con tenofovir DF en comparación con los grupos de control. En todos los estudios pediátricos, el crecimiento esquelético (estatura) no se vio afectado. Para obtener más información, consulte la ficha técnica del tenofovir DF. Se desconoce si los cambios asociados con el tenofovir DF en la DMO y los marcadores bioquímicos afectan la salud ósea a largo plazo y el riesgo futuro de fracturas. Debe considerarse la evaluación de la DMO en los pacientes adultos y pediátricos infectados por el VIH-1 que tienen antecedentes de fractura ósea patológica u otros factores de riesgo de osteoporosis o pérdida de masa ósea. Si bien no se ha estudiado el efecto de los suplementos de calcio y vitamina D, es posible que el uso de tales suplementos sea beneficioso para todos los pacientes. Se debe obtener asesoramiento adecuado si se sospecha la presencia de anomalías óseas. Defectos de mineralización: Se han informado casos de osteomalacia asociada con tubulopatía renal proximal, que se manifiesta como dolor óseo o dolor en las extremidades y que puede contribuir a las fracturas, en relación con el uso de tenofovir DF [ver Reacciones adversas]. También se han notificado artralgias y síntomas de dolor o debilidad muscular en los casos de tubulopatía renal proximal. Debe considerarse la posibilidad de que se produzcan hipofosfatemia y osteomalacia secundarias a la tubulopatía renal proximal en los pacientes con riesgo de disfunción renal que presenten persistencia o empeoramiento de los síntomas musculares u óseos mientras reciben productos que contienen tenofovir DF [ver Advertencias]. Síndrome de reconstitución inmune: Se ha informado el síndrome de reconstitución inmune en pacientes tratados con terapia antirretroviral combinada, incluyendo STRIBILD®. Durante la fase inicial del tratamiento antirretroviral combinado, los pacientes cuyo sistema inmune responde pueden presentar una respuesta inflamatoria a infecciones oportunistas indolentes o residuales [como infección por Mycobacterium avium, citomegalovirus, neumonía por Pneumocystis jirovecii (PCP), o tuberculosis], que pueden necesitar posterior evaluación y tratamiento. También se han informado trastornos autoinmunes (como enfermedad de Graves, polimiositis, síndrome de Guillain-Barré y hepatitis autoinmune) que aparecieron en el contexto de reconstitución inmune; no obstante, el tiempo hasta la aparición es más variable y puede producirse muchos meses después del inicio del tratamiento.
Interacciones.
No se recomienda usar con otros medicamentos antirretrovirales: STRIBILD® es un régimen completo para el tratamiento de la infección por el VIH-1; por ello, STRIBILD® no se debe administrar con otros fármacos antirretrovirales para el tratamiento de la infección por el VIH-1. No se proporciona la información completa con respecto a las interacciones fármaco-fármaco con otros medicamentos antirretrovirales [ver Contraindicaciones, Advertencias y Acción Farmacológica Farmacología Clínica]. Posibilidad de STRIBILD® de afectar a otros fármacos: Cobicistat, un componente de STRIBILD®, es un inhibidor de CYP3A y CYP2D6 y un inhibidor de los siguientes transportadores: p-glucoproteína (P-gp), BCRP, OATP1B1 y OATP1B3. De esta manera, la coadministración de STRIBILD® con fármacos que son principalmente metabolizados por CYP3A o CYP2D6, o son sustratos de P-gp, BCRP, OATP1B1 u OATP1B3 pueden causar aumento de la concentración en plasma de dichos medicamentos. La coadministración de STRIBILD® con medicamentos que tienen metabolitos activos formados por CYP3A puede resultar en una concentración plasmática reducida de estos metabolitos activos (Tabla 8). Elvitegravir es un modesto inductor de CYP2C9 y puede disminuir las concentraciones en plasma de sustratos de CYP2C9. Posibilidad de que otros fármacos afecten a uno o más componentes de STRIBILD®: Elvitegravir y cobicistat, componentes de STRIBILD®, son metabolizados por CYP3A. Cobicistat también es metabolizado, en menor grado, por CYP2D6. Se espera que los fármacos que inducen la actividad de CYP3A aumenten el aclaramiento de elvitegravir y cobicistat, produciendo una disminución de la concentración en plasma de cobicistat y elvitegravir, que puede conducir a la pérdida del efecto terapéutico de STRIBILD® y el desarrollo de resistencia (Tabla 8). La coadministración de STRIBILD® con otros fármacos que inhiben CYP3A puede disminuir el aclaramiento y aumentar la concentración en plasma de cobicistat (Tabla 8). Fármacos que afectan la función renal: Como la emtricitabina y el tenofovir, componentes de STRIBILD®, son principalmente excretados por los riñones por una combinación de filtración glomerular y secreción tubular activa, la coadministración de STRIBILD® con fármacos que reducen la función renal o compiten por la secreción tubular activa puede aumentar las concentraciones de emtricitabina, tenofovir, y otros fármacos que se eliminan por vía renal, lo cual puede incrementar el riesgo de reacciones adversas. Algunos ejemplos de fármacos que se eliminan por medio de secreción activa tubular, pero no están limitados a, son aciclovir, cidofovir, ganciclovir, valaciclovir, valganciclovir, aminoglucósidos (p. ej., gentamicina), y dosis altas de AINE o múltiples AINE [ver Advertencias]. Interacciones establecidas y otras interacciones potencialmente significativas: La Tabla 8 provee una lista de interacciones farmacológicas establecidas o potencialmente clínicamente significativas. Las interacciones de los fármacos descriptos se basan en estudios realizados con STRIBILD®, con los componentes de STRIBILD® (elvitegravir, cobicistat, emtricitabina y tenofovir DF) como agentes individuales y/o en combinación, o están previstas como interacciones de fármacos que pueden producirse con STRIBILD® [por magnitud de la interacción, consulte Farmacología Clínica]. La tabla incluye interacciones potencialmente significativas sin ser una enumeración exhaustiva [ver Contraindicaciones y Acción Farmacológica Farmacología Clínica].
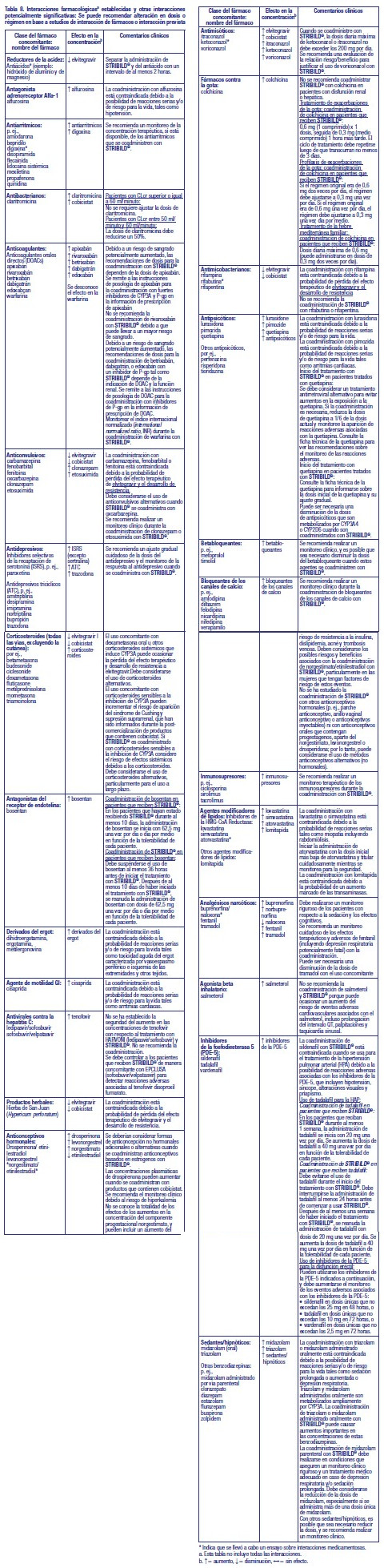
Fármacos sin interacciones clínicamente significativas con STRIBILD®: Basado en estudios de interacción de fármacos con los componentes de STRIBILD®, no se han observado ni se esperan interacciones de fármacos clínicamente significativas cuando STRIBILD® está combinado con los siguientes fármacos: famciclovir, famotidina, metadona, omeprazol, Prasugrel (metabolito activo) y sertralina. Carcinogénesis, Mutagénesis, trastornos de la Fertilidad: Elvitegravir: Se realizaron estudios de carcinogénesis a largo plazo de elvitegravir en ratones (104 semanas) y en ratas por hasta 88 semanas (machos) y 90 semanas (hembras). No se encontraron aumentos relacionados con el fármaco en la incidencia de tumores en ratones a dosis de hasta 2000 mg por kg por día solo o en combinación con 25 mg por kg por día de RTVa exposiciones de 3 y 14 veces, respectivamente, la exposición sistémica humana a la dosis diaria recomendada de 150 mg. No se encontraron aumentos relacionados con el fármaco en la incidencia de tumores en ratas a dosis de hasta 2000 mg por kg por día a exposiciones de 12 a 27 veces, respectivamente en macho y hembra, la exposición sistémica humana. Elvitegravir no fue genotóxico en la prueba bacteriana de mutación inversa (prueba de Ames) y en los estudios de micronúcleos en ratas. En una prueba de aberración cromosómica in vitro, elvitegravir fue negativo con la activación de metabolismo; sin embargo, se observó una respuesta equívoca sin activación. Elvitegravir no afectó la fertilidad en ratas machos y hembras en exposiciones mayores a, aproximadamente, 16 y 30 veces (ABC) respectivamente, la de humanos a la dosis terapéutica de 150 mg diarios. La fertilidad fue normal en las crías de ratas expuestas diariamente desde antes del nacimiento (in utero) hasta la maduración sexual a exposiciones diarias (ABC) de aproximadamente 18 veces mayores que las exposiciones en seres humanos con la dosis recomendada de 150 mg diarios. Cobicistat: En un estudio a largo plazo sobre la carcinogenicidad en ratones, no se observaron incrementos relacionados con el fármaco en la incidencia de tumores al administrar dosis de hasta 50 y 100 mg/kg/día (machos y hembras, respectivamente). Las exposiciones al cobicistat con estas dosis fueron aproximadamente 7 (machos) y 16 (hembras) veces mayores, respectivamente, que la exposición sistémica en seres humanos con la dosis terapéutica diaria. En un estudio a largo plazo sobre la carcinogenicidad del cobicistat en ratas, se observó un aumento en la incidencia de adenomas y/o carcinomas foliculares de la glándula tiroides al administrar dosis de 25 y 50 mg/kg/día en machos y dosis de 30 mg/kg/día en hembras. Se considera que los hallazgos sobre las células foliculares son específicos de las ratas, secundarios a la inducción de enzimas microsomales hepáticas y al desequilibrio hormonal tiroideo, y no son relevantes para los seres humanos. Con las dosis más altas evaluadas en el estudio sobre la carcinogenicidad en ratas, las exposiciones sistémicas fueron aproximadamente 2 veces mayores que la exposición sistémica en los seres humanos con la dosis terapéutica diaria. El cobicistat no fue genotóxico en la prueba bacteriana de mutación inversa (prueba de Ames), o en los estudios de linfoma de ratón o de micronúcleos en ratas. Cobicistat no afectó la fertilidad en ratas machos y hembras a exposiciones diarias (ABC) aproximadamente 4 veces mayores que las exposiciones humanas a dosis recomendadas de 150 mg diarios. La fertilidad fue normal en las crías de ratas expuestas diariamente desde antes del nacimiento (in utero) hasta la maduración sexual a exposiciones diarias (ABC) aproximadamente 1,2 veces mayores que las exposiciones en seres humanos con la dosis recomendada de 150 mg diarios. Emtricitabina: En estudios de carcinogenicidad a largo plazo de emtricitabina, no se encontraron aumentos en la incidencia tumoral relacionados con el fármaco en ratones con dosis de hasta 750 mg por kg por día (23 veces la exposición sistémica para seres humanos en la dosis terapéutica de 200 mg por día) ni en ratas con dosis de hasta 600 mg por kg por día (28 veces la exposición sistémica para seres humanos en la dosis terapéutica). La emtricitabina no fue genotóxica en la prueba bacteriana de mutación inversa (prueba de Ames), o en los estudios de linfoma de ratón y de micronúcleos en ratón. La emtricitabina no afectó la fertilidad de las ratas macho con exposiciones aproximadamente 140 veces superiores, ni en ratones machos y hembras con exposiciones aproximadamente 60 veces más altas (ABC) a la de los seres humanos que reciben la dosis recomendada de 200 mg diarios. La fertilidad fue normal en las crías de ratones expuestas diariamente desde antes del nacimiento (in utero) hasta la maduración sexual a exposiciones diarias (ABC) aproximadamente 60 veces más altas que las exposiciones en seres humanos con la dosis recomendada de 200 mg diarios. Tenofovir DF: Los estudios a largo plazo de la carcinogenicidad oral de tenofovir DF en ratas y ratones se llevaron a cabo con exposiciones de hasta aproximadamente 10 veces (ratones) y 4 veces (ratas) más que las observadas en seres humanos a una dosis terapéutica para infección porel VIH-1. En la dosis alta en ratones hembra, se incrementaron los adenomas de hígado a exposiciones de 10 veces la de los humanos. En ratas, el estudio fue negativo para descubrimientos carcinogénicos a exposiciones hasta 4 veces la observada en humanos en dosis terapéuticas. Tenofovir DF fue mutagénico en el estudio in vitro de linfoma de ratón y negativo en una prueba in vitro de mutagenicidad bacteriana (prueba de Ames). En un estudio in vivo de micronúcleo en ratones, el tenofovir DF resultó negativo cuando se administró a ratones machos. No hubo efectos en la fertilidad, la capacidad de apareamiento ni el desarrollo embrionario temprano cuando se administró tenofovir DF a ratas macho en una dosis equivalente a 10 veces la dosis para seres humanos según comparaciones del área de superficie corporal durante 28 días antes del apareamiento y a ratas hembra durante 15 días antes del apareamiento hasta el séptimo día de gestación. Hubo, sin embargo, una alteración del ciclo estral en las ratas hembras. Uso en poblaciones específicas: Embarazo: Registro de exposiciones durante el embarazo: Existe un registro de exposiciones durante el embarazo que supervisa los desenlaces clínicos de los embarazos en mujeres expuestas a STRIBILD® durante su embarazo. Se promueve el registro de pacientes por parte de los médicos en el registro de embarazos con antirretrovirales (Antiretroviral Pregnancy Registry, APR) mundial www.apregistry.com, o la comunicación de los médicos al +54 11 4858 9000 o a farmacovigilancia@gador.com. Resumen de riesgos: No se recomienda el uso de STRIBILD® durante el embarazo [ver Dosificación]. Un informe de la literatura que evaluó la farmacocinética (FC) de los antirretrovirales durante el embarazo demostró exposiciones sustancialmente menores de elvitegravir y cobicistat en el segundo y el tercer trimestres (ver Datos). Los datos prospectivos sobre los embarazos que figuran en el APR no son suficientes para evaluar adecuadamente el riesgo de defectos congénitos o abortos espontáneos. Sin embargo, se ha evaluado el uso de elvitegravir, cobicistat, emtricitabina y tenofovir DF durante el embarazo en una cantidad limitada de mujeres que se registraron en el APR. Los datos disponibles en el APR, no muestran una diferencia significativa en el riesgo general de defectos congénitos importantes por el elvitegravir, el cobicistat, la emtricitabina o el tenofovir DF en comparación con la tasa prevalente de defectos congénitos importantes del 2,7 % en una población estadounidense de referencia estudiada en el Programa metropolitano de Atlanta sobre defectos congénitos (Metropolitan Atlanta Congenital Defects Program, MACDP ver Datos). La tasa de abortos espontáneos no ha sido informada en el APR. En la población general estadounidense el riesgo prevalente estimado de abortos espontáneos en embarazos clínicamente confirmados es de 15-20%. En los estudios con animales, no se observaron efectos adversos en el desarrollo al administrar los componentes de STRIBILD® por separado durante el período de organogénesis, con exposiciones hasta 23 y 0,2 veces (elvitegravir en ratas y conejos, respectivamente), 1,8 y 4,3 veces (cobicistat en ratas y conejos, respectivamente), y 60 y 120 veces (emtricitabina en ratones y conejos, respectivamente) mayores que la exposición con la dosis diaria recomendada de estos componentes incluidos en STRIBILD®; ni con exposiciones 14 y 19 veces (tenofovir DF en ratas y conejos, respectivamente) mayores que la dosis para seres humanos, sobre la base de comparaciones de la superficie corporal [ver Datos]. Del mismo modo, tampoco se observaron efectos adversos en el desarrollo al administrar elvitegravir o cobicistat a ratas hasta la lactancia, con exposiciones hasta 18 o 1,2 veces mayores, respectivamente, que la exposición con la dosis terapéutica diaria recomendada, ni al administrar emtricitabina a ratones hasta la lactancia, con exposiciones aproximadamente hasta 60 veces mayores que la exposición con la dosis terapéutica diaria recomendada. No se observaron efectos adversos en las crías de ratas al administrar tenofovir DF hasta la lactancia, con exposiciones al tenofovir aproximadamente 2,7 veces mayores que la exposición con la dosis diaria recomendada de STRIBILD®. Datos: Datos en seres humanos: Un estudio prospectivo informado en la literatura, registró 30 mujeres embarazadas que tenían VIH que recibían regímenes basados en elvitegravir y cobicistat en el segundo o el tercer trimestres del embarazo y durante 6 a 12 semanas postparto para evaluar la farmacocinética (FC) de los antirretrovirales durante el embarazo. Veintiocho mujeres completaron el estudio hasta el período postparto. Los datos de FC pareados de embarazo/postparto se encontraban disponibles de 14 y 24 mujeres para el segundo y el tercer trimestres, respectivamente. Las exposiciones de elvitegravir y cobicistat eran sustancialmente más bajas durante el segundo y el tercer trimestres en comparación con el postparto. La proporción de mujeres embarazadas que estaban virológicamente suprimidas fue de 77% en el segundo trimestre, 92% en el tercer trimestre, y 76% postparto. No se observó una correlación entre la supresión viral y la exposición a elvitegravir. El estado de VIH también fue evaluado para los bebés: 25 no estaban infectados, 2 tenían un estado indeterminado y no se encontraba disponible información para 3 bebés. Los informes prospectivos del APR de defectos congénitos importantes en general en embarazos expuestos a los componentes de STRIBILD® son comparados con la tasa de defectos congénitos importantes prevalentes en los EE.UU. Las limitaciones metodológicas del APR incluyen el uso de MACDP como el grupo comparador externo. La población de MACDP no es específica de la enfermedad, evalúa a mujeres y bebés de un área geográfica limitada y no incluye los resultados de los nacimientos que ocurrieron antes de las 20 semanas de gestación. Elvitegravir: Basados en informes prospectivos al APR sobre exposiciones durante el embarazoa esquemas terapéuticos con elvitegravir durante embarazos que resultaron en nacimientos con vida (incluyendo mas de 300 expuestos durante el primer trimestre y mas de 60 expuestos durante el segundo y tercer trimestre) la prevalencia de defectos de nacimiento en los nacidos vivos fue del 3,4% (IC del 95%: 1,7% a 6,0%) y del 1,5% (IC del 95%: 0% a 7,9%) después de la exposición al primer y segundo / tercer trimestre, respectivamente, a los regímenes que contenían elvitegravir. Cobicistat: Basados en informes prospectivos al APR sobre exposiciones durante el embarazo a esquemas terapéuticos con cobicistat durante embarazos que resultaron en nacimientos con vida (incluyendo mas de 400 expuestos durante el primer trimestre y mas de 80 expuestos durante el segundo y tercer trimestre) la prevalencia de defectos de nacimiento en los nacidos vivos fue del 3,9% (IC del 95%: 2,3% a 6,0%) y del 1,2% (IC del 95%: 0% a 6,5%) después de la exposición al primer y segundo / tercer trimestre., respectivamente, a los regímenes que contenían cobicistat. Emtricitabina: Basados en informes prospectivos al APR sobre exposiciones durante el embarazo a esquemas terapéuticos con emtricitabina durante embarazos que resultaron en nacimientos con vida (incluyendo mas de 3600 expuestos durante el primer trimestre y mas de 1400 expuestos durante el segundo y tercer trimestre) la prevalencia de defectos de nacimiento en los nacidos vivos fue del 2,6% (IC del 95%: 2,1% a 3,2%) y del 2,4% (IC del 95%: 1% a 3,3%) después de la exposición al primer y segundo / tercer trimestre., respectivamente, a los regímenes que contenían emtricitabina. Tenofovir DF: Basados en informes prospectivos al APR sobre exposiciones durante el embarazo a esquemas terapéuticos con TDF durante embarazos que resultaron en nacimientos con vida (incluyendo mas de 4200 expuestos durante el primer trimestre y mas de 1800 expuestos durante el segundo y tercer trimestre) la prevalencia de defectos de nacimiento en los nacidos vivos fue del 2,4% (IC del 95%: 1,9% a 2,9%) y del 2,4% (IC del 95%: 1,8% a 3,2%) después de la exposición al primer y segundo / tercer trimestre, respectivamente, a los regímenes que contenían tenofovir DF. Datos animales: Elvitegravir: Se administró elvitegravir por vía oral a ratas preñadas (en dosis de 0, 300, 1000 y 2000 mg/kg/día) y a conejas preñadas (en dosis de 0, 50, 150 y 450 mg/kg/día) hasta la organogénesis (los días 7 a 17 y los días 7 a 19 de gestación, respectivamente). No se observaron efectos toxicológicos significativos en los estudios de toxicidad embriofetal realizados con el elvitegravir en ratas con exposiciones (área bajo la curva [ABC]) aproximadamente 23 veces más altas ni en conejos con exposiciones aproximadamente 0,2 veces más altas que las exposiciones en seres humanos con la dosis diaria recomendada. En un estudio sobre el desarrollo prenatal/posnatal en ratas, se administró elvitegravir por vía oral en dosis de 0, 300, 1000 y 2000 mg/kg desde el día 7 de gestación hasta el día 20 de lactancia. Con dosis de 2000 mg/kg/día de elvitegravir, no se observó toxicidad materna ni del desarrollo. Las exposiciones sistémicas (ABC) con esta dosis fueron 18 veces mayores que las exposiciones en seres humanos con la dosis diaria recomendada. Cobicistat: Se administró cobicistat por vía oral a ratas preñadas en dosis de 0, 25, 50 y 125 mg/kg/día los días 6 a 17 de gestación. Se observaron aumentos en la pérdida de la preñez con posterioridad a la implantación y reducciones en el peso fetal al administrar la dosis de 125 mg/kg/día que provoca toxicidad materna. No se observaron malformaciones al administrar dosis de hasta 125 mg/kg/día. Las exposiciones sistémicas (ABC) tras administrar 50 mg/kg/día a hembras preñadas fueron 1,8 veces más altas que las exposiciones en seres humanos con la dosis diaria recomendada. En conejas preñadas, se administró cobicistat por vía oral en dosis de 0, 20, 50 y 100 mg/kg/día durante los días 7 a 20 de gestación. No se observaron efectos maternos ni embriofetales al administrar la dosis más alta de 100 mg/kg/día. Las exposiciones sistémicas (ABC) tras administrar 100 mg/kg/ día fueron 4,3 veces más altas que las exposiciones en seres humanos con la dosis diaria recomendada. En un estudio sobre el desarrollo prenatal/posnatal en ratas, se administró cobicistat por vía oral en dosis de 0, 10, 30 y 75 mg/kg desde el día 6 de gestación hasta los días 20, 21 o 22 posnatales. Con dosis de 75 mg/kg/día de cobicistat, no se observó toxicidad materna ni del desarrollo. Las exposiciones sistémicas (ABC) con esta dosis fueron 1,2 veces mayores que las exposiciones en seres humanos con la dosis diaria recomendada. Emtricitabina: Se administró emtricitabina por vía oral a ratas preñadas (en dosis de 0, 250, 500 o 1000 mg/kg/día) y a conejas preñadas (en dosis de 0, 100, 300 o 1000 mg/kg/día) hasta la organogénesis (los días 6 a 15 y los días 7 a 19 de gestación, respectivamente). No se observaron efectos toxicológicos significativos en los estudios de toxicidad embriofetal realizados con la emtricitabina en ratones con exposiciones (ABC) aproximadamente 60 veces más altas ni en conejos con exposiciones aproximadamente 120 veces más altas que las exposiciones en seres humanos con la dosis diaria recomendada. En un estudio sobre el desarrollo prenatal/posnatal en ratones, se administró emtricitabina por vía oral en dosis de hasta 1000 mg/kg/día; no se observaron efectos adversos significativos directamente relacionados con el fármaco en las crías expuestas a diario desde antes del nacimiento (exposición intrauterina) hasta la madurez sexual, con exposiciones diarias (ABC) aproximadamente 60 veces más altas que las exposiciones en seres humanos con la dosis diaria recomendada. Tenofovir DF: Se administró tenofovir DF por vía oral a ratas preñadas (en dosis de 0, 50, 150 o 450 mg/kg/día) y a conejas preñadas (en dosis de 0, 30, 100 o 300 mg/kg/día) hasta la organogénesis (los días 7 a 17 y los días 6 a 18 de gestación, respectivamente). No se observaron efectos toxicológicos significativos en los estudios de toxicidad embriofetal realizados con el tenofovir DF en ratas tratadas con dosis hasta 14 veces mayores que la dosis para seres humanos, sobre la base de comparaciones de la superficie corporal, ni en conejos tratados con dosis hasta 19 veces mayores que la dosis para seres humanos, sobre la base de comparaciones de la superficie corporal. En un estudio sobre el desarrollo prenatal/posnatal en ratas, se administró tenofovir DF por vía oral hasta la lactancia en dosis de hasta 600 mg/kg/día; no se observaron efectos adversos en las crías tras exposiciones al tenofovir aproximadamente 2,7 veces más altas que las exposiciones en seres humanos con la dosis diaria recomendada de STRIBILD®. Lactancia: Resumen de los riesgos: Se recomienda que las madres infectadas con VIH no amamanten a sus hijos para evitar el riesgo de transmisión postnatal del VIH. Los estudios en ratas han demostrado que elvitegravir, cobicistat y tenofovir son excretados en la leche. Se desconoce si el elvitegravir o el cobicistat se excretan en la leche materna humana. De acuerdo con la limitada cantidad de datos publicados, se ha demostrado que la emtricitabina y el tenofovir están presentes en la leche materna humana. No se sabe si el elvitegravir o el cobicistat están presentes en la leche materna humana, aunque sí se ha observado la presencia de elvitegravir y cobicistat en la leche de ratas (ver Datos). No se sabe si los componentes de STRIBILD® afectan a la producción de leche o si producen efectos en el bebé amamantado. Se debe indicar a las madres que no amamanten a sus hijos si están recibiendo STRIBILD®, debido a la posibilidad de: (1) transmisión del VIH (en lactantes VIH negativos); (2) desarrollo de resistencia viral (en lactantes VIH positivos); y (3) reacciones adversas en el bebé amamantado, similares a las observadas en los adultos (ver Datos). Datos en animales: Elvitegravir: Durante el estudio toxicológico sobre el desarrollo prenatal y posnatal con dosis de hasta 2000 mg/kg/día, la media de la relación leche: plasma del elvitegravir fue de 0,1 al medirse 30 minutos después de la administración a ratas el día 14 de lactancia. Cobicistat: Durante el estudio toxicológico sobre el desarrollo prenatal y posnatal con dosis de hasta 75 mg/kg/día, la media de la relación leche: plasma del cobicistat fue de hasta 1,9 al medirse 2 horas después de la administración a ratas el día 10 de lactancia. Uso pediátrico: Se evaluaron la farmacocinética, la seguridad, y las respuestas virológicas e inmunológicas en 50 sujetos infectados por el VIH-1 sin tratamiento previo, de edad entre 12 y menos de 18 años, que pesaban al menos 35 kg (77 lb) y que recibieron STRIBILD® durante 48 semanas en un ensayo abierto (estudio 112). La seguridad y la eficacia de STRIBILD® en estos sujetos fueron similares a las de los adultos sin tratamiento antirretroviral previo [ver Dosificación, Reacciones adversas, Acción Farmacológica Farmacología Clínica y Estudios clínicos]. No se ha establecido la seguridad y efectividad de STRIBILD® en pacientes pediátricos menores a 12 años de edad o cuyo peso es inferior a 35 kg (77 lb) [Consulte Acción Farmacológica - Farmacología Clínica]. Uso geriátrico: Los estudios clínicos de STRIBILD® no incluyeron números suficientes de sujetos de 65 años o mayores para determinar si respondían de manera diferente a los sujetos más jóvenes. En general, se debe tener precaución al administrar STRIBILD® en los pacientes de edad avanzada, teniendo en cuenta la mayor frecuencia de disminución de las funciones hepática, renal o cardíaca y de enfermedades concomitantes u otra terapia con fármacos [Consulte Acción Farmacológica - Farmacología Clínica]. Insuficiencia renal: No se recomienda iniciar el tratamiento con STRIBILD® en pacientes con aclaramiento estimado de creatinina por debajo de 70 mL por minuto. Como STRIBILD® es un comprimido de combinación de dosis fija, STRIBILD® debe interrumpirse si el aclaramiento estimado de creatinina declina por debajo de 50 mL por minuto durante el tratamiento con STRIBILD®, ya que no se puede alcanzar el ajuste de intervalo de dosis requerido para emtricitabina y tenofovir DF [Consulte Advertencias, Reacciones Adversas, Acción Farmacológica Farmacología Clínica, y Estudios Clínicos]. No hay datos disponibles que determinen recomendaciones posológicas para pacientes pediátricos con disfunción renal. Estudios clínicos en sujetos adultos con disfunción renal de leve a moderada En el estudio 118, se examinaron 33 sujetos infectados por el VIH-1 sin tratamiento previo que tenían disfunción renal de leve a moderada (TFGe mediante el método de Cockcroft-Gault entre 50 y 89 ml/minuto) en un ensayo clínico abierto donde se evaluó la seguridad del tratamiento con STRIBILD® durante 48 semanas. Después de 48 semanas de tratamiento, el cambio medio en la creatinina sérica fue de 0,17 ± 0,14 mg/dl, y el cambio medio en la TFGe mediante el método de Cockcroft-Gault fue de -6,9 ± 9,0 ml/minuto para los sujetos tratados con STRIBILD®. Doce de los 33 sujetos estudiados tenían un valor basal de TFGe de entre 50 y 70 ml/minuto. Tres sujetos, todos con un valor basal de TFGe de 50-60 ml/minuto, suspendieron el tratamiento con STRIBILD® debido a un evento adverso renal. La seguridad de STRIBILD® en 21 de los 33 sujetos con un valor basal de TFGe superior o igual a 70 ml/minuto concordó con el perfil de seguridad observado en los estudios 102 y 103. Insuficiencia hepática: No se requiere ajuste de dosis de STRIBILD® en pacientes con insuficiencia hepática leve (Clase A de Child-Pugh) o moderada (Clase B de Child-Pugh). No se dispone de datos farmacocinéticos o de seguridad con respecto al us

