RAPAMUNE
PFIZER
Comprimidos recubiertos
Agente inmunosupresor.
Composición.
Cada comprimido recubierto contiene: Rapamune 0,5 mg: Sirolimus (NanoCrystal®) 0,5 mg. Azúcar 215,7 mg. Lactosa 86,4 mg. Polietilenglicol 8000: 28,8 mg. Sulfato de calcio 10,7 mg. Celulosa microcristalina 7,83 mg. Shellac 5,62 mg. Talco 4,20 mg. Poloxamer 0,255 mg. Dióxido de titanio 1,95 mg. Estearato de magnesio 0,600 mg. Povidona 0,587 mg. Polietilenglicol 20000: 0,300 mg. Vitamina E 0,051 mg. Monooleato de glicerilo 0,150 mg. Cera carnauba 0,079 mg. Óxido de hierro amarillo 0,154 mg. Óxido de hierro marrón 0,062 mg. Rapamune 1 mg: Sirolimus (NanoCrystal®) 1 mg. Azúcar 215,8 mg. Lactosa 86,4 mg. Polietilenglicol 8000 28,8 mg. Sulfato de calcio 10,7 mg. Celulosa microcristalina 8,034 mg. Shellac 5,62 mg. Talco 4,20 mg. Poloxamer 0,51 mg. Dióxido de titanio 1,023 mg. Estearato de magnesio 0,600 mg. Povidona 0,587 mg. Polietilenglicol 20000: 0,300 mg. Vitamina E 0,051 mg. Monooleato de glicerilo 0,150 mg. Cera carnauba 0,079 mg. Rapamune 2 mg: Sirolimus (NanoCrystal®) 2 mg. Azúcar 214,38 mg. Lactosa 86,4 mg. Polietilenglicol 8000 28,8 mg. Sulfato de calcio 10,7 mg. Celulosa microcristalina 7,73 mg. Shellac 5,62 mg. Talco 4,20 mg. Poloxamer 1,02 mg. Dióxido de titanio 1,14 mg. Estearato de magnesio 0,600 mg. Povidona 0,587 mg. Polietilenglicol 20000: 0,300 mg. Vitamina E 0,051 mg. Monooleato de glicerilo 0,150 mg. Cera carnauba 0,079 mg. Óxido de hierro amarillo 0,092 mg. Óxido de hierro marrón 0,012 mg.
Farmacología.
Descripción: Rapamune (sirolimus) es un agente inmunosupresivo. El sirolimus es una lactona macrocíclica producida por el Streptomyces hygroscopicus, cuyo nombre químico es: (3S, 6R, 7E, 9R, 10R, 12R, 14S, 15E, 17E, 19E, 21S, 23S, 26R, 27R, 34aS) 9, 10, 12, 13, 14, 21, 22, 23, 24, 25, 26, 27, 32, 33, 34, 34a -hexadecahidro - 9, 27 - dihidroxi -3 - [(1R) - 2 - [(1S, 3R, 4R) - 4 - hidroxi - 3 - metoxiciclohexil] - 1 - metiletil] - 10, 21 - dimetoxi - 6, 8, 12, 14, 20, 26 - hexametil - 23, 27 - epoxi - 3H - pirido [2,1-c] [1,4] oxaazaciclohentriacontina -1, 5, 11, 28, 29 (4H,6H,31H) - pentona. Su fórmula molecular es C51H79NO13 y su peso molecular 914,2. A continuación, figura la fórmula estructural del sirolimus.
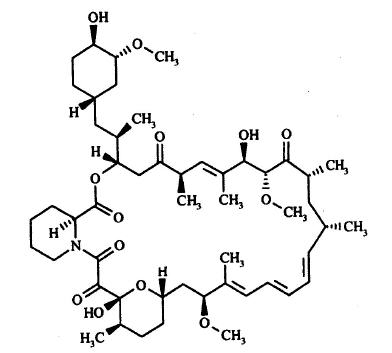
Sirolimus es un polvo blanco a blancuzco y es insoluble en agua pero soluble en alcohol bencílico, cloroformo, acetona y acetonitrilo. Mecanismo de acción: El sirolimus inhibe la activación y proliferación de los linfocitos T que se producen como respuesta a la estimulación inducida por antígenos y citoquinas (interleucina [IL]-2, IL-4 e IL-15), por un mecanismo diferente del observado con otros inmunosupresores. El sirolimus también inhibe la producción de anticuerpos. En las células, el sirolimus se une a la inmunofilina, proteína ligadora de la FK-12 (FK Binding Protein-12, FKBP-12), para generar un complejo inmunosupresor. El complejo sirolimus: FKBP-12 no ejerce efecto alguno sobre la actividad de la calcineurina. Este complejo se une e inhibe la activación del "objetivo de la rapamicina" de los mamíferos (mammallian Target of Rapamycin, mTOR), una quinasa reguladora importante. Esta inhibición suprime la proliferación de las células T inducida por las citoquinas, inhibiendo así la progresión de las fases G1 a S del ciclo celular. Los estudios llevados a cabo en modelos experimentales en ratones, ratas, cerdos, perros y/o monos sobrevivientes, muestran que el sirolimus prolonga la sobrevida de los injertos (riñón, corazón, piel, células de islotes, intestino delgado, pancreático-duodenal y médula ósea). El sirolimus previene el rechazo agudo de los aloinjertos de corazón y riñón en ratas y prolonga la sobrevida del órgano en ratas presensibilizadas. En algunos estudios, el efecto inmunosupresor del sirolimus perduró hasta seis meses después de la interrupción del tratamiento. Este efecto de tolerancia es específico para los aloantígenos. En modelos (roedores) con enfermedad autoinmune, el sirolimus suprime los eventos mediados por fenómenos inmunológicos asociados con: lupus eritematoso sistémico, artritis inducida por colágeno, diabetes autoinmune tipo I, miocarditis autoinmune, encefalomielitis alérgica experimental, enfermedad injerto versus huésped y uveorretinitis autoinmune. La linfangioleiomiomatosis consiste en la infiltración del tejido pulmonar con células similares a las del músculo liso, que albergan mutaciones inactivadoras del gen del complejo de esclerosis tuberosa (TSC) (células LAM). La pérdida de la función del gen TSC activa la ruta de señalización mTOR, dando como resultado la proliferación celular y la liberación de factores de crecimiento linfangiogénicos. Sirolimus inhibe la vía mTOR activada y, por tanto, la proliferación de células LAM. Farmacodinamia: La administración por vía oral de Rapamune, a dosis de 2 mg/día y 5 mg/día, redujo significativamente la incidencia de rechazo de órganos en pacientes con trasplante renal de leve a moderado riesgo inmunológico a los 6 meses tras el trasplante, en comparación con azatioprina o placebo (ver Estudios Clínicos). No hubo ninguna ventaja demostrable en la eficacia de una dosis de mantenimiento diaria de 5 mg con una dosis de carga de 15 mg sobre una dosis de mantenimiento diaria de 2 mg con una dosis de carga de 6 mg. El monitoreo terapéutico del fármaco debe usarse para mantener los niveles de sirolimus dentro del rango objetivo (ver Dosificación). Farmacocinética: La actividad farmacocinética de sirolimus, ha sido determinada luego de la administración en pacientes sanos, pacientes pediátricos, pacientes con deterioro hepático y pacientes con trasplante renal. Los parámetros farmococinéticos de sirolimus en pacientes adultos con trasplante renal después de la administración de dosis múltiples de Rapamune 2 mg, en combinación con ciclosporina y corticoides, se resumen en la siguiente tabla.
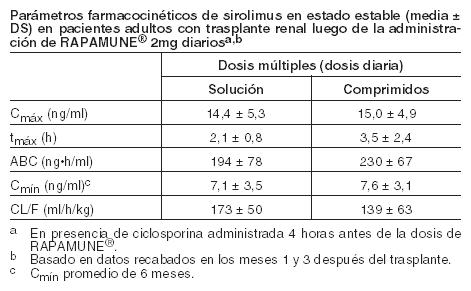
Las concentraciones mínimas de sirolimus en sangre entera, determinadas por Cromatografía Líquida/Espectrometría de masas en tándem (LC/MS/MS), se correlacionaron significativamente con el ABCt,ss. Luego de la administración repetida dos veces al día sin dosis inicial de carga en un estudio de dosis múltiples, la concentración mínima promedio de sirolimus aumenta aproximadamente 2 a 3 veces en los primeros 6 días de tratamiento, tiempo en el que alcanza el estado estable. Una dosis de carga 3 veces superior a la dosis de mantenimiento proporcionará concentraciones cercanas al estado estable dentro de las 24 horas en la mayoría de los pacientes (ver Dosificación y Advertencias). Absorción: Luego de la administración de Rapamune (sirolimus) Solución Oral, el sirolimus se absorbe rápidamente. El tiempo medio hasta alcanzar la concentración máxima (Cmáx) es de aproximadamente una hora después de una dosis única en pacientes sanos y de aproximadamente dos horas después de dosis orales múltiples en pacientes con trasplante renal. Luego de la administración de Rapamune comprimidos en pacientes sanos, la biodisponibilidad media de sirolimus fue aproximadamente un 27% más alto en relación a la solución. Los comprimidos de sirolimus no son bioequivalentes a la solución; sin embargo, la equivalencia clínica ha sido demostrada a un nivel de dosis de 2 mg. La concentración de sirolimus, luego de la administración de Rapamune Solución Oral en pacientes con trasplante renal estable, son dosis proporcionales, entre 3 y 12 mg/m2. Efectos de los alimentos: Para minimizar la variabilidad en las concentraciones de sirolimus, tanto Rapamune Oral Solución como los comprimidos deben tomarse consistentemente con o sin alimentos (ver Dosificación). En sujetos sanos, una comida rica en grasa (861,8 kcal, 54,9% kcal de grasa) aumentó la exposición total media (ABC) del sirolimus en un 23 a 35%, en comparación con el ayuno. El efecto del alimento sobre la Cmáx media del sirolimus fue inconsistente dependiendo de la forma de dosificación de Rapamune evaluada. Distribución: La relación sangre/plasma del sirolimus (± DE) fue 36 (± 18) en pacientes con trasplante renal alogénico estables, observándose que el sirolimus se distribuye en forma extensiva en los distintos elementos de la sangre. El volumen medio de distribución (Vss/F) del sirolimus con la administración de Rapamune es de 12 ± 8 l/kg. En los seres humanos, el sirolimus se une extensamente a las proteínas plasmáticas (aproximadamente 92 %). En el hombre, se demostró que la unión del sirolimus se encuentra asociada principalmente a la albúmina sérica (97 %), a la glucoproteína ácida a1 y a las lipoproteínas. Metabolismo: El sirolimus constituye un sustrato adecuado, tanto para el citocromo P450 IIIA4 (CYP3A4), como para la glucoproteína P. Sirolimus es metabolizado en forma extensiva en la pared instestinal e hígado y es transportado desde los enterocitos del intestino delgado al lumen del intestino. Los inhibidores de CYP3A4 y glucoproteína P aumentan las concentraciones de sirolimus. Los inductores de CYP3A4 y glucoproteína P disminuyen las concentraciones de sirolimus (ver Advertencias e Interacciones). El sirolimus es metabolizado en forma extensiva por O-desmetilación y/o por hidroxilación. En la sangre entera, se pueden identificar siete (7) metabolitos principales, incluyendo los derivados hidroxi, desmetil e hidroxidesmetil. Algunos de estos metabolitos también pueden detectarse en las muestras de plasma, de materia fecal y urinarias. Los glucurónidos y los sulfatos conjugados no se encuentran presentes en ninguna de las matrices biológicas. En los seres humanos, el sirolimus constituye el principal componente en la sangre entera y contribuye en más del 90 % con la actividad inmunosupresora. Excreción: Después de la administración de una dosis única de sirolimus [C14] a voluntarios sanos, la mayor parte de la radioactividad (91 %) fue recuperada en las heces y solamente una pequeña cantidad (2,2 %) se excretó en la orina. La vida media de eliminación terminal (t1/2) promedio ± DS del sirolimus después de dosis múltiples de Rapamune solución oral en pacientes estables con trasplante renal fue de alrededor de 62 ± 16 horas. Concentraciones de sirolimus (equivalencias cromatográficas) observadas en estudios clínicos de Fase 3: Las siguientes concentraciones de sirolimus (equivalencias cromatográficas) se observaron en estudios clínicos de Fase 3, para profilaxis del rechazo de órganos en pacientes con trasplante renal de novo (ver Estudios Clínicos).
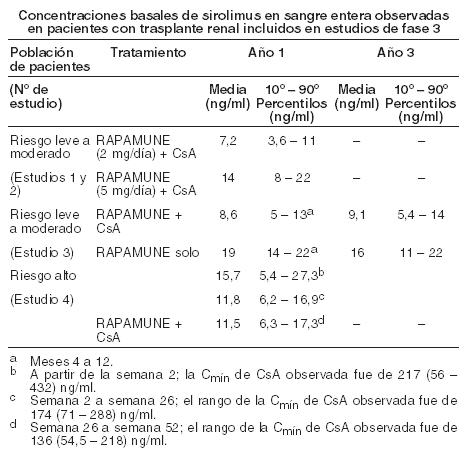
La discontinuación de la ciclosporina y los aumentos simultáneos en las concentraciones mínimas de sirolimus hasta el estado de equilibrio requerían aproximadamente 6 semanas. Tras la discontinuación de la ciclosporina, se requirieron dosis más altas de Rapamune debido a la ausencia de inhibición del metabolismo del sirolimus y el transporte por ciclosporina y para lograr concentraciones de referencia más altas de sirolimus durante la administración controlada por concentración (ver Dosificación e Interacciones). Linfangioleiomiomatosis: En un estudio clínico en pacientes con linfangioleiomiomatosis, la concentración media de sirolimus en sangre entera, luego de 3 semanas recibiendo comprimidos de sirolimus a dosis de 2 mg/día, fue de 6,8 ng/ml (rango intercuartil 4,6 a 9,0 ng/ml; n = 37). Farmacocinética en poblaciones especiales: Pacientes con compromiso hepático: Se administró Rapamune solución oral (15 mg) como dosis oral única a sujetos con función hepática normal y a pacientes con deterioro hepático primario grado A (leve), B (moderado) o C (severo) de la clasificación de Child-Pugh. En comparación con los valores del grupo con función hepática normal, el grupo con compromiso hepático leve, moderado y severo presentaron valores medios del 43 %, 94 % y 189 % más altos de ABC respectivamente, sin diferencias significativas estadísticamente en la Cmáx media. A medida que la severidad del deterioro de la función hepática, hubo aumentos constantes en la media de sirolimus t1/2, y disminuciones en la eliminación media de sirolimus normalizado para el peso corporal (CL/ F/kg). Deberá reducirse la dosis de mantenimiento de Rapamune en aproximadamente un tercio en pacientes con compromiso hepático leve a moderado y en aproximadamente un medio en pacientes con compromiso hepático severo (ver Dosificación). No es necesario en pacientes con compromiso hepático leve, moderado o severo modificar la dosis de carga de Rapamune. Deberá considerarse necesario el monitoreo en todos los pacientes con disfunción hepática (ver Dosificación). Pacientes con disfunción renal: No se conoce el efecto de la insuficiencia renal sobre la farmacocinética del sirolimus. Sin embargo, existe un mínimo (2,2%) de excreción renal del fármaco o de sus metabolitos en voluntarios sanos. Las dosis de carga y mantenimiento de Rapamune no necesitan ser ajustadas en pacientes con insuficiencia renal (ver Dosificación). Pacientes pediátricos con trasplante renal: Se recabaron datos farmacocinéticos del sirolimus en estudios de concentración controlada en pacientes pediátricos con trasplante renal que también recibían ciclosporina y corticosteroides. Los rangos deseados de concentración mínima fueron de 10-20 ng/ml para los 21 chicos que recibieron los comprimidos o de 5-15 ng/ml para el único niño que recibió la solución oral. Los niños entre 6 y 11 años (n = 8) recibieron dosis medias ± DS de 1,75 ± 0,71 mg/día (0,064 ± 0,018 mg/Kg; 1,65 ± 0,43 mg/m2). Los niños entre 12 y 18 años (n = 14) recibieron dosis medias ± DS de 2,79 ± 1,25 mg/día (0,053 ± 0,0150 mg/Kg; 1,86 ± 0,61 mg/m2). En el momento del dosaje sanguíneo de sirolimus para la evaluación farmacocinética, la mayoría (80 %) de estos pacientes pediátricos habían recibido la dosis de sirolimus 16 horas después de la dosis única diaria de ciclosporina.
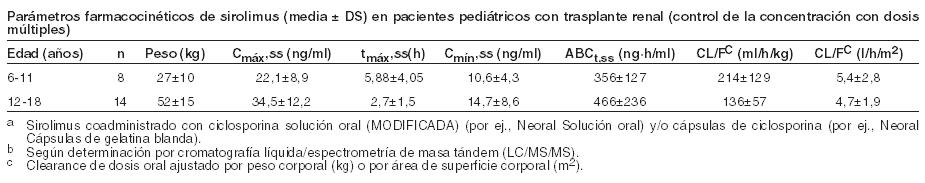
La siguiente Tabla resume los datos farmacocinéticos obtenidos en pacientes pediátricos bajo diálisis, con disfunción renal crónica.
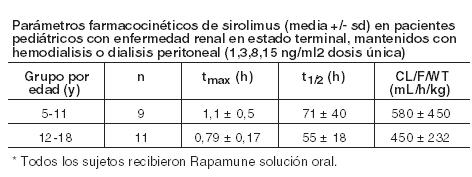
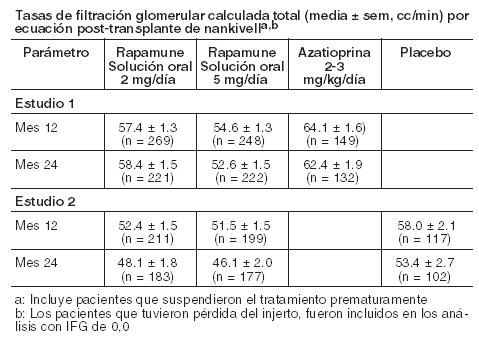
Pacientes geriátricos: Los estudios clínicos de Rapamune no incluyeron un número suficiente de pacientes > 65 años de edad para determinar si responderán de manera diferente que los pacientes más jóvenes. Después de la administración de Rapamune Solución Oral o Comprimidos, los datos de concentración de sirolimus en pacientes con trasplante renal mayores de 65 años fueron similares a los de la población adulta de 18 a 65 años. Género: El clearance de sirolimus en los varones fue un 12% menor que en las mujeres; los sujetos varones tenían un t1/2 significativamente más largo que las mujeres (72,3 horas versus 61,3 horas). No se recomiendan los ajustes de dosis basados en el género. Raza: En los ensayos de Fase 3 para la profilaxis del rechazo de órganos tras el trasplante renal utilizando solución o comprimidos de Rapamune y solución oral de ciclosporina (por ejemplo, Neoral® Solución oral y/o cápsulas de ciclosporina (por ejemplo, Neoral® Cápsulas de gelatina blanda) (ver Estudios Clínicos), no hubo diferencias significativas en las concentraciones medias de sirolimus a lo largo del tiempo entre los pacientes de raza negra (n = 190) y pacientes que no son de raza negra (n = 852) durante los primeros 6 meses después del trasplante. Interacción fármaco con fármaco: Es sabido que el sirolimus es un sustrato tanto para el citocromo CYP3A4 como para la glicoproteína P. La interacción farmacocinética entre el sirolimus y los fármacos administrados concomitantemente se discute a continuación. No se han realizado estudios de interacción con fármacos distintos de los descriptos a continuación. Ciclosporina: La ciclosporina es un sustrato e inhibidor de CYP3A4 y de la glicoproteína P. El sirolimus debe tomarse 4 horas después de la administración de la solución oral y/o cápsulas de ciclosporina. Las concentraciones de sirolimus pueden disminuir cuando se suspende la ciclosporina, a menos que la dosis de Rapamune sea aumentada (ver Dosificación e Interacciones). En un estudio de interacción fármaco-fármaco de dosis única en 24 voluntarios sanos, se les administró comprimidos de 10 mg de Rapamune simultáneamente o 4 horas después de una dosis de 300 mg de cápsulas de gelatina blanda Neoral®. Para la administración simultánea, la Cmáx media y el ABC se incrementaron en 512% y 148%, respectivamente, con relación a la administración de sirolimus solo. Sin embargo, cuando se administraron 4 horas después de la administración de ciclosporina, la Cmáx y el ABC del sirolimus aumentaron sólo en un 33% en comparación con la administración de sirolimus solo. Diltiazem: Diltiazem es un sustrato e inhibidor de CYP3A4 y la glicoproteína P; las concentraciones de sirolimus deben ser monitoreadas y puede ser necesario un ajuste de dosis (ver Interacciones). La administración oral simultánea de 10 mg de solución oral de sirolimus y 120 mg de diltiazem a 18 voluntarios sanos afectó significativamente la biodisponibilidad del sirolimus. La Cmáx, tmax y ABC de sirolimus aumentaron 1,4, 1,3 y 1,6 veces, respectivamente. El sirolimus no afectó la farmacocinética del diltiazem ni de sus metabolitos desacetildiltiazem y desmetildiltiazem. Eritromicina: La eritromicina es un sustrato e inhibidor de CYP3A4 y glicoproteína P; no se recomienda la administración simultánea de sirolimus comprimidos y eritromicina (ver Advertencias e Interacciones). La administración oral simultánea de 2 mg diarios de solución oral de sirolimus y 800 mg de eritromicina cada 8 hs como comprimidos de eritromicina etil succinato en estado estacionario a 24 voluntarios sanos afectó significativamente la biodisponibilidad de sirolimus y eritromicina. La Cmáx y el ABC del sirolimus aumentaron respectivamente 4,4 y 4,2 veces y el tmax aumentó en 0,4 horas. La Cmáx y el ABC de eritromicina aumentaron 1,6 y 1,7 veces, respectivamente, y el tmax aumentó 0,3 h. Ketoconazol: El ketoconazol es un fuerte inhibidor de CYP3A4 y la glicoproteína P; no se recomienda la coadministración de comprimidos de sirolimus y ketoconazol (ver Advertencias e Interacciones). La administración de dosis múltiples de ketoconazol afectó significativamente la tasa y el grado de absorción y la exposición al sirolimus después de la administración de la solución oral de Rapamune, reflejada por aumentos de la Cmáx, tmax y ABC del sirolimus, de 4,3 veces, 38% y 10,9 veces, respectivamente. Sin embargo, la t½ terminal del sirolimus no fue cambiada. La dosis única de sirolimus no afectó las concentraciones plasmáticas de ketoconazol en el estado de equilibrio a las 12 horas. Rifampina: La rifampina es un fuerte inductor de CYP3A4 y de la glicoproteína P; no se recomienda la coadministración de Rapamune comprimidos con rifampicina. En pacientes donde está indicada la rifampicina, se deben considerar agentes terapéuticos alternativos con menor potencial de inducción enzimática (ver Advertencias e Interacciones). El pretratamiento de 14 voluntarios sanos con dosis múltiples de rifampicina, 600 mg diarios durante 14 días, seguido de una dosis única de 20 mg de sirolimus en solución oral, redujo significativamente el ABC y la Cmáx del sirolimus en un 82% y 71%, respectivamente. Verapamilo: El verapamilo es un sustrato e inhibidor de CYP3A4 y de la glicoproteína P; las concentraciones de sirolimus deben ser monitoreadas y puede ser necesario un ajuste de dosis (ver Interacciones). La administración oral simultánea de 2 mg diarios de solución oral de sirolimus y 180 mg cada 12 hs de verapamilo en estado estacionario, a 26 voluntarios sanos, afectó significativamente la biodisponibilidad de sirolimus y verapamilo. La Cmáx y ABC de sirolimus se incrementaron 2,3 y 2,2 veces, respectivamente, sin cambio sustancial en la tmax. La Cmáx y el ABC del enantiómero S(-) farmacológicamente activo del verapamilo, aumentaron 1,5 veces y el tmax disminuyó 1,2 hs. Medicamentos que pueden ser coadministrados sin el ajuste de la dosis: No se observaron interacciones farmacocinéticas clínicamente significativas entre fármacos, en los estudios con los fármacos enumerados a continuación. Sirolimus y estos fármacos pueden ser coadministrados sin ajustes de dosis. Aciclovir. Atorvastatina. Digoxina. Gliburida. Nifedipina. Norgestrel/etinilestradiol. Prednisolona. Trimetoprima-sulfametoxazol. Otras interacciones fármaco - fármaco: La coadministración de Rapamune con otros inhibidores potentes conocidos de CYP3A4 y/o glicoproteína P (tales como voriconazol, itraconazol, telitromicina o claritromicina) u otros inductores potentes conocidos de CYP3A4 y / o P-gp (como rifabutina) no es recomendado (ver Advertencias e Interacciones). En pacientes en los que se indican potentes inhibidores o inductores de CYP3A4, se deben considerar agentes terapéuticos alternativos con menor potencial de inhibición o inducción de CYP3A4. Se debe tener cuidado cuando los fármacos u otras sustancias que son sustratos y/o inhibidores o inductores de CYP3A4, se administren concomitantemente con Rapamune. Otros fármacos que tienen el potencial de aumentar las concentraciones sanguíneas de sirolimus incluyen (pero no se limitan a): Bloqueadores de los canales de calcio: nicardipina. Agentes antifúngicos: clotrimazol, fluconazol. Antibióticos: troleandomicina. Agentes procinéticos gastrointestinales: cisaprida, metoclopramida. Otros fármacos: bromocriptina, cimetidina, danazol, inhibidores de la proteasa (Ej. para VIH y hepaticis C que incluyen fármacos como ritonavir, indinavir, boceprevir, telaprevir. Otras drogas que tienen el potencial de disminuir la concentración de sirolimus (pero no se limitan a): Anticonvulsionantes: carbamazepina, fenobarbital, fenitoína. Antibióticos: rifapentina. Otras interacciones fármaco - alimentos: El jugo de pomelo reduce el metabolismo del fármaco mediado por CYP3A4. El jugo de pomelo no debe tomarse ni utilizarse para la dilución de Rapamune (ver Dosificación e Interacciones). Otras interacciones con hierbas: La hierba de San Juan (Hypericum perforatum) es un inductor del CYP3A4 y de la glicoproteína P. Dado que el sirolimus es un sustrato tanto para el citocromo CYP3A4 como para la glicoproteína P, existe el potencial de que el uso de la hierba de San Juan en pacientes que reciben Rapamune, podría reducir las concentraciones de sirolimus (ver Interacciones). Estudios clínicos: La seguridad y eficacia de Rapamune Solución Oral en la prevención del rechazo de órganos con posterioridad al trasplante renal fueron evaluadas en dos estudios multicéntricos, controlados, doble-ciegos y aleatorios. En estos estudios se compararon dos niveles de dosis de Rapamune Solución Oral (2 mg y 5 mg, una vez al día), con azatioprina (Estudio 1) o placebo (Estudio 2), administrados en combinación con CsA y corticosteroides. El Estudio 1 fue realizado en 38 centros de los Estados Unidos. Se reclutaron 719 pacientes que fueron asignados al azar a uno u otro grupo de tratamiento con posterioridad al trasplante: 284 pacientes fueron asignados al grupo con Rapamune Solución Oral 2 mg diarios, 274 fueron asignados al grupo con Rapamune Solución Oral 5 mg diarios y, 161, al grupo con azatioprina 2 a 3 mg/kg diarios. El Estudio 2 comparativo de Rapamune (2 mg y 5 mg una vez al día) se llevó a cabo en Australia, Canadá, Europa y los Estados Unidos, en un total de 34 centros. Se incorporaron en este estudio 576 pacientes, que se asignaron aleatoriamente a uno u otro grupo de tratamiento antes de producirse el trasplante: 227 fueron asignados al grupo con Rapamune Solución Oral 2 mg diarios, mientras que 219 fueron asignados al grupo con Rapamune Solución Oral 5 mg diarios y, 130 pacientes, al grupo con placebo. En ambos estudios, se prohibió el uso de terapia de inducción de anticuerpos anti-linfocitos. El fracaso del tratamiento fue definido como el primer episodio agudo de rechazo (confirmado por biopsia), pérdida del órgano o muerte. Las siguientes tablas resumen los resultados de los análisis de la eficacia primaria en estos estudios. Rapamune Solución Oral, administrado en dosis de 2 mg/día y 5 mg/día, redujo significativamente la incidencia de fracaso al tratamiento (estadísticamente significativa al nivel de < 0,025; nivel de significación nominal ajustado para comparaciones de dosis múltiples) 6 meses después del trasplante, en comparación con la azatioprina y el placebo.
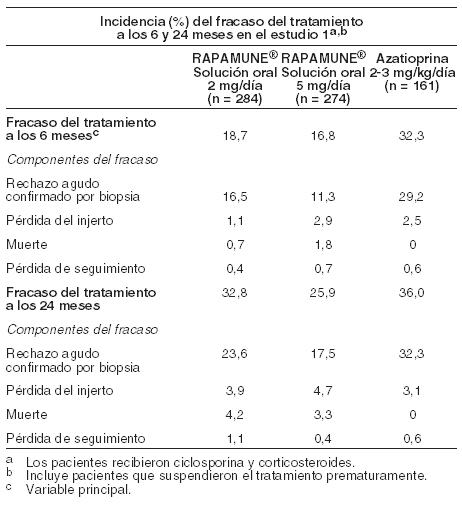
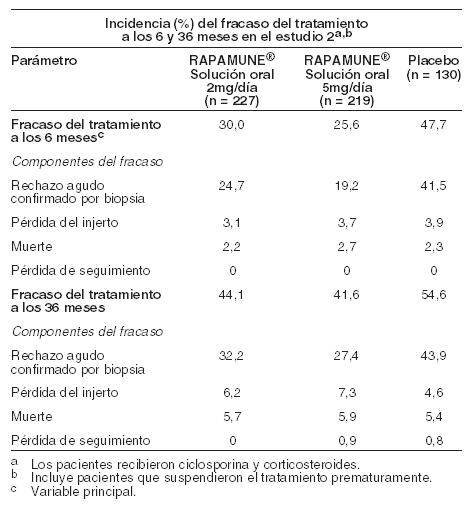
Los objetivos co-primarios fueron la sobrevida del paciente y del injerto al cabo de 1 año. La siguiente Tabla presenta la sobrevida del injerto y del paciente después de 1 y 2 años en el Estudio 1 y de 1 y 3 años en el Estudio 2. Los índices de sobrevida del injerto y del paciente fueron similares entre los pacientes tratados con Rapamune y los tratados con los agentes comparativos.
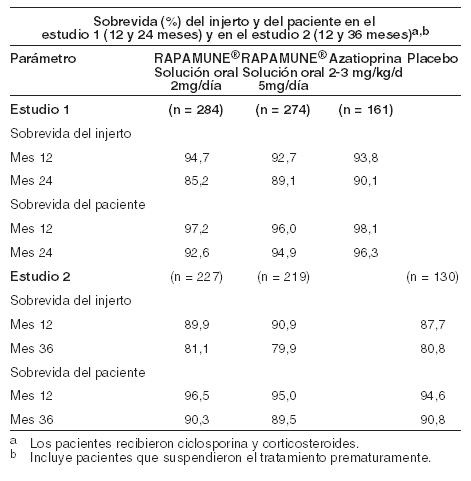
La reducción en la incidencia de episodios de primer rechazo agudo confirmado por biopsia en los pacientes tratados con Rapamune en comparación con los grupos de control incluyó una reducción en todos los grados de rechazo. En el estudio 1, que fue prospectivamente estratificado por raza dentro de cada centro, el índice de fracaso del tratamiento fue similar con Rapamune 2 mg/día e inferior con Rapamune 5 mg/día en comparación con la azatioprina en los pacientes de raza negra. En el estudio, que no fue prospectivamente estratificado por raza, el índice de fracaso del tratamiento fue similar con ambas dosis de Rapamune en comparación con el placebo en los pacientes de raza negra. La decisión de usar la dosis más alta de Rapamune Solución Oral en pacientes de raza negra debe ser comparada con el mayor riesgo de eventos adversos dependientes de la dosis que se observaron con la dosis de 5 mg de Rapamune Solución Oral (ver Reacciones Adversas).
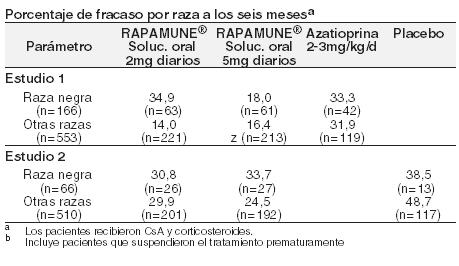
Los índices medios de filtración glomerular (IFG) un año después del trasplante se calcularon empleando la ecuación de Nankivell para todos los sujetos incluidos en cada estudio que contaban con una determinación de creatinina sérica a los 12 meses. En ambos estudios, el IFG medio al año fue inferior en los pacientes tratados con CsA y Rapamune que en los tratados con CsA y azatioprina o placebo.
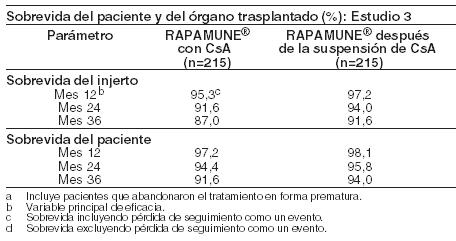
Dentro de cada grupo de tratamiento en los Estudios 1 y 2, el IFG medio 1 año después del trasplante fue inferior en aquellos pacientes que presentaron por lo menos un episodio de rechazo agudo confirmado por biopsia que en los que no lo hicieron. La función renal debe ser controlada, y se debe considerar un apropiado ajuste de la terapia inmunosupresiva, en pacientes con niveles de creatinina sérica, elevados o en aumento (ver Advertencias). Rapamune comprimidos: Se demostró que la seguridad y la eficacia de Rapamune Solución Oral y Rapamune comprimidos para la prevención del rechazo de órganos tras el trasplante renal, eran clínicamente equivalentes en un ensayo controlado, aleatorizado y multicéntrico (ver Farmacología). Estudio de la suspensión de ciclosporina en pacientes con trasplante renal: Se evaluó la seguridad y la eficacia de Rapamune como régimen de mantenimiento, a partir de la suspensión de la CsA, a los tres y cuatro meses después del trasplante renal. El estudio 3 fue multicéntrico, controlado y aleatorio que se llevó a cabo en 57 centros de Australia, Canadá y Europa. Se incorporaron en el estudio 525 pacientes. Todos los pacientes recibieron Rapamune Comprimidos. En este estudio se comparó a los pacientes que recibieron Rapamune, CsA y corticosteroides en forma continua, con pacientes que recibieron el mismo tratamiento estandarizado durante los primeros tres meses posteriores al trasplante (período previo a la asignación al azar a uno de los tratamientos) y luego se les suspendió la administración de CsA. Durante el período de suspensión de la CsA, las dosis de Rapamune se ajustaron hasta alcanzar las concentraciones basales de sirolimus deseadas en sangre entera (16 a 24 ng/ml, hasta el mes 12, luego 12 a 20 ng/ml, expresados como valores de ensayos cromatográficos). A los tres meses, 430 pacientes fueron igualmente seleccionados al azar para recibir, o bien Rapamune con CsA, o bien Rapamune como régimen de mantenimiento posterior a la suspensión de la CsA. Los pacientes aptos para participar de la selección al azar no debían haber presentado ningún episodio agudo de rechazo (grado 3 de Banff) o rechazo vascular dentro de las cuatro semanas previas a la asignación aleatoria y debían contar con niveles de creatinina sérica ≤ 4,5 mg/dl y con una función renal adecuada (según la opinión del investigador) como para tolerar la suspensión de la CsA. La variable primaria de eficacia fue la sobrevida del órgano a los 12 meses del trasplante. Las variables secundarias de eficacia fueron el índice de episodios agudos de rechazo confirmados por biopsia, la sobrevida de los pacientes, la incidencia de fracaso del tratamiento (definido como el primer episodio agudo de rechazo confirmado por biopsia, pérdida del órgano o muerte) y fracaso terapéutico (definido como la primera aparición de abandono del tratamiento, rechazo agudo, pérdida del injerto o muerte). En el cuadro que se encuentra más abajo, se resumen los resultados de este estudio respecto de la sobrevida de los pacientes y de los órganos a los 12, 24, 36, 48 y 60 meses en este estudio. A los 12, 24 y 36 meses, la supervivencia del injerto y del paciente fue similar en ambos grupos.
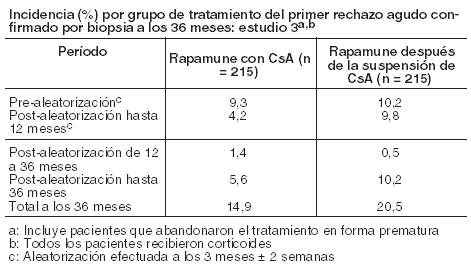
El siguiente cuadro resume los resultados del primer episodio de rechazo agudo comprobado por biopsia a los 12 y a los 60 meses. Respecto del primer episodio de rechazo agudo comprobado por biopsia, se observó una diferencia significativa entre los dos grupos del estudio, en el período que va desde la asignación al azar a uno u otro esquema de tratamiento hasta los 12 meses posteriores al trasplante. La mayoría de los episodios de rechazo agudo posteriores a la asignación a un esquema de tratamiento se produjeron dentro de los tres primeros meses posteriores a esta asignación al tratamiento.
El siguiente cuadro resume el IFG calculado en el Estudio 3 (Estudio de la suspensión de CsA).
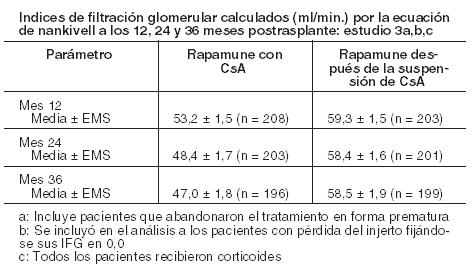
Los índices medios de filtración glomerular, a los 12, 24 y 36 meses, calculados por medio de la ecuación de Nankivell, fueron significativamente más altos en los pacientes que recibieron Rapamune como régimen de mantenimiento posterior a la suspensión de la CsA, que en el grupo de pacientes que recibió Rapamune y CsA. Los pacientes que presentaron un episodio agudo de rechazo en algún momento después del trasplante registraron un IFG más alto con posterioridad a la suspensión de la CsA, en comparación con los pacientes asignados al grupo con Rapamune y CsA. No hubo diferencias significativas en la IFG entre los grupos de pacientes que experimentaron rechazo agudo después de la aleatorización. Aunque el protocolo inicial fue diseñado para 36 meses, hubo una enmienda posterior para ampliar este estudio. Los resultados del grupo de la suspensión de la ciclosporina a los meses 48 y 60 fueron consistentes con los resultados al mes 36. El 52% (112/215) de los pacientes en el grupo de la suspensión de Rapamune con ciclosporina permaneció en terapia hasta el mes 60 y mostró un IFG sostenido. Pacientes de alto riesgo inmunológico con trasplante renal: Se evaluó Rapamune en un estudio clínico (Estudio 4) de 1 año de duración en pacientes de alto riesgo definidos como receptores de trasplante de raza negra y/o receptores de retrasplante renal por pérdida del aloinjerto anterior debido a razones inmunológicas y/o pacientes con alto panel de anticuerpos reactivos (PAR; nivel máximo de PAR > 80 %). Los pacientes recibieron sirolimus a una concentración-controlada y ciclosporina y corticosteroides según práctica local. La dosis de Rapamune se ajustó para alcanzar concentraciones de sirolimus de 10 a 15 ng/ml (método cromatográfico) a lo largo del período de estudio de 12 meses. La dosis de ciclosporina se ajustó para alcanzar concentraciones de referencia en sangre total de 200-300 ng/mL a lo largo de la semana 2, 150-200 ng/mL de la semana 2 a la semana 26 y 100-150 ng/mL de la semana 26 a la semana 52 para las concentraciones de concentraciones mínimas observadas. Se permitió inducción de anticuerpos por protocolo según lo definido prospectivamente en cada centro de trasplante, empleándose en el 88,4 % de los pacientes. El estudio se llevó a cabo en 35 centros de Estados Unidos. Un total de 224 pacientes recibió un trasplante y por lo menos una dosis de sirolimus y ciclosporina y comprendió 77,2 % de raza negra, 24,1 % con retrasplante renal y 13,5 % con alto PAR. La eficacia se evaluó con las siguientes variables, determinadas a los 12 meses: fracaso al tratamiento (definido como la primera aparición de rechazo agudo confirmado por biopsia, pérdida del injerto o muerte), primera aparición de pérdida del injerto o muerte, y función renal conforme a lo determinado por el IFG calculado con la fórmula de Nankivell. La Tabla a continuación resume los resultados de estas variables.

La sobrevida del paciente a los 12 meses fue del 94,6%. La incidencia de rechazo agudo confirmado por biopsia fue del 17,4 % y la mayoría de los episodios de rechazo agudo fueron de severidad leve. Conversión desde los inhibidores de calcineurina a Rapamune en pacientes con trasplante renal de mantenimiento: Se evaluó la conversión de inhibidores de la calcineurina (ICN) a Rapamune en pacientes con trasplante renal en mantenimiento desde los 6 meses hasta los 10 años postrasplante (Estudio 5). Este estudio fue multicéntrico, controlado y con asignación aleatoria llevado a cabo en 111 centros de Estados Unidos y Europa, y pretendía demostrar que la función renal se mejoró mediante la conversión de ICN a Rapamune. Se incluyeron y estratificaron por índice de filtración glomerular basal calculado (IFG 20-40 ml/min vs. mayor de 40 ml/min) 830 pacientes. En este ensayo no hubo ningún beneficio asociado con la conversión con respecto a la mejora de la función renal y una mayor incidencia de proteinuria en el grupo de conversión de Rapamune. La incorporación en el estrato de pacientes con índice de filtración glomerular basal calculado inferior a 40 ml/min se suspendió debido a un desequilibrio en los efectos secundarios, incluyendo neumonía, rechazo agudo, pérdida del injerto y muerte (ver Reacciones Adversas). El estudio comparó pacientes con trasplante renal (6-120 meses después del trasplante) cambiados de inhibidores de la calcineurina a Rapamune, con pacientes que continuaron recibiendo inhibidores de la calcineurina. Las medicaciones inmunosupresoras concomitantes incluyeron micofenolato mofetil (MMF), azatioprina (AZA) y corticoides. Se administró una única dosis inicial de carga de 12-20 mg de Rapamune, tras lo cual se ajustó la dosificación para alcanzar la concentración basal deseada de sirolimus en sangre de 8-20 ng/ml (método cromatográfico). La variable principal de eficacia fue el IFG calculado a los 12 meses después de la aleatorización. Las variables secundarias incluyeron rechazo agudo confirmado por biopsia, pérdida del injerto y muerte. Los hallazgos en el estrato de pacientes con IFG basal calculado mayor a 40 ml/min (conversión a Rapamune, n = 497; continuación con ICN, n = 246) se resumen a continuación. No se observó una mejoría clínica o estadísticamente significativa en el IFG de Nankivell en comparación con el basal.

El rango de la función renal y los índices de rechazo agudo, pérdida del injerto y muerte fueron similares al cabo de 1 y 2 años. Los eventos adversos emergentes del tratamiento se produjeron con mayor frecuencia durante los primeros 6 meses después de la conversión a Rapamune. Los índices de neumonía fueron significativamente superiores en el grupo de conversión a sirolimus. Mientras que los valores medios y medianas de la relación proteínas urinarias a creatinina fueron similares entre los grupos de tratamiento en la visita basal, se observaron valores medios y medianas de excreción de proteínas urinarias significativamente más elevados en el grupo de conversión a Rapamune al año y a los 2 años, como ilustra la tabla a continuación (ver Advertencias). Además, en comparación con los pacientes que continuaron recibiendo inhibidores de la calcineurina, un mayor porcentaje de pacientes presentó una relación de proteínas urinarias a creatinina > 1 al cabo de 1 y 2 años de la conversión a sirolimus. Esta diferencia se observó tanto en pacientes que tenían una relación de proteínas urinarias a creatinina ≤ 1 como en aquellos cuya relación basal era > 1. Un mayor porcentaje de pacientes en el grupo de conversión a sirolimus desarrolló proteinuria nefrótica, de acuerdo con la relación proteínas urinarias a creatinina > 3,5 (46/482 [9,5 %] vs. 9/239 [3,8 %], aun cuando los pacientes con proteinuria nefrótica basal fueron excluidos. La incidencia de proteinuria nefrótica fue significativamente superior en el grupo de conversión al sirolimus en comparación con el grupo de continuación de inhibidores de la calcineurina con una relación basal de proteínas urinarias a creatinina > 1 (13/29 vs. 1/14), excluyéndose a los pacientes con proteinuria nefrótica basal.
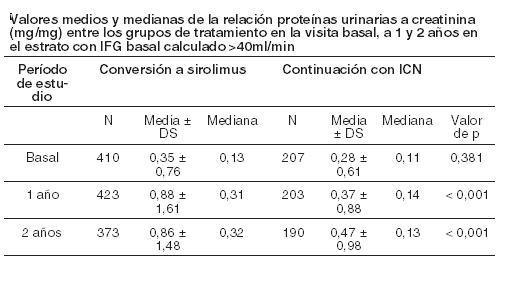
La información precedente debe tomarse en cuenta cuando se considere la conversión de inhibidores de la calcineurina a Rapamune en pacientes con trasplante renal estables debido a la falta de evidencia que demuestre que la función renal mejora luego de la conversión, al hallazgo de un mayor incremento en la excreción de proteínas urinarias y a una mayor incidencia de proteinuria nefrótica emergente del tratamiento después de la conversión a Rapamune. Esto pudo comprobarse entre los pacientes con excreción anormal existente de proteínas urinarias antes de la conversión. Conversión desde un régimen basado en ICN a un régimen basado en sirolimus en pacientes con trasplante hepático: Se evaluó en pacientes con trasplante hepático estable. El estudio clínico fue 2:1, aleatorizado, multicéntrico y controlado; realizado en 82 centros en todo el mundo, incluidos los EE.UU. y Europa, y tenía la intención de demostrar que la función renal se mejoró mediante la conversión de un CNI a Rapamune sin afectar negativamente la eficacia o la seguridad. Un total de 607 pacientes fueron inscritos. El estudio no demostró la superioridad de la conversión a un régimen basado en Rapamune en comparación con la continuación de un régimen basado en ICN en el IFG ajustado al inicio, estimada por Cockcroft-Gault, a los 12 meses (62 mL/min en el grupo de conversión Rapamune y 63 ml/min en el grupo de continuación de ICN). El estudio no demostró tampoco inferioridad en el grupo de conversión de Rapamune en comparación con el grupo
de continuación de CNI (6,6% frente a 5,6%), con respecto a la variable principal de eficacia que consiste en la pérdida del injerto y la muerte (incluidos los pacientes con datos de supervivencia faltantes). Los casos de muertes en el grupo de conversión de Rapamune (15/393, 3,8%) fueron más elevados que en el grupo de continuación con ICN (3/214, 1,4%), aunque la diferencia no fue estadísticamente significativa. Los índices de suspensión prematura del estudio (principalmente debido a eventos adversos o falta de eficacia), los eventos adversos en general (infecciones, específicamente) y rechazo agudo del injerto hepático confirmado por biopsia a los 12 meses fueron significativamente superiores en el grupo de conversión Rapamune versus el grupo de continuación con ICN. Pacientes pediátricos con trasplante renal: Un estudio clínico abierto, controlado y aleatorizado de 36 meses de duración, llevado a cabo en 14 centros norteamericanos, evaluó Rapamune en receptores pediátricos (de 3 a < 18 años) de trasplante renal considerados de alto riesgo inmunológico de desarrollar nefropatía crónica por aloinjerto, definido como antecedentes de uno o más episodios de rechazo agudo del aloinjerto y/o presencia de nefropatía crónica por aloinjerto en una biopsia renal. Se distribuyeron al azar 78 sujetos en una relación de 2:1 para recibir Rapamune (concentración deseada de sirolimus de 5 a 15 ng/ml, por cromatografía, n = 53) en combinación con un inhibidor de la calcineurina y corticoides o para continuar con el tratamiento inmunosupresor basado en inhibidores de la calcineurina (n = 25). La variable principal del estudio fue el fracaso al tratamiento, definido como la primera aparición de ya sea rechazo agudo confirmado por biopsia, pérdida del injerto o muerte, y el estudio fue diseñado para demostrar la superioridad de Rapamune agregado a un régimen inmunosupresor basado en inhibidores de la calcineurina en comparación con un régimen basado en inhibidores de la calcineurina. La incidencia acumulada del fracaso al tratamiento hasta los 36 meses fue del 45,3 % en el grupo de Rapamune versus el 44,0% en el grupo de control, no demostrando superioridad. Se produjo un deceso en cada grupo. Se asoció el empleo de Rapamune en combinación con inhibidores de la calcineurina y corticoides con un mayor riesgo de deterioro de la función renal, anormalidades en los lípidos séricos (que incluyeron, entre otros, aumento del colesterol y triglicéridos séricos), e infecciones urinarias (ver Advertencias). Este estudio no avala el agregado de Rapamune al tratamiento inmunosupresor con inhibidores de la calcineurina en esta subpoblación de pacientes pediátricos con trasplante renal. Pacientes con Linfangioleiomiomatosis: Se evaluaron la seguridad y la eficacia de Rapamune para el tratamiento de la linfangioleiomiomatosis (LAM) en un estudio aleatorizado, doble ciego, multicéntrico y controlado. En este estudio se comparó Rapamune (con dosis ajustada para mantener las concentraciones mínimas en sangre entre 5-15 ng/ml) con placebo durante un período de tratamiento de 12 meses, seguido de un período de observación de 12 meses. Se enroló a ochenta y nueve (89) pacientes; 43 pacientes fueron aleatorizados para recibir placebo y 46 pacientes para recibir Rapamune. El criterio de valoración primario fue la diferencia entre los grupos en el índice de cambio (pendiente) por mes en el volumen espiratorio forzado en 1 segundo (VEF1). Durante el período de tratamiento, la pendiente VEF1 fue de -12 ± 2 mL por mes en el grupo placebo y 1 ± 2 mL por mes en el grupo Rapamune (diferencia de tratamiento = 13 mL (IC del 95%: 7, 18). La diferencia absoluta entre grupos en el cambio medio en el VEF1 durante el período de tratamiento de 12 meses fue 153 ml, o aproximadamente, el 11% del VEF1 medio en el enrolamiento. Se observaron mejoras similares respecto a la capacidad vital forzada (CVF). Después de la discontinuación de Rapamune, el deterioro en la función pulmonar se reanudó en el grupo de Rapamune, y se asemejó a la del grupo placebo (ver la Figura 1).
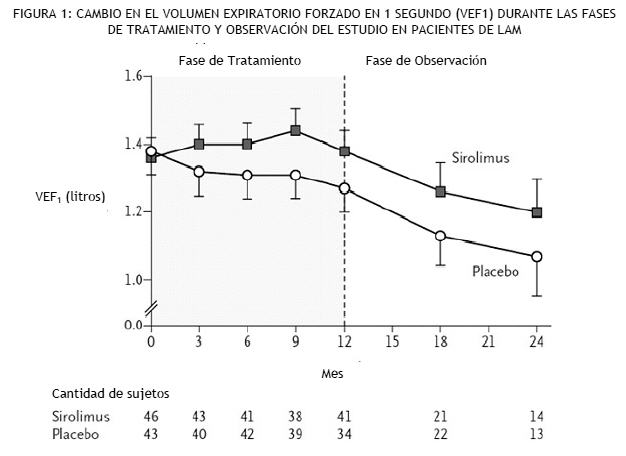
El índice de cambio durante 12 meses del factor D de crecimiento endotelial vascular (vascular endothelial growth factor D, VEGF-D), un factor de crecimiento linfangiogénico, que se ha demostrado que está elevado en pacientes con LAM, fue significativamente diferente en el grupo tratado con Rapamune (-88,0 ± 16,6 pg/mL/mes) en comparación con placebo (-2,42 ± 17,2 pg/mL/mes) con una diferencia en función del tratamiento de -86 pg/mL/mes (IC del 95%: 133, -39). La diferencia absoluta entre grupos en el cambio medio en VEGF-D durante el período de tratamiento de 12 meses fue -1017,2 o, aproximadamente 50% del VEGF-D medio en el enrolamiento.
Indicaciones.
Rapamune (sirolimus) está indicado para la profilaxis del rechazo de órganos en pacientes a partir de los 13 años de edad que reciben trasplantes renales. En los pacientes con riesgo inmunológico leve a moderado: Se recomienda utilizar Rapamune inicialmente en un esquema con CsA y corticosteroides; se suspenderá la CsA entre los dos y los cuatro meses después del trasplante (ver Dosificación). En pacientes de alto riesgo inmunológico (definidos como receptores de trasplante de raza negra y/o receptores de retrasplante renal por pérdida del aloinjerto anterior debido a razones inmunológicas y/o pacientes con alto panel de anticuerpos reactivos [PAR; nivel máximo de PAR > 80 %]), se recomienda emplear Rapamune en combinación con ciclosporina y corticoides durante el primer año después del trasplante (ver Dosificación y Estudios Clínicos). Limitaciones de uso en trasplante renal: No se ha evaluado el retiro de la ciclosporina en pacientes con rechazo agudo grado III de Banff 93 o rechazo vascular antes del retiro de la ciclosporina, pacientes dializados o con creatinina sérica > 4,5 mg/dl, pacientes de raza negra, pacientes con retrasplante renal, con multitrasplante de órganos o en pacientes con alto panel de anticuerpos reactivos (ver Estudios Clínicos). En pacientes de alto riesgo inmunológico: No se ha evaluado la seguridad y eficacia de estas combinaciones en pacientes de alto riesgo por un período superior a 1 año; por lo tanto, después del primer año postrasplante, se deberá considerar el ajuste al régimen inmunosupresor en base al estado clínico del paciente (ver Estudios Clínicos). En pacientes pediátricos: la seguridad y eficacia de Rapamune no ha sido establecida en pacientes < 13 años de edad, o en pacientes pediátricos ( < 18 años de edad), con trasplante renal, considerados de alto riesgo inmunológico (ver Reacciones adversas y Estudios Clínicos). La seguridad y eficacia del uso de novo de Rapamune sin ciclosporinas, no ha sido establecida en pacientes con trasplante renal (ver Advertencias). La seguridad y eficacia de los inhibidores conversores de calcineurina de Rapamune en el mantenimiento de los pacientes trasplantados, no ha sido establecida (ver Estudios Clínicos). Tratamiento de pacientes con linfangioleiomiomatosis: Rapamune (sirolimus) está indicado para el tratamiento de pacientes con linfangioleiomiomatosis (LAM).
Dosificación.
Rapamune debe administrarse únicamente por vía oral 1 vez al día, ya sea con o sin comida. Los comprimidos no deben ser triturados, masticados o partidos. En pacientes que no puedan tomar los comprimidos, deberá recetarse la solución instruyéndolos en el modo de administración. Guía para posología general en pacientes con trasplante renal: La dosis inicial de Rapamune debe administrarse tan pronto como sea posible después del trasplante. Se recomienda que se tome Rapamune 4 horas después de la administración de la solución oral y/o cápsulas de ciclosporina (ver Interacciones). Los ajustes frecuentes de dosis de Rapamune basados en concentraciones de sirolimus no estacionarias pueden conducir a una sobredosis o una subdosificación porque el sirolimus tiene una semivida larga. Una vez ajustada la dosis de mantenimiento de Rapamune, los pacientes deben continuar con la nueva dosis de mantenimiento durante al menos 7 a 14 días antes de un ajuste posológico adicional con monitorización de la concentración. En la mayoría de los pacientes, los ajustes de la dosis pueden basarse en una proporción simple: nueva dosis de Rapamune = dosis actual x (concentración objetivo/concentración actual). Se debe considerar una dosis de carga además de una nueva dosis de mantenimiento cuando sea necesario aumentar las concentraciones mínimas de sirolimus: dosis de carga de Rapamune = 3 x (nueva dosis de mantenimiento - dosis de mantenimiento actual). La dosis máxima de Rapamune administrada en cualquier día no debe exceder de 40 mg. Si una dosis diaria estimada supera los 40 mg a causa de la adición de una dosis de carga, la dosis de carga debe administrarse durante 2 días. Las concentraciones mínimas de sirolimus deben ser monitoreadas al menos 3 a 4 días después de una(s) dosis de carga. Dos miligramos (2 mg) de Rapamune Solución Oral han demostrado ser clínicamente equivalentes a 2 mg de Rapamune Comprimidos; por consiguiente, estas dos formulaciones son intercambiables. Sin embargo, no se ha demostrado si dosis más altas de Rapamune Solución Oral son clínicamente equivalentes a dosis más altas de Rapamune Comprimidos sobre la base de mg a mg. Pacientes de riesgo inmunológico reducido a moderado: Terapia combinada de Rapamune con ciclosporinas: En pacientes con trasplante renal de novo, se recomienda administrar Rapamune Solución Oral y Comprimidos en esquemas con CsA y corticosteroides. Se deberá administrar una dosis de carga de Rapamune tres veces la dosis de mantenimiento, por ejemplo una dosis de mantenimiento diaria de 2 mg, debe ser precedida por una dosis de carga de 6 mg. Se debe llevar a cabo un monitoreo terapéutico del fármaco, para mantener la concentración de sirolimus dentro del rango de referencia (ver Dosificación). Rapamune después de la suspensión de la CsA: Entre los dos y los cuatro meses después del trasplante, la CsA se discontinuará en forma progresiva durante un período de cuatro a ocho semanas y la dosis de Rapamune se irá ajustando, hasta obtener concentraciones plasmáticas de sirolimus dentro del rango de referencia. La CsA inhibe el metabolismo y transporte del sirolimus y, consecuentemente, las concentraciones de sirolimus disminuirán a medida que se discontinúe la CsA, salvo que se aumente la dosis de Rapamune (ver Farmacología). Pacientes de alto riesgo inmunológico: En pacientes de alto riesgo inmunológico, se recomienda emplear Rapamune en combinación con ciclosporina y corticoides durante el primer año después del trasplante (ver Estudios Clínicos). No se ha evaluado la seguridad y eficacia de esta combinación por un período superior a 1 año en pacientes de alto riesgo. Por lo tanto, después del primer año postrasplante, se deberá considerar el ajuste del régimen inmunosupresor en base al estado clínico del paciente. En pacientes que reciban Rapamune con ciclosporina, el tratamiento con Rapamune deberá iniciarse con una dosis de carga de hasta 15 mg el primer día después del trasplante. A partir del día 2, deberá administrarse una dosis inicial de mantenimiento de 5 mg/día. Deberá obtenerse el nivel mínimo entre los días 5 y 7 y la dosis diaria de Rapamune debe ajustarse consecuentemente (ver Dosificación). La dosis inicial de ciclosporina debe ser de hasta 7 mg/kg/día administrada en dosis divididas y ajustándose luego para alcanzar concentraciones sanguíneas mínimas de referencia en sangre entera (ver Dosificación). La prednisona debe administrarse a una dosis mínima de 5 mg/día. Podrá emplearse tratamiento inductor de anticuerpos. Posología en pacientes con linfangioleiomiomatosis: En pacientes con linfangioleiomiomatosis, la dosis inicial de Rapamune debe ser de 2 mg/día. Las concentraciones mínimas de sirolimus en sangre entera deben medirse en 10-20 días, con ajuste de la dosis a fin de mantener las concentraciones entre 5-15 ng/mL (ver Dosificación). En la mayoría de los pacientes, los ajustes de la dosis pueden basarse en una proporción sencilla: nueva dosis de Rapamune = dosis actual x (concentración ideal/concentración actual). Los ajustes frecuentes basados en concentraciones de sirolimus en estado no estacionario pueden dar lugar a sobredosis o subdosis, debido a que el sirolimus tiene una vida media larga. Una vez que se ajusta la dosis de mantenimiento de Rapamune, los pacientes deben continuar con la nueva dosis de mantenimiento durante, al menos, 7 a 14 días antes de un nuevo ajuste de la dosis con monitorización de la concentración. Una vez que se alcance una dosis estable, se debe realizar una monitorización terapéutica, al menos cada tres meses. Monitoreo de las concentraciones sanguíneas mínimas de sirolimus: Deberán controlarse las concentraciones sanguíneas mínimas de sirolimus en todos los pacientes, especialmente en aquellos pacientes con alteraciones en el metabolismo de fármacos, en pacientes ≥ 13 años que pesen menos de 40 kg, en pacientes con disfunción hepática, cuando se realiza un cambio en la forma de dosificación de Rapamune y durante la administración concurrente de inductores e inhibidores potentes del CYP3A4 (ver Interacciones). El monitoreo de los niveles terapéuticos de la droga no debe constituir la base exclusiva para ajustar el tratamiento con sirolimus. Deberá prestarse especial atención a los signos/síntomas, biopsias de tejido y parámetros de laboratorio. Cuando se usan en combinación con ciclosporina, las concentraciones mínimas de sirolimus deben mantenerse dentro del rango de referencia (ver Estudios Clínicos y Farmacología). Después de la discontinuación de la ciclosporina en pacientes trasplantados con riesgo inmunológico bajo o moderado, las concentraciones mínimas de referencia de sirolimus deberían ser de 16 a 24 ng/mL durante el primer año después del trasplante. A partir de entonces, las concentraciones de sirolimus de referencia deben ser de 12 a 20 ng/mL. Los rangos recomendados de concentración mínima de 24 horas para sirolimus se basan en métodos cromatográficos. En la práctica clínica actual, las concentraciones sanguíneas de sirolimus se determinan por cromatografía y por inmunoensayo. Dado que las concentraciones medidas de sangre entera de sirolimus dependen del tipo de ensayo utilizado, las concentraciones obtenidas por estas diferentes metodologías no son recíprocas (ver Advertencias y Farmacología). Deberán realizarse ajustes al rango de referencia de acuerdo con el ensayo utilizado para determinar la concentración mínima de sirolimus. Dado que los resultados son analíticos y dependientes del laboratorio, y los resultados pueden cambiar con el tiempo, los ajustes al rango terapéutico deben hacerse con un conocimiento detallado del ensayo específico empleado en cada centro. Por lo tanto, la comunicación debe mantenerse con el laboratorio que realiza el ensayo. Pacientes con bajo peso corporal: La dosificación inicial en pacientes ≥ 13 años de edad que pesen menos de 40 kg deberá ajustarse en función de la superficie corporal (1 mg/m2 diarios). La dosis inicial de carga será de 3 mg/m2. Pacientes con disfunción hepática: Se recomienda reducir la dosis de mantenimiento de Rapamune en aproximadamente un tercio a un medio en pacientes con deterioro de la función hepática. Sin embargo, en estos casos, no será necesario modificar la dosis de carga de Rapamune. Pacientes con disfunción renal: En base a datos farmacocinéticos clínicos no se requiere ajuste de la dosis en pacientes con deterioro de la función renal.
Contraindicaciones.
Rapamune está contraindicado en pacientes con hipersensibilidad a sirolimus.
Reacciones adversas.
Las siguientes reacciones adversas se discuten con mayor detalle en otras secciones del prospecto: Aumento de la susceptibilidad a infecciones, linfoma y malignidades (ver Advertencias). Mortalidad excesiva, pérdida del injerto y trombosis de la arteria hepática, en pacientes con trasplante de hígado (ver Advertencias). Dehiscencia de la anastomosis bronquial en pacientes con trasplante de pulmón (ver Advertencias). Reacciones de Hipersensibilidad (ver Advertencias). Dermatitis exfoliativa (ver Advertencias). Angioedema (ver Advertencias). Cicatrización de heridas y retención hídrica (ver Advertencias). Hipertrigliceridemia, hipercolesterolemia (ver Advertencias). Deterioro de la función renal en terapias a largo plazo de Ciclosporina combinada con Rapamune (ver Advertencias). Proteinuria (ver Advertencias). Enfermedad intersticial pulmonar (ver Advertencias). Aumento del riesgo de SUH/PT/MAT inducido por inhibidores de la calcineurina. Las reacciones adversas más frecuentes (≥ 30%) observadas con Rapamune en los estudios clínicos de profilaxis de rechazo de órganos en receptores de trasplante renal son: edema periférico, hipertrigliceridemia, hipertensión, hipercolesterolemia, aumento de creatinina, estreñimiento, dolor abdominal, diarrea, infección del tracto urinario, anemia, náuseas, artralgia, dolor y trombocitopenia. Las reacciones adversas más frecuentes (≥ 20%) observadas con Rapamune en los estudios clínicos para el tratamiento de la LAM son: estomatitis, diarrea, dolor abdominal, náuseas, nasofaringitis, acné, dolor torácico, edema periférico, mareos, mialgia e hipercolesterolemia. Las siguientes reacciones adversas resultaron en una tasa de discontinuación > 5% en los estudios clínicos de profilaxis de rechazo de trasplante renal: aumento de la creatinina, hipertrigliceridemia y PT. En pacientes con LAM, el 11% de los sujetos interrumpieron la terapia debido a reacciones adversas, sin una única reacción adversa que condujo a la interrupción de la terapia en más de un paciente tratado con Rapamune. Experiencia en estudios clínicos en la profilaxis del rechazo de órganos tras el trasplante renal: La seguridad y eficacia de Rapamune Solución Oral para la prevención del rechazo de órganos tras el trasplante renal se evaluaron en dos ensayos controlados aleatorios, doble ciego, multicéntricos (ver Estudios Clínicos). Los perfiles de seguridad en los dos estudios fueron similares. La incidencia de reacciones adversas en el estudio aleatorizado, doble ciego, multicéntrico, controlado con placebo (Estudio 2), en el que 219 pacientes con trasplante renal recibieron Rapamune Solución Oral 2 mg/día, 208 recibieron Rapamune Solución Oral 5 mg/día y 124 recibieron placebo; se presenta en la Tabla a continuación. La población del estudio tenía una edad media de 46 años (rango de edad 15 a 71 años), la distribución era del 67% masculino y la composición por raza era: caucásico (78%), raza negra (11%), asiático (3%), hispanos (2%) y otras razas (5%). Todos los pacientes fueron tratados con ciclosporina y corticosteroides. Los datos (≥ 12 meses después del trasplante) presentados en la siguiente Tabla muestran las reacciones adversas que ocurrieron en al menos uno de los grupos de tratamiento con Rapamune con una incidencia ≥ 20%. El perfil de seguridad del comprimido no difirió del de la formulación en solución oral (ver Estudios Clínicos). En general, las reacciones adversas relacionadas con la administración de Rapamune dependían de la dosis/concentración. Aunque se demostró que una dosis diaria de mantenimiento de 5 mg, con una dosis de carga de 15 mg, era segura y efectiva, no se pudo establecer una ventaja de eficacia sobre la dosis de 2 mg para los pacientes con trasplante renal. Los pacientes que recibieron 2 mg de Rapamune Solución Oral por día demostraron un mejor perfil de seguridad global que los pacientes que recibieron 5 mg de Rapamune Solución Oral por día. Debido a que los estudios clínicos se realizan bajo condiciones muy diversas, las tasas de reacción adversa observadas en un estudio clínico de un fármaco no pueden compararse directamente con las tasas en los estudios clínicos del mismo o de otro fármaco y pueden no reflejar las tasas observadas en la práctica.
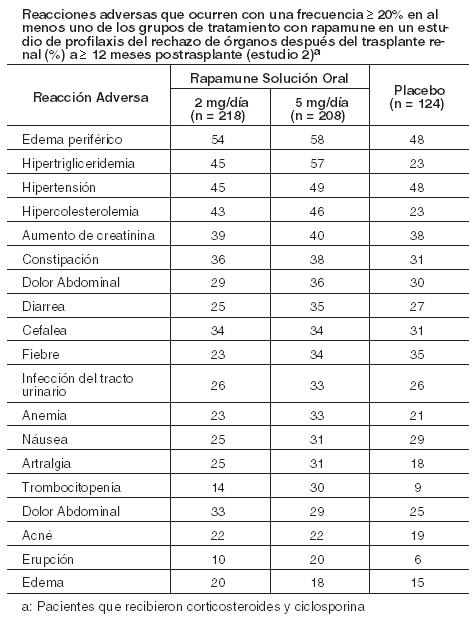
Las siguientes reacciones adversas se notificaron con menos frecuencia (≥ 3%, pero < 20%). General: Sepsis, linfocele, Herpes zóster, Herpes simplex. Cardiovascular: Tromboembolismo venoso (incluyendo embolia pulmonar, trombosis venosa profunda), taquicardia. Sistema digestivo: Estomatitis. Sistema hematológico y linfático: Trombocitopenia trombótica. Metabolismo/nutrición: Cicatrización anormal, aumento de la dehidrogenasa láctica, hipopotasemia, diabetes mellitus. Sistema músculo-esquelético: Necrosis del hueso. Sistema respiratorio: Neumonía, epixtasis. Piel: Melanoma, carcinoma de células escamosas, carcinoma de células basales. Sistema urogenital: Pielonefritis, deterioro de la función renal (aumento de creatinina) en terapias a largo plazo de Ciclosporina combinada con Rapamune (ver Advertencias), quistes ováricos, trastornos menstruales (incluyendo amenorrea y menorragia). Con menos frecuencia ( < 3%) ocurrieron las siguientes reacciones adversas: linfoma/trastorno linfoproliferativo postrasplante, infecciones micobacterianas (incluyendo M. tuberculosis), pancreatitis, citomegalovirus (CMV) y virus de Epstein-Barr. Aumento del colesterol sérico y los triglicéridos: El uso de Rapamune en pacientes con trasplante renal se asoció con un aumento del colesterol sérico y triglicéridos que pueden requerir tratamiento. En los estudios 1 y 2, en pacientes con trasplante renal de novo, que iniciaron el estudio con colesterol sérico total < 200 mg/dl o triglicéridos séricos totales < 200 mg/dl con ayuno, hubo un aumento de la incidencia de hipercolesterolemia (colesterol en ayunas > 240 mg/dL) o hipertrigliceridemia (triglicéridos sérico en ayunas > 500 mg/dL), respectivamente, en pacientes que recibieron Rapamune 2 mg y Rapamune 5 mg en comparación con los controles de azatioprina y placebo. El tratamiento de la hipercolesterolemia de nueva aparición con agentes hipolipemiantes fue necesario en el 42- 52% de los pacientes incluidos en los grupos de Rapamune de los estudios 1 y 2, en comparación con el 16% de los pacientes del grupo placebo y el 22% de los pacientes del grupo de azatioprina. En otros estudios de trasplante renal con Rapamune, hasta el 90% de los pacientes requirieron tratamiento para hiperlipidemia e hipercolesterolemia con terapia hipolipemiante (ej. estatinas, fibratos). A pesar del manejo hipolipemiante, hasta el 50% de los pacientes tenían niveles séricos de colesterol en ayunas > 240 mg/dl y triglicéridos por encima de los niveles recomendados (ver Advertencias). Cicatrización anormal: Los eventos de cicatrización anormal después de la cirugía de trasplante incluyen dehiscencia fascial, hernia incisional y disrupción de anastomosis (Ej. herida, vascular, vía aérea, ureteral, biliar). Malignidades: La siguiente Tabla resume la incidencia de neoplasias malignas en los dos ensayos controlados (Estudios 1 y 2) para la prevención del rechazo agudo (ver Estudios Clínicos). A los 24 meses (Estudio 1) y 36 meses (Estudio 2) postrasplante, no hubo diferencias significativas entre los grupos de tratamiento.
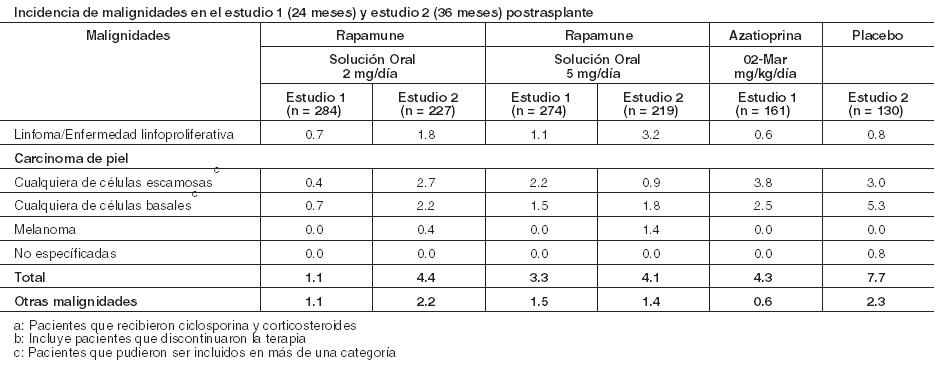
Rapamune luego de la discontinuación de ciclosporina: La incidencia de reacciones adversas se determinó a través de un ensayo aleatorizado, multicéntrico, controlado (Estudio 3) a 36 meses, en el que 215 pacientes con trasplante renal recibieron Rapamune con un régimen de mantenimiento después de la discontinuación de la ciclosporina y 215 pacientes recibieron Rapamune con ciclosporina (ver Estudios Clínicos). Todos los pacientes fueron tratados con corticosteroides. El perfil de seguridad antes de la aleatorización (comienzo de la discontinuación de la ciclosporina) fue similar al de los grupos de Rapamune de 2 mg en los Estudios 1 y 2. Después de la aleatorización (a los 3 meses), los pacientes que habían discontinuado la ciclosporina de su terapia, experimentaron mayores incidencias de las siguientes reacciones adversas: pruebas anormales de la función hepática (incluyendo aumento de AST/SGOT y aumento de ALT/SGPT), hipopotasemia, trombocitopenia y cicatrización anormal. Por el contrario, la incidencia de los siguientes eventos adversos fue mayor en pacientes que permanecieron con ciclosporina que aquellos que habían discontinuado la ciclosporina del tratamiento: hipertensión, toxicidad por ciclosporina, aumento de creatinina, función renal anormal, nefropatía tóxica, edema, hiperpotasemia, hiperuricemia e hiperplasia de las encías. La presión arterial sistólica y diastólica media mejoró significativamente después de la discontinuación de la ciclosporina. Malignidades: La incidencia de malignidades en el Estudio 3 (ver Estudios Clínicos) se presenta en la siguiente tabla. En el Estudio 3, la incidencia de linfoma/enfermedad linfoproliferativa fue similar en todos los grupos de tratamiento. La incidencia global de malignidad fue mayor en los pacientes que recibieron Rapamune más ciclosporina en comparación con los pacientes que habían discontinuado la ciclosporina. No se pudo sacar conclusiones sobre estas diferencias en la incidencia de malignidades, porque el Estudio 3 no fue diseñado para considerar los factores de riesgo de malignidad o para la búsqueda sistemática de malignidades en sujetos. Además, más pacientes en el grupo de Rapamune con ciclosporina, tuvieron antecedentes de carcinoma de piel.
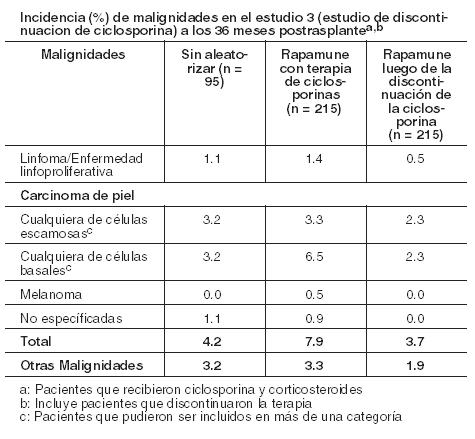
Pacientes con trasplante del alto riesgo inmunológico: La seguridad se evaluó en 224 pacientes que recibieron al menos una dosis de sirolimus con ciclosporina (ver Estudios Clínicos). En general, la incidencia y la naturaleza de las reacciones adversas fueron similares a las observadas en estudios anteriores de combinación con Rapamune. La incidencia de malignidad fue del 1,3% a los 12 meses. Conversión desde los Inhibidores de Calcineurina a Rapamune en el mantenimiento de la población con trasplante renal: No se ha establecido la seguridad y la eficacia de la conversión desde los inhibidores de la calcineurina a Rapamune en el mantenimiento de la población con trasplante renal (ver Estudios Clínicos). En un estudio que evaluó la seguridad y la eficacia de la conversión desde los inhibidores de la calcineurina a Rapamune (concentraciones iniciales de sirolimus de referencia de 12-20 ng/mL y luego de 8-20 ng/mL, por ensayo cromatográfico) en pacientes en mantenimiento de trasplante renal, se detuvo la inscripción en el subgrupo de pacientes (n = 87) con una tasa de filtración glomerular basal menor a 40 mL/min. Hubo una mayor tasa de eventos adversos graves, incluyendo neumonía, rechazo agudo, pérdida de injerto y muerte, en este estrato del grupo de tratamiento con Rapamune. El subgrupo de pacientes con una tasa de filtración glomerular basal menor a 40 mL/min, tuvo 2 años de seguimiento después de la aleatorización. En esta población, la tasa de neumonía fue del 25,9% (15/58) frente al 13,8% (4/29), la pérdida del injerto (excluyendo la muerte con pérdida funcional del injerto) fue del 22,4% (13/58) frente al 31,0% (9/29) y la muerte fue del 15,5% (9/58) frente al 3,4% (1/29) en el grupo de conversión a sirolimus y en el grupo de continuación de ICN, respectivamente. En el subgrupo de pacientes con una tasa de filtración glomerular basal mayor a 40 mL/min, no hubo beneficio asociado con la conversión, con respecto a la mejora de la función renal y una mayor incidencia de proteinuria en el grupo de conversión a Rapamune. En general, en este estudio, se observó un aumento de 5 veces, en los informes de tuberculosis entre los grupos de tratamiento con sirolimus 2,0% (11/551) y el comparador 0,4% (1/273) con un esquema de asignación al azar 2:1. Pacientes pediátricos con trasplante renal: La seguridad se evaluó en un estudio clínico controlado en pacientes pediátricos con trasplante renal ( < 18 años de edad) considerados de alto riesgo inmunológico, definido como historia de uno o más episodios de rechazo agudo de aloinjerto y/o presencia de nefropatía crónica de aloinjerto en una biopsia renal (ver Estudios Clínicos). El uso de Rapamune en combinación con inhibidores de la calcineurina y corticosteroides se asoció con una mayor incidencia del deterioro de la función renal (aumento de la creatinina) en comparación con la terapia basada en inhibidores de la calcineurina, anomalías de los lípidos en el suero (incluyendo pero no limitado a triglicéridos séricos y colesterol), e infecciones del tracto urinario. Pacientes con Linfangioleiomiomatosis: Se evaluó la seguridad en un estudio controlado en que se inscribió a 89 pacientes con linfangioleiomiomatosis, 46 de los cuales recibieron tratamiento con Rapamune (ver Estudios clínicos). Las reacciones medicamentosas adversas observadas en este estudio concordaron con el perfil de seguridad respecto de pacientes con trasplante renal que recibieron Rapamune, con la incorporación de la disminución de peso que se informó con una mayor incidencia con Rapamune en comparación con el placebo. Las reacciones adversas que se produjeron con una frecuencia ≥ 20% en el grupo tratamiento con Rapamune, y mayor que con placebo incluyeron estomatitis, diarrea, dolor abdominal, náuseas, nasofaringitis, acné, dolor torácico, edema periférico, infección de las vías respiratorias altas, cefalea, mareos, mialgia e hipercolesterolemia. Experiencia post-marketing: Las siguientes reacciones adversas se han identificado durante el uso posterior a la aprobación de Rapamune en pacientes con trasplante. Debido a que estas reacciones se informan voluntariamente en una población de tamaño incierto, no siempre es posible estimar con fiabilidad su frecuencia o establecer una relación causal con la exposición al fármaco. General: linfedema. Cardiovascular: Efusión del pericardio (incluyendo efusiones hemodinámicas significativas y taponamientos, que requirieron intervención en niños y adultos) y acumulación de fluidos. Sistema digestivo: Ascitis. Sistema hematológico y linfático: Pancitopenia, neutropenia. Trastornos hepatobiliares: Hepatotoxicidad, incluyendo necrosis hepática fatal, con concentraciones mínimas elevadas de sirolimus. Sistema inmune: Reacciones de hipersensibilidad, incluyendo reacciones anafilácticas/anafilactoideas, angioedema y vasculitis hipersensible (ver Advertencias). Infecciones: Tuberculosis. Se ha observado nefropatía asociada al virus BK en pacientes que recibieron inmunosupresores, incluyendo Rapamune. Esta infección puede estar asociada con resultados graves, incluyendo el deterioro de la función renal y la pérdida del injerto renal. Se han notificado casos de leucoencefalopatía multifocal progresiva (LMP), a veces fatal, en pacientes tratados con inmunosupresores, incluyendo Rapamune (ver Advertencias). Enterocolitis por Clostridium difficile. Metabolismo/nutrición: Pruebas hepáticas anormales, aumento de AST/SGOT, aumento de ALT/SGPT, hipofosfatemia, hiperglicemia, diabetes mellitus. Sistema Nervioso: Síndrome de encefalopatía posterior reversible. Respiratorio: Se han producido casos de enfermedad pulmonar intersticial (incluyendo neumonitis, bronquiolitis obliterante con neumonía organizante y fibrosis pulmonar), algunos fatales, sin etiología infecciosa identificada en pacientes que recibieron regímenes inmunosupresores incluyendo Rapamune. En algunos casos, la enfermedad intersticial pulmonar se ha resuelto al suspender o reducir la dosis de Rapamune. El riesgo puede aumentar a medida que aumenta la concentración mínima de sirolimus (ver Advertencias); hemorragia pulmonar; derrame pleural; proteinosis alveolar. Piel: Carcinoma de piel neuroendócrino (carcinoma de células de Merkel), dermatitis exfoliativa (ver Advertencias). Urogenital: Síndrome nefrótico, proteinuria, glomeruloesclerosis segmentaria focal, quistes ováricos, trastornos menstruales (incluyendo amenorrea y menorragia). Azoospermia se ha informado con el uso de Rapamune y ha sido reversible en la interrupción de Rapamune en la mayoría de los casos.
Advertencias.
Advertencia especial: el uso de inmunosupresores no se recomienda en pacientes con trasplante de hígado o pulmón. La inmunosupresión puede dar como resultado un aumento de la susceptibilidad a las infecciones y un posible desarrollo de linfoma u otras malignidades. La inmunosupresión puede tener como resultado el aumento de la susceptibilidad a las infecciones y el posible desarrollo de linfomas. Sólo podrán prescribir Rapamune aquellos médicos que posean experiencia en tratamientos inmunosupresores y manejo de pacientes con trasplante renal. Los pacientes que reciban este fármaco deben ser tratados en instituciones que cuenten con recursos de equipo, personal de laboratorio y apoyo médico adecuados. El médico responsable del tratamiento de mantenimiento deberá contar con la información completa requerida para el seguimiento del paciente. La seguridad y eficacia de Rapamune (sirolimus) como terapia inmunosupresora no ha sido establecida en pacientes con trasplante de hígado o pulmón, por lo tanto no se recomienda su uso. Trasplante de hígado - Mortalidad excesiva, pérdida del injerto y Trombosis hepática arterial (TAH): El uso de Rapamune en combinación con tacrolimus se asoció con mortalidad excesiva y pérdida del injerto en un estudio en pacientes de trasplante de hígado de novo. Muchos de estos pacientes tenían evidencia de infección o estaban en estado terminal. En el estudio anterior y en otro estudio de trasplante de hígado de novo, el uso de Rapamune en combinación con ciclosporina o tacrolimus, se asoció a un aumento del TAH; la mayoría de los casos de TAH ocurrieron 30 días post-trasplante y la mayoría concluyó con pérdida del injerto y muerte. Trasplante de pulmón - Dehiscencia de la anastomosis bronquial: Se han reportado casos, la mayoría fatales, de dehiscencia de la anastomosis bronquial, en trasplantes de pulmón de novo, cuando se utilizó Rapamune, como parte de una terapia inmunosupresiva. Linfoma: La inmunosupresión puede resultar en una mayor susceptibilidad a las infecciones y en el posible desarrollo de linfomas y otras enfermedades malignas, particularmente enfermedades de la piel. Las tasas de linfoma/enfermedad linfoproliferativa observadas en los estudios 1 y 2 fueron 0,7-3,2% (para los pacientes tratados con Rapamune) versus 0,6-0,8% (azatioprina y placebo) (ver Reacciones adversas). La sobreinmunosupresión también puede aumentar la susceptibilidad a las infecciones, incluso a la aparición de infecciones oportunistas, infecciones fatales y sepsis. Sólo deberán utilizar Rapamune aquellos médicos con experiencia en inmunosupresión y en el tratamiento de pacientes con trasplantes de órganos. Los pacientes que reciban esta droga deberán ser tratados en instituciones que cuenten con equipos, personal de laboratorio y apoyo médico adecuados. El médico responsable del tratamiento de mantenimiento deberá poseer un profundo conocimiento del producto, necesario para el adecuado control del paciente. Trasplante de hígado - Mayor mortalidad, Pérdida del injerto y Trombosis Arterial Hepática: La seguridad y la eficacia de Rapamune como terapia inmunosupresora no se han establecido en los pacientes con trasplante de hígado; por lo tanto, tal uso no se recomienda. El uso de Rapamune se ha asociado con resultados adversos en pacientes luego de un trasplante de hígado, incluyendo exceso de mortalidad, pérdida de injerto y trombosis de la arteria hepática (TAH). En un estudio en receptores de trasplante de hígado de novo se asoció la administración de Rapamune en combinación con tacrolimus con mayor mortalidad y pérdida del injerto. Muchos de estos pacientes presentaban infección en el momento o poco antes del deceso. En éste y otro estudio en receptores de trasplante hepático de novo se asoció la combinación de Rapamune y CsA o tacrolimus con una mayor incidencia de trombosis arterial hepática (7% en combinación versus 2% en el grupo control); la mayoría de los casos se produjo en los 30 días posteriores al trasplante y la mayoría derivó en pérdida del injerto o fallecimiento. Un estudio clínico en pacientes con trasplante hepático aleatorizados a la conversión a un régimen con sirolimus versus continuación de un régimen con inhibidores de la calcineurina (ICN) 6-144 meses después del trasplante de hígado demostró mayor casos de muerte en el grupo de conversión a sirolimus en comparación con el grupo de continuación de ICN, si bien la diferencia no fue estadísticamente significativa (3,8% versus 1,4%) (ver Estudios clínicos). Trasplante de Pulmón - Dehiscencia de la anastomosis bronquial: Se han comunicado casos de dehiscencia de la anastomosis bronquial, la mayoría fatales, en pacientes con trasplante pulmonar de novo cuando se administró sirolimus como parte de un régimen inmunosupresor. La seguridad y eficacia de Rapamune como terapia inmunosupresora no se han establecido en pacientes de trasplante de pulmón; por lo tanto, tal uso no se recomienda. Reacciones de hipersensibilidad: Las reacciones de hipersensibilidad, entre ellas las reacciones anafilácticas/anafilactoides, angioedema, dermatitis exfoliativa y vasculitis de hipersensibilidad se han visto asociadas a la administración de sirolimus (ver Reacciones Adversas). Angioedema: Rapamune se ha asociado con el desarrollo de angioedema. El uso concomitante de Rapamune con otros fármacos que se sabe causan angioedema, como los inhibidores de la enzima convertidora de angiotensina (ECA), puede aumentar el riesgo de desarrollar angioedema. Los niveles elevados de sirolimus (con o sin inhibidores de la ECA concomitantes) también pueden potenciar el angioedema (ver Interacciones). En algunos casos, el angioedema se ha resuelto al suspender o reducir la dosis de Rapamune. Cicatrización de heridas y retención hídrica: Se ha informado de cicatrización retardada o deficiente en pacientes que recibieron Rapamune, incluido linfocele y dehiscencia de la herida (ver Reacciones Adversas). Los inhibidores de mTOR tales como sirolimus han demostrado in vitro inhibición de la producción de ciertos factores de crecimiento que pueden afectar a la angiogénesis, la proliferación de fibroblastos y la permeabilidad vascular. El linfocele, una complicación quirúrgica conocida del trasplante renal, se ha registrado con una frecuencia significativamente mayor y en relación con la dosis administrada en pacientes tratados con Rapamune (ver Reacciones Adversas). En consecuencia, deberán considerarse las medidas adecuadas para minimizar esta complicación. De acuerdo con la literatura médica, los pacientes con IMC superior a 30 kg/m2 pueden presentar mayor riesgo de cicatrización anormal de la herida. Asimismo se ha informado de acumulación de líquido, tales como edema periférico, linfedema, derrame pleural y derrames pericárdicos (que incluyeron derrames hemodinámicamente significativos en niños y adultos), en pacientes que recibieron Rapamune. Hiperlipidemia: El aumento del colesterol sérico y de los triglicéridos que requieren tratamiento se produjo con mayor frecuencia en los pacientes tratados con Rapamune en comparación con los controles de azatioprina o placebo en los estudios 1 y 2 (ver Reacciones Adversas). Hubo una mayor incidencia de hipercolesterolemia (4
3-46%) y/o hipertrigliceridemia (45-57%) en los pacientes que recibieron Rapamune en comparación con los controles con placebo (cada uno 23%). El riesgo/beneficio debe ser cuidadosamente considerado en pacientes con hiperlipidemia establecida antes de iniciar un régimen inmunosupresor incluyendo Rapamune. Cualquier paciente que se administre Rapamune debe ser monitorizado para la hiperlipidemia. Si se detecta, deben iniciarse intervenciones como la dieta, el ejercicio y los agentes hipolipemiantes, como se indica en las directrices del Programa Nacional de Educación del Colesterol. En ensayos clínicos de pacientes que recibieron Rapamune más ciclosporina o Rapamune después de la suspensión de la ciclosporina, hasta el 90% de los pacientes requirieron tratamiento para hiperlipidemia e hipercolesterolemia con terapia hipolipemiante (por ejemplo, estatinas, fibratos). A pesar del tratamiento hipolipemiante, hasta el 50% de los pacientes tenían niveles de colesterol sérico en ayunas > 240 mg/dl y triglicéridos por encima de los niveles recomendados. La administración concomitante de Rapamune e inhibidores de la HMG-CoA reductasa resultó en reacciones adversas como elevaciones de CPK (3%), mialgia (6,7%) y rabdomiolisis ( < 1%). En estos ensayos, el número de pacientes era demasiado pequeño y la duración del seguimiento era demasiado corta para evaluar el impacto a largo plazo de Rapamune sobre la mortalidad cardiovascular. Deterioro de la función renal: La función renal debe monitorearse estrechamente durante la coadministración de Rapamune con ciclosporina, ya que la administración a largo plazo de esta combinación se ha asociado con el deterioro de la función renal. En los pacientes tratados con CsA y Rapamune, se observaron niveles de creatinina sérica más altos e índices de filtración glomerular más bajos, que los registrados en los pacientes tratados con CsA y placebo o CsA y azatioprina. El índice de deterioro de la función renal en estos estudios fue superior en el grupo de pacientes que recibían Rapamune y CsA, en comparación con los grupos que recibían el tratamiento control (Estudio 1 y 2). Por lo tanto, se deberá controlar la función renal y considerar ajustes adecuados del régimen inmunosupresor, incluyendo medidas como discontinuación de Rapamune y/o ciclosporinas y/o tacrolimus, en pacientes con niveles elevados de creatinina sérica. En pacientes con riesgo inmunológico leve a moderado, la continuación de la terapia de combinación con ciclosporina más allá de los 4 meses después del trasplante sólo debe considerarse cuando los beneficios superan los riesgos de esta combinación para los pacientes individuales. Se debe tener cuidado al usar agentes (por ejemplo, aminoglucósidos y anfotericina B) que se sabe que tienen un efecto de deterioro sobre la función renal. En pacientes con retraso en la función del injerto, Rapamune puede retrasar la recuperación de la función renal. Proteinuria: Se recomiendan controles periódicos cuantitativos de la excreción urinaria de proteínas. En un estudio que evaluó la conversión de inhibidores de la calcineurina (ICN) a Rapamune en pacientes con trasplante renal en mantenimiento 6 - 120 meses después del trasplante, se observó mayor excreción urinaria de proteínas por lo regular entre los 6 y 24 meses después de la conversión a Rapamune en comparación con la continuación de ICN (ver Reacciones Adversas y Estudios Clínicos). Los pacientes en el cuartil más elevado de excreción urinaria de proteínas antes de la conversión a Rapamune fueron aquellos con mayor aumento de excreción proteica después de la conversión. En el 2,2 % de los pacientes del grupo de conversión a Rapamune versus el 0,4% del grupo de pacientes con continuación de ICN se comunicó nefrosis de reciente comienzo (síndrome nefrótico). También se informó proteinuria de rango nefrótico (definida como proporción de proteína urinaria a creatinina > 3,5) en el 9,2% en el grupo de pacientes de conversión a Rapamune en comparación con el 3,7% en el grupo de pacientes con continuación de CNI. Se observó una reducción del grado de excreción urinaria de proteínas en casos individuales después de suspender Rapamune. No se ha establecido la seguridad y eficacia de la conversión de inhibidores de la calcineurina a sirolimus en pacientes con trasplante renal en mantenimiento. Infecciones virales latentes: Los pacientes tratados con inmunosupresores, incluido Rapamune, presentan mayor riesgo de desarrollar infecciones oportunistas, así como también activación de infecciones virales latentes. Entre estas infecciones se encuentran la nefropatía asociada al virus BK, que se ha observado en pacientes con trasplante renal que reciben inmunosupresores, incluyendo Rapamune. Esta infección puede estar asociada con resultados graves, como el deterioro de la función renal y la pérdida del injerto (ver Reacciones Adversas). La monitorización del paciente puede ayudar a detectar riesgo de nefropatía asociada al virus BK. Se debe considerar la reducción de la inmunosupresión en los pacientes que desarrollan evidencia de nefropatía asociada al virus BK. Se han reportado casos de leucoencefalopatía multifocal progresiva (PML) en pacientes que reciben inmunosupresores, incluyendo Rapamune. PML se presenta comúnmente con hemiparesia, apatía, confusión, deficiencias cognitivas y ataxia. Los factores de riesgo para la PML incluyen el tratamiento con terapias inmunosupresoras y el deterioro de la función inmune. En los pacientes inmunosuprimidos, los médicos deben considerar la PML en el diagnóstico diferencial en pacientes que informan de síntomas neurológicos y la consulta con un neurólogo debe considerarse como clínicamente indicado. Se debe considerar la posibilidad de reducir la cantidad de inmunosupresión en pacientes que desarrollan PML. En los pacientes con trasplante, los médicos también deben considerar el riesgo para el injerto, de reducción de la inmunosupresión. Enfermedad pulmonar intersticial: Se han producido casos de enfermedad pulmonar intersticial (neumonitis, bronquiolitis obliterante con neumonía organizante y fibrosis pulmonar), en algunos casos fatales, sin etiología infecciosa identificada en pacientes que recibieron regímenes inmunosupresores incluyendo Rapamune. En algunos casos, la enfermedad intersticial pulmonar se informó con hipertensión pulmonar (incluida la hipertensión arterial pulmonar) como un evento secundario. En algunos casos, la enfermedad intersticial pulmonar se ha resuelto tras la interrupción o reducción de la dosis de Rapamune. El riesgo puede incrementarse a medida que aumenta la concentración de sirolimus (ver Reacciones Adversas). Uso de novo sin Ciclosporinas: La seguridad y la eficacia del uso de novo de Rapamune sin ciclosporina no están establecidas en pacientes con trasplante renal. En un estudio clínico multicéntrico, los pacientes con trasplante renal de novo tratados con Rapamune, micofenolato mofetilo (MMF), esteroides y un antagonista del receptor de IL-2, tuvieron tasas de rechazo agudo significativamente más altas y tasas de mortalidad numéricamente más altas en comparación con los pacientes tratados con ciclosporina, esteroides y antagonistas del receptor de IL-2. Un beneficio, en términos de mejor función renal, no fue evidente en el grupo de tratamiento con el uso de novo de Rapamune sin ciclosporina. Estos hallazgos también se observaron en un grupo de tratamiento similar de otro ensayo clínico. Síndrome urémico hemolítico/púrpura trombocitopénica trombótica/microangiopatía trombótica, inducidos por inhibidores de la calcineurina: La administración concomitante de sirolimus y un inhibidor de la calcineurina puede aumentar el riesgo de síndrome urémico hemolítico/púrpura trombocitopénica trombótica/microangiopatía trombótica (SUH/PTT/MAT) inducidos por los inhibidores de la calcineurina (ver Reacciones Adversas). Profilaxis antimicrobiana: Se han registrado casos de neumonía por Pneumocystis carinii en pacientes que no recibían profilaxis antimicrobiana. Por lo tanto, deberá administrarse antibioticoterapia preventiva frente a neumonía por Pneumocystis carinii durante un período de 1 año después del trasplante. Se recomienda efectuar un tratamiento profiláctico contra el citomegalovirus (CMV) durante los tres meses posteriores al trasplante, particularmente en aquellos pacientes que presenten un mayor riesgo de enfermedad por CMV. Diferentes concentraciones mínimas de Sirolimus reportadas entre metodologías cromatográficas e inmunoensayo: Actualmente, en la práctica clínica, las concentraciones en sangre entera de sirolimus se miden mediante diversas metodologías cromatográficas e inmunoensayos. Los valores de concentración de la muestra del paciente de diferentes ensayos pueden no ser intercambiables (ver Dosificación). Carcinomas de piel: Los pacientes con terapia inmunosupresora tienen un mayor riesgo de cáncer de piel. La exposición a la luz solar y rayos UV debe limitarse mediante el empleo de ropa protectora y una crema pantalla solar con alto factor de protección (ver Reacciones Adversas). Interacción con Inhibidores Fuertes e Inductores de CYP3A4 y/o P-gp: Evite el uso concomitante de Rapamune con fuertes inhibidores de CYP3A4 y/o glicoproteína P (como ketoconazol, voriconazol, itraconazol, eritromicina, telitromicina o claritromicina) o fuertes inductores de CYP3A4 y/o glicoproteína P, como rifampina o rifabutina (ver Interacciones). Carcinogénesis, mutagénesis y deterioro de la fertilidad: Se realizaron estudios de carcinogenicidad en ratones y ratas. En un estudio con ratones hembra de 86 semanas con dosis de sirolimus 30 a 120 veces la dosis clínica diaria de 2 mg (ajustada para la superficie corporal), hubo un aumento estadísticamente significativo de linfoma maligno en todos los niveles de dosis en comparación con los controles. En un segundo estudio en ratones con dosis que fueron aproximadamente de 3 a 16 veces la dosis clínica (ajustada para la superficie corporal), se consideró relación con el sirolimus, adenomas hepatocelulares y carcinomas en machos. En el estudio con ratas de 104 semanas, con dosis iguales o inferiores a la dosis clínica de 2 mg diarios (ajustada por superficie corporal), no hubo hallazgos significativos. El sirolimus no fue genotóxico en el ensayo de mutación reversa bacteriana in vitro, en el ensayo de aberración cromosómica de células de ovario de hámster chino, en el ensayo de mutación directa de células de linfoma de ratón o en el ensayo de micronúcleo de ratón in vivo. La fertilidad disminuyó levemente en ratas machos y hembras después de la administración oral de sirolimus en dosis aproximadamente 10 o 2 veces, respectivamente, la dosis clínica de 2 mg diarios (ajustada para la superficie corporal). En ratas machos se observó atrofia de testículos, epidídimo, próstata, túbulos seminíferos y/o reducción en el recuento espermático. En ratas hembras, se observó tamaño reducido de ovarios y útero. La reducción del recuento de espermatozoides en ratas macho fue reversible al cesar la dosificación en un estudio. La degeneración tubular testicular también se observó en un estudio intravenoso de 4 semanas de sirolimus en monos a dosis que eran aproximadamente iguales a la dosis clínica (ajustada para la superficie corporal). Embarazo: Sirolimus resultó embrio/fetotóxico en ratas, con dosis aproximadamente 0,2 a 0,5 veces la dosis clínica en humanos ajustada según la superficie corporal. La toxicidad embrionaria/fetal se manifestó como mortalidad y reducción del peso fetal (con retrasos asociados en la osificación del esqueleto). Sin embargo, no se registraron evidencias de teratogénesis. En combinación con la CsA, las ratas registraron una mayor mortalidad embrionaria/fetal que con Rapamune administrado como agente único. No se registraron alteraciones en el desarrollo del conejo con una dosificación maternalmente tóxica con dosis aproximadamente 0,3 a 0,8 veces la dosis clínica ajustada según la superficie corporal. No se dispone de estudios adecuados y bien controlados en mujeres embarazadas. Deberá utilizarse un método anticonceptivo eficaz antes de iniciar el tratamiento con Rapamune, durante el tratamiento y hasta 12 semanas después de haberse interrumpido la medicación. Se prescribirá Rapamune durante el embarazo sólo en aquellos casos en que el beneficio potencial de la paciente supere el riesgo potencial del embrión/feto. Utilización durante la lactancia: El sirolimus se excreta en mínima cantidad en la leche de ratas en período de lactancia. Sin embargo, no se sabe si el sirolimus se excreta en la leche humana. Se desconocen los perfiles farmacocinético y de seguridad del sirolimus en lactantes. Dado que son muchas las drogas que se excretan en la leche humana y dada la posibilidad de que se produzcan reacciones adversas secundarias al sirolimus en lactantes alimentados al pecho materno, deberá tomarse la decisión de interrumpir la alimentación al pecho o de interrumpir el tratamiento, teniendo en cuenta la importancia que éste pudiera tener para la madre. Utilización en Pediatría: Trasplante renal: No se ha establecido la seguridad y la eficacia de Rapamune en pacientes por debajo de los 13 años de edad. Se ha evaluado la seguridad y eficacia de Rapamune Solución oral y Rapamune Comprimidos en niños de 13 años o mayores considerados de riesgo inmunológico reducido a moderado. El empleo de Rapamune solución oral y Rapamune comprimidos en esta subpoblación de niños de 13 años o mayores se encuentra avalado por los resultados de estudios clínicos adecuados y bien controlados con Rapamune Solución oral en adultos y datos farmacocinéticos adicionales en receptores pediátricos de trasplante renal. La información de seguridad y eficacia de un estudio clínico controlado en receptores pediátricos y adolescentes ( < 18 años) de trasplante renal considerados de alto riesgo inmunológico, determinado por antecedentes de uno o más episodios de rechazo agudo y/o por la presencia de nefropatía crónica por aloinjerto, no avalan el uso crónico de Rapamune Solución oral o Comprimidos en combinación con inhibidores de la calcineurina y corticosteroides, debido al mayor riesgo de anormalidades lipídicas y deterioro de la función renal asociado con estos regímenes inmunosupresores, sin mayores beneficios con respecto al rechazo agudo, sobrevida del injerto o del paciente. Linfangioleiomiomatosis: La seguridad y eficacia de Rapamune en pacientes pediátricos < 18 años de edad no ha sido establecida. Utilización en Geriatría: Los estudios clínicos con Rapamune Solución Oral o Rapamune Comprimidos Recubiertos no incluyeron un número suficiente de pacientes mayores de 65 años o más como para determinar si la seguridad y la eficacia en esta población difieren respecto de la eficacia y la seguridad en pacientes más jóvenes. La información respecto de las concentraciones basales de sirolimus indican que no es necesario realizar ajustes en la dosificación, en función de la edad, en pacientes geriátricos con trasplante renal. En general, la selección de dosis para un paciente de edad avanzada debe ser prudente, normalmente comenzando en el extremo inferior del rango de dosificación, lo que refleja la mayor frecuencia de disminución de la función hepática o cardiaca y de la enfermedad concomitante u otro tratamiento farmacológico. Pacientes con disfunción hepática: La dosis de mantenimiento de Rapamune debe ser reducida en pacientes con disfunción hepática (ver Dosificación). Pacientes con disfunción renal: No se requiere ajuste de la dosis en pacientes con disfunción renal (ver Dosificación).
Interacciones.
Se sabe que el sirolimus constituye un sustrato adecuado, tanto para el citocromo CYP3A4, como para la glucoproteína P. Más abajo se detallan las interacciones farmacocinéticas que pueden producirse entre el sirolimus y los medicamentos que se administren en forma concomitante. Sólo se han realizado estudios de interacción entre drogas con los medicamentos que se describen más abajo. Ciclosporina: Se demostró que la ciclosporina, un sustrato e inhibidor de CYP3A4 y de la glicoproteína P, aumentaba las concentraciones de sirolimus cuando se administraba con este mismo. Para disminuir el efecto de esta interacción con la ciclosporina, se recomienda tomar Rapamune 4 horas después de la administración de la solución oral y/o cápsulas de ciclosporina. Si se suspende la ciclosporina de la terapia combinada con Rapamune, se necesitan dosis más elevadas de Rapamune para mantener los rangos de concentración recomendados de sirolimus (ver Dosificación y Farmacología). Inductores e inhibidores potentes de la CYP3A4 y la glicoproteína P: Evite el uso concomitante de sirolimus con inductores potentes (ej., Rifampina, rifabutina) e inhibidores potentes (ej. ketoconazol, voriconazol, itraconazol, eritromicina, telitromicina, claritromicina) de CYP3A4 y glicoproteína P. Se deben considerar agentes alternativos con menor potencial de interacción con sirolimus (ver Advertencias y Farmacología). Jugo de pomelo: Debido a que el jugo de pomelo inhibe el metabolismo del sirolimus mediado por CYP3A4, no debe tomarse ni utilizarse para la dilución de Rapamune (ver Dosificación, Interacciones y Farmacología). Inductores débiles y moderados o inhibidores de CYP3A4 y glicoproteína P: Tenga precaución al usar sirolimus con fármacos o agentes que son moduladores de CYP3A4 y glicoproteína P. Se puede necesitar un ajuste en la dosis de Rapamune y/o del fármaco coadministrado (ver Farmacología). Fármacos que aumentan la concentración de sirolimus: Bromocriptina, cimetidina, cisaprida, clotrimazol, danazol, diltiazem, fluconazol, inhibidores de proteasa (por ejemplo, VIH y hepatitis C que incluyen fármacos como ritonavir, indinavir, boceprevir y telaprevir), metoclopramida, nicardipina, troleandomicina, verapamilo. Fármacos u otros agentes que puede disminuir la concentración de sirolimus: Carbamazepina, fenobarbital, fenitoína, rifapentina, hierba de San Juan (Hypericum perforatum). Fármacos cuya concentración pueda ser aumentada cuando se utiliza Rapamune: Verapamilo. Vacunas: Los inmunosupresores pueden afectar la respuesta a la vacunación. Por lo tanto, durante el tratamiento con Rapamune, la vacunación puede ser menos eficaz. Debe evitarse el uso de vacunas vivas; las vacunas vivas pueden incluir, pero no se limitan a las siguientes: sarampión, paperas, rubéola, polio oral, BCG, fiebre amarilla, varicela y tifoidea TY21a.
Conservación.
Conservar a temperatura ambiente entre 20°C y 25°C. Proteger de la luz.
Sobredosificación.
La experiencia existente con sobredosificación es limitada. En términos generales, los efectos adversos de la sobredosis guardan relación con los que se detallan en la sección Reacciones adversas (ver Reacciones adversas). En todos los casos de sobredosis, se tomarán las medidas de apoyo habituales. Sobre la base de la limitada solubilidad en líquidos y la alta capacidad de unión a las proteínas plasmáticas y a los eritrocitos que tiene Rapamune, es posible deducir que Rapamune no responderá a la diálisis en grado significativo. En ratones y ratas, la dosis letal aguda por vía oral fue superior a los 800 mg/kg. Ante la eventualidad de una sobredosificación, concurrir al Hospital más cercano o comunicarse con alguno de los Centros de Toxicología del país. Entre otros: Hospital de Pediatría Ricardo Gutiérrez: Tel. (011) 4962-6666/2247. Hospital A. Posadas: Tel. (011) 4654-6648/4658-7777. Hospital de Pediatría "Dr. Garrahan": (011) 4943-1455. Información para los pacientes: Los pacientes deben recibir instrucciones completas sobre la dosificación. Deberá informarse a las mujeres potencialmente fértiles respecto de los riesgos que pueden producirse durante el embarazo y deberá indicárseles la necesidad de utilizar medidas anticonceptivas eficaces antes de iniciar un tratamiento con Rapamune, durante el tratamiento y hasta 12 semanas después de haber interrumpido el tratamiento. Será necesario informar a los pacientes que deberán limitar la exposición al sol y a los rayos UV, usando ropa que los proteja y utilizando pantallas protectoras con alto factor de protección, dado el mayor riesgo de padecer cáncer de piel.
Presentación.
Rapamune 0,5 mg: Envase por 100 comprimidos recubiertos. Rapamune 1 mg: Envase por 60 comprimidos recubiertos. Rapamune 2 mg: Envase por 30 comprimidos recubiertos.
Revisión.
Abril-2018. LPD: 11/APR17.
RAPAMUNE
PFIZER
Solución oral 1mg/ml
Agente inmunosupresor.
Composición.
Cada mililitro contiene: Sirolimus 1 mg. Excipientes: polisorbato 80 y phosal 50 PG.
Farmacología.
Descripción: Rapamune (sirolimus) es un agente inmunosupresivo. El sirolimus es una lactona macrocíclica producida por el Streptomyces hygroscopicus, cuyo nombre químico es: (3S, 6R, 7E, 9R, 10R, 12R, 14S, 15E, 17E, 19E, 21S, 23S, 26R, 27R, 34aS) 9, 10, 12, 13, 14, 21, 22, 23, 24, 25, 26, 27, 32, 33, 34, 34a -hexadecahidro - 9, 27 - dihidroxi -3 - [(1R) - 2 - [(1S, 3R, 4R) - 4 - hidroxi - 3 - metoxiciclohexil] - 1 - metiletil] - 10, 21 - dimetoxi - 6, 8, 12, 14, 20, 26 - hexametil - 23, 27 - epoxi - 3H - pirido [2,1-c] [1,4] oxaazaciclohentriacontina -1, 5, 11, 28, 29 (4H,6H,31H) - pentona. Su fórmula molecular es C51H79NO13 y su peso molecular 914,2. A continuación, figura la fórmula estructural del sirolimus.
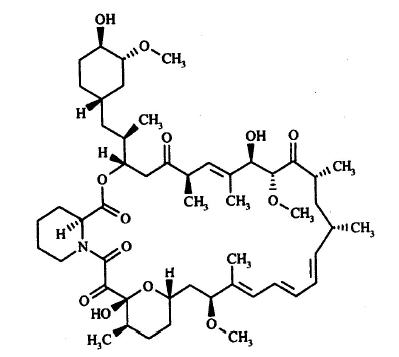
Sirolimus es un polvo blanco a blancuzco y es insoluble en agua pero soluble en alcohol bencílico, cloroformo, acetona y acetonitrilo. Mecanismo de acción: El sirolimus inhibe la activación y proliferación de los linfocitos T que se producen como respuesta a la estimulación inducida por antígenos y citoquinas (interleucina [IL]-2, IL-4 e IL-15), por un mecanismo diferente del observado con otros inmunosupresores. El sirolimus también inhibe la producción de anticuerpos. En las células, el sirolimus se une a la inmunofilina, proteína ligadora de la FK-12 (FK Binding Protein-12, FKBP-12), para generar un complejo inmunosupresor. El complejo sirolimus: FKBP-12 no ejerce efecto alguno sobre la actividad de la calcineurina. Este complejo se une e inhibe la activación del "objetivo de la rapamicina" de los mamíferos (mammallian Target of Rapamycin, mTOR), una quinasa reguladora importante. Esta inhibición suprime la proliferación de las células T inducida por las citoquinas, inhibiendo así la progresión de las fases G1 a S del ciclo celular. Los estudios llevados a cabo en modelos experimentales en ratones, ratas, cerdos, perros y/o monos sobrevivientes, muestran que el sirolimus prolonga la sobrevida de los injertos (riñón, corazón, piel, células de islotes, intestino delgado, pancreático-duodenal y médula ósea). El sirolimus previene el rechazo agudo de los aloinjertos de corazón y riñón en ratas y prolonga la sobrevida del órgano en ratas presensibilizadas. En algunos estudios, el efecto inmunosupresor del sirolimus perduró hasta seis meses después de la interrupción del tratamiento. Este efecto de tolerancia es específico para los aloantígenos. En modelos (roedores) con enfermedad autoinmune, el sirolimus suprime los eventos mediados por fenómenos inmunológicos asociados con: lupus eritematoso sistémico, artritis inducida por colágeno, diabetes autoinmune tipo I, miocarditis autoinmune, encefalomielitis alérgica experimental, enfermedad injerto versus huésped y uveorretinitis autoinmune. La linfangioleiomiomatosis consiste en la infiltración del tejido pulmonar con células similares a las del músculo liso, que albergan mutaciones inactivadoras del gen del complejo de esclerosis tuberosa (TSC) (células LAM). La pérdida de la función del gen TSC activa la ruta de señalización mTOR, dando como resultado la proliferación celular y la liberación de factores de crecimiento linfangiogénicos. Sirolimus inhibe la vía mTOR activada y, por tanto, la proliferación de células LAM. Farmacodinamia: La administración por vía oral de Rapamune, a dosis de 2 mg/día y 5 mg/día, redujo significativamente la incidencia de rechazo de órganos en pacientes con trasplante renal de leve a moderado riesgo inmunológico a los 6 meses tras el trasplante, en comparación con azatioprina o placebo (ver Estudios Clínicos). No hubo ninguna ventaja demostrable en la eficacia de una dosis de mantenimiento diaria de 5 mg con una dosis de carga de 15 mg sobre una dosis de mantenimiento diaria de 2 mg con una dosis de carga de 6 mg. El monitoreo terapéutico del fármaco debe usarse para mantener los niveles de sirolimus dentro del rango objetivo (ver Dosificación). Farmacocinética: La actividad farmacocinética de sirolimus, ha sido determinada luego de la administración en pacientes sanos, pacientes pediátricos, pacientes con deterioro hepático y pacientes con trasplante renal. Los parámetros farmacocinéticos de sirolimus en pacientes adultos con trasplante renal después de la administración de dosis múltiples de Rapamune 2 mg, en combinación con ciclosporina y corticoides, se resumen en la siguiente tabla.
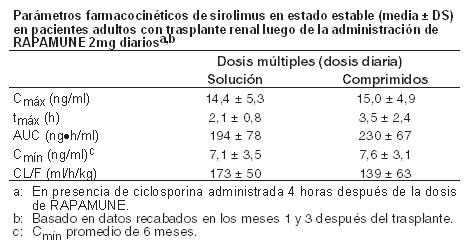
Las concentraciones mínimas de sirolimus en sangre entera, determinadas por Cromatografía Líquida/Espectrometría de masas en tándem (LC/MS/MS), se correlacionaron significativamente con el ABCt,ss. Luego de la administración repetida dos veces al día sin dosis inicial de carga en un estudio de dosis múltiples, la concentración mínima promedio de sirolimus aumenta aproximadamente 2 a 3 veces en los primeros 6 días de tratamiento, tiempo en el que alcanza el estado estable. Una dosis de carga 3 veces superior a la dosis de mantenimiento proporcionará concentraciones cercanas al estado estable dentro de las 24 horas en la mayoría de los pacientes (ver Dosificación y Advertencias). Absorción: Luego de la administración de Rapamune (sirolimus) Solución Oral, el sirolimus se absorbe rápidamente. El tiempo medio hasta alcanzar la concentración máxima (Cmáx) es de aproximadamente una hora después de una dosis única en pacientes sanos y de aproximadamente dos horas después de dosis orales múltiples en pacientes con trasplante renal. Luego de la administración de Rapamune comprimidos en pacientes sanos, la biodisponibilidad media de sirolimus fue aproximadamente un 27% más alto en relación a la solución. Los comprimidos de sirolimus no son bioequivalentes a la solución; sin embargo, la equivalencia clínica ha sido demostrada a un nivel de dosis de 2 mg. La concentración de sirolimus, luego de la administración de Rapamune Solución Oral en pacientes con trasplante renal estable, son dosis proporcionales, entre 3 y 12 mg/m2. Efectos de los alimentos: Para minimizar la variabilidad en las concentraciones de sirolimus, tanto Rapamune Solución Oral como los comprimidos deben tomarse consistentemente con o sin alimentos (ver Dosificación). En sujetos sanos, una comida rica en grasa (861,8 kcal, 54,9% kcal de grasa) aumentó la exposición total media (ABC) del sirolimus en un 23 a 35%, en comparación con el ayuno. El efecto del alimento sobre la Cmáx media del sirolimus fue inconsistente dependiendo de la forma de dosificación de Rapamune evaluada. Distribución: La relación sangre/plasma del sirolimus (± DE) fue 36 (± 18) en pacientes con trasplante renal alogénico estables, observándose que el sirolimus se distribuye en forma extensiva en los distintos elementos de la sangre. El volumen medio de distribución (Vss/F) del sirolimus con la administración de Rapamune es de 12 ± 8 l/kg. En los seres humanos, el sirolimus se une extensamente a las proteínas plasmáticas (aproximadamente 92 %). En el hombre, se demostró que la unión del sirolimus se encuentra asociada principalmente a la albúmina sérica (97 %), a la glucoproteína ácida a1 y a las lipoproteínas. Metabolismo: El sirolimus constituye un sustrato adecuado, tanto para el citocromo P450 IIIA4 (CYP3A4), como para la glucoproteína P. Sirolimus es metabolizado en forma extensiva en la pared instestinal e hígado y es transportado desde los enterocitos del intestino delgado al lumen del intestino. Los inhibidores de CYP3A4 y glucoproteína P aumentan las concentraciones de sirolimus. Los inductores de CYP3A4 y glucoproteína P disminuyen las concentraciones de sirolimus (ver Advertencias e Interacciones). El sirolimus es metabolizado en forma extensiva por O-desmetilación y/o por hidroxilación. En la sangre entera, se pueden identificar siete (7) metabolitos principales, incluyendo los derivados hidroxi, desmetil e hidroxidesmetil. Algunos de estos metabolitos también pueden detectarse en las muestras de plasma, de materia fecal y urinarias. Los glucurónidos y los sulfatos conjugados no se encuentran presentes en ninguna de las matrices biológicas. En los seres humanos, el sirolimus constituye el principal componente en la sangre entera y contribuye en más del 90 % con la actividad inmunosupresora. Excreción: Después de la administración de una dosis única de sirolimus [C14] a voluntarios sanos, la mayor parte de la radioactividad (91 %) fue recuperada en las heces y solamente una pequeña cantidad (2,2 %) se excretó en la orina. La vida media de eliminación terminal (t1/2) promedio ± DS del sirolimus después de dosis múltiples de Rapamune Solución oral en pacientes estables con trasplante renal fue de alrededor de 62 ± 16 horas. Concentraciones de sirolimus (equivalencias cromatográficas) observadas en estudios clínicos de Fase 3: Las siguientes concentraciones de sirolimus (equivalencias cromatográficas) se observaron en estudios clínicos de Fase 3, para profilaxis del rechazo de órganos en pacientes con trasplante renal de novo (ver Estudios Clínicos).
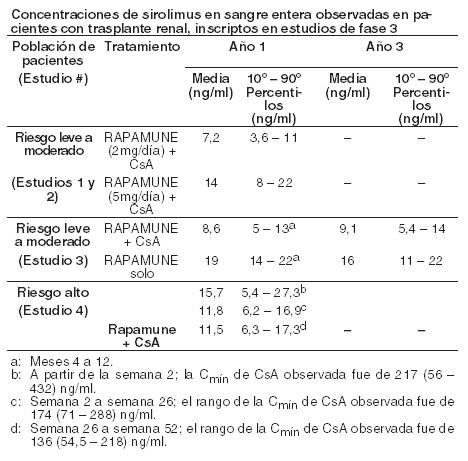
La discontinuación de la ciclosporina y los aumentos simultáneos en las concentraciones mínimas de sirolimus hasta el estado de equilibrio requerían aproximadamente 6 semanas. Tras la discontinuación de la ciclosporina, se requirieron dosis más altas de Rapamune debido a la ausencia de inhibición del metabolismo del sirolimus y el transporte por ciclosporina y para lograr concentraciones de referencia más altas de sirolimus durante la administración controlada por concentración (ver Dosificación e Interacciones). Linfangioleiomiomatosis: En un estudio clínico en pacientes con linfangioleiomiomatosis, la concnetración media de sirolimus en sangre entera, luego de 3 semanas recibiendo comprimidos de sirolimus a dosis de 2 mg/día, fue de 6,8 ng/ml (rango intercuartil 4,6 a 9,0 ng/ml; n = 37). Farmacocinética en poblaciones especiales: Pacientes con compromiso hepático: Se administró Rapamune Solución oral (15 mg) como dosis oral única a sujetos con función hepática normal y a pacientes con deterioro hepático primario grado A (leve), B (moderado) o C (severo) de la clasificación de Child-Pugh. En comparación con los valores del grupo con función hepática normal, el grupo con compromiso hepático leve, moderado y severo presentaron valores medios del 43 %, 94 % y 189 % más altos de ABC respectivamente, sin diferencias significativas estadísticamente en la Cmáx media. A medida que la severidad del deterioro de la función hepática, hubo aumentos constantes en la media de sirolimus t1/2, y disminuciones en la eliminación media de sirolimus normalizado para el peso corporal (CL/ F/kg). Deberá reducirse la dosis de mantenimiento de Rapamune en aproximadamente un tercio en pacientes con compromiso hepático leve a moderado y en aproximadamente un medio en pacientes con compromiso hepático severo (ver Dosificación). No es necesario en pacientes con compromiso hepático leve, moderado o severo modificar la dosis de carga de Rapamune. Deberá considerarse necesario el monitoreo en todos los pacientes con disfunción hepática (ver Dosificación). Pacientes con disfunción renal: No se conoce el efecto de la insuficiencia renal sobre la farmacocinética del sirolimus. Sin embargo, existe un mínimo (2,2%) de excreción renal del fármaco o de sus metabolitos en voluntarios sanos. Las dosis de carga y mantenimiento de Rapamune no necesitan ser ajustadas en pacientes con insuficiencia renal (ver Dosificación). Pacientes pediátricos con trasplante renal: Se recabaron datos farmacocinéticos del sirolimus en estudios de concentración controlada en pacientes pediátricos con trasplante renal que también recibían ciclosporina y corticosteroides. Los rangos deseados de concentración mínima fueron de 10-20 ng/ml para los 21 chicos que recibieron los comprimidos o de 5-15 ng/ml para el único niño que recibió la solución oral. Los niños entre 6 y 11 años (n = 8) recibieron dosis medias ± DS de 1,75 ± 0,71 mg/día (0,064 ± 0,018 mg/Kg; 1,65 ± 0,43 mg/m2). Los niños entre 12 y 18 años (n = 14) recibieron dosis medias ± DS de 2,79 ± 1,25 mg/día (0,053 ± 0,0150 mg/Kg; 1,86 ± 0,61 mg/m2). En el momento del dosaje sanguíneo de sirolimus para la evaluación farmacocinética, la mayoría (80 %) de estos pacientes pediátricos habían recibido la dosis de sirolimus 16 horas después de la dosis única diaria de ciclosporina.
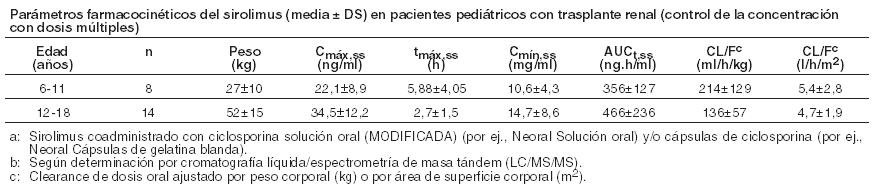
La siguiente Tabla resume los datos farmacocinéticos obtenidos en pacientes pediátricos bajo diálisis, con disfunción renal crónica:
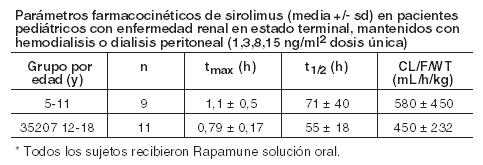
Pacientes geriátricos: Los estudios clínicos de Rapamune no incluyeron un número suficiente de pacientes > 65 años de edad para determinar si responderán de manera diferente que los pacientes más jóvenes. Después de la administración de Rapamune Solución Oral o Comprimidos, los datos de concentración de sirolimus en pacientes con trasplante renal mayores de 65 años fueron similares a los de la población adulta de 18 a 65 años. Género: El clearance de sirolimus en los varones fue un 12% menor que en las mujeres; los sujetos varones tenían un t1/2 significativamente más largo que las mujeres (72,3 horas versus 61,3 horas). No se recomiendan los ajustes de dosis basados en el género. Raza: En los ensayos de Fase 3 para la profilaxis del rechazo de órganos tras el trasplante renal utilizando solución o comprimidos de Rapamune y solución oral de ciclosporina (por ejemplo, Neoral® Solución oral y/o cápsulas de ciclosporina (por ejemplo, Neoral® Cápsulas de gelatina blanda) (ver Estudios Clínicos), no hubo diferencias significativas en las concentraciones medias de sirolimus a lo largo del tiempo entre los pacientes de raza negra (n = 190) y pacientes que no son de raza negra (n = 852) durante los primeros 6 meses después del trasplante. Interacción fármaco con fármaco: Es sabido que el sirolimus es un sustrato tanto para el citocromo CYP3A4 como para la glicoproteína P. La interacción farmacocinética entre el sirolimus y los fármacos administrados concomitantemente se discute a continuación. No se han realizado estudios de interacción con fármacos distintos de los descriptos a continuación. Ciclosporina: La ciclosporina es un sustrato e inhibidor de CYP3A4 y de la glicoproteína P. El sirolimus debe tomarse 4 horas después de la administración de la solución oral y/o cápsulas de ciclosporina. Las concentraciones de sirolimus pueden disminuir cuando se suspende la ciclosporina, a menos que la dosis de Rapamune sea aumentada (ver Dosificación e Interacciones). En un estudio de dosis única de interacción fármaco-fármaco, 24 voluntarios sanos recibieron 10 mg de Rapamune Solución Oral simultáneamente o 4 horas después de una dosis de 300 mg de cápsulas de gelatina blanda Neoral® (cápsulas de ciclosporina). Para la administración simultánea, la Cmáx media y el ABC del sirolimus, después de la administración simultánea, se incrementaron en un 116% y 230%, respectivamente, con relación a la administración de sirolimus solo. Sin embargo, cuando se administró 4 horas después de la administración de Neoral® Soft Gelatin Capsules (cápsulas de ciclosporina), sirolimus Cmáx y ABC aumentaron sólo en un 37% y 80%, respectivamente, en comparación con la administración de Rapamune solo. En un estudio de interacción fármaco-fármaco de dosis única, 33 voluntarios sanos recibieron 5 mg de Rapamune Solución Oral solo, 2 horas antes y 2 horas después de una dosis de 300 mg de Neoral® Soft Gelatin Capsules (cápsulas de ciclosporina). Cuando se administraron 2 horas antes de la administración de Neoral® Soft Gelatin Capsules (cápsulas de ciclosporina), Cmáx y AUC de sirolimus fueron comparables a aquellas con administración de sirolimus solo. Sin embargo, cuando se dieron 2 horas después, la Cmáx media y el ABC del sirolimus aumentaron en 126% y 141%, respectivamente, con relación a la administración de sirolimus solo. La Cmáx y el ABC de la ciclosporina no fueron significativamente afectados cuando se administraron Rapamune Solución Oral simultáneamente o cuando se administraron 4 horas después de Neoral® Soft Gelatin Capsules (cápsulas de ciclosporina). Sin embargo, tras la administración de dosis múltiples de sirolimus administrado 4 horas después de Neoral® en pacientes con trasplante renal durante 6 meses, se redujo el clearance de la dosis oral de ciclosporina y se requirieron dosis más bajas de Neoral® Soft Gelatin Capsules [cápsulas de ciclosporina) para mantener la concentración de ciclosporina de referencia. En un estudio de dosis múltiple en 150 pacientes con psoriasis, se administró sirolimus 0,5, 1,5 y 3 mg/m2/ día simultáneamente con solución oral de Sandimmune® (solución oral de ciclosporina) 1,25 mg kg/día. El aumento de las concentraciones mínimas medias de sirolimus osciló entre el 67% y el 86% con respecto a cuándo se administró Rapamune sin ciclosporina. La variabilidad intersujeto (CV%) para las concentraciones mínimas de sirolimus, varió de 39.7% a 68.7%. No hubo un efecto significativo de dosis múltiples de sirolimus en las concentraciones de la ciclosporina después de la administración de la solución oral de Sandimmune® (administración oral de ciclosporina). Sin embargo, el CV% fue mayor (rango 85.9% - 165%) que los de estudios previos. Diltiazem: Diltiazem es un sustrato e inhibidor de CYP3A4 y la glicoproteína P; las concentraciones de sirolimus deben ser monitoreadas y puede ser necesario un ajuste de dosis (ver Interacciones). La administración oral simultánea de 10 mg de solución oral de sirolimus y 120 mg de diltiazem a 18 voluntarios sanos afectó significativamente la biodisponibilidad del sirolimus. La Cmáx, tmax y ABC de sirolimus aumentaron 1,4, 1,3 y 1,6 veces, respectivamente. El sirolimus no afectó la farmacocinética del diltiazem ni de sus metabolitos desacetildiltiazem y desmetildiltiazem. Eritromicina: La eritromicina es un sustrato e inhibidor de CYP3A4 y glicoproteína P; no se recomienda la administración simultánea de sirolimus comprimidos y eritromicina (ver Advertencias e Interacciones). La administración oral simultánea de 2 mg diarios de solución oral de sirolimus y 800 mg de eritromicina cada 8 hs como comprimidos de eritromicina etil succinato en estado estacionario a 24 voluntarios sanos afectó significativamente la biodisponibilidad de sirolimus y eritromicina. La Cmáx y el ABC del sirolimus aumentaron respectivamente 4,4 y 4,2 veces y el tmax aumentó en 0,4 horas. La
Cmáx y el ABC de eritromicina aumentaron 1,6 y 1,7 veces, respectivamente, y el tmax aumentó 0,3 h. Ketoconazol: El ketoconazol es un fuerte inhibidor de CYP3A4 y la glicoproteína P; no se recomienda la coadministración de comprimidos de sirolimus y ketoconazol (ver Advertencias e Interacciones). La administración de dosis múltiples de ketoconazol afectó significativamente la tasa y el grado de absorción y la exposición al sirolimus después de la administración de la solución oral de Rapamune, reflejada por aumentos de la Cmáx, tmax y ABC del sirolimus, de 4,3 veces, 38% y 10,9 veces, respectivamente. Sin embargo, la t½ terminal del sirolimus no fue cambiada. La dosis única de sirolimus no afectó las concentraciones plasmáticas de ketoconazol en el estado de equilibrio a las 12 horas. Rifampicina: La rifampina es un fuerte inductor de CYP3A4 y de la glicoproteína P; no se recomienda la coadministración de Rapamune comprimidos con rifampicina. En pacientes donde está indicada la rifampicina, se deben considerar agentes terapéuticos alternativos con menor potencial de inducción enzimática (ver Advertencias e Interacciones). El pretratamiento de 14 voluntarios sanos con dosis múltiples de rifampicina, 600 mg diarios durante 14 días, seguido de una dosis única de 20 mg de sirolimus en solución oral, redujo significativamente el ABC y la Cmáx del sirolimus en un 82% y 71%, respectivamente. Verapamilo: El verapamilo es un sustrato e inhibidor de CYP3A4 y de la glicoproteína P; las concentraciones de sirolimus deben ser monitoreadas y puede ser necesario un ajuste de dosis; (ver Interacciones). La administración oral simultánea de 2 mg diarios de solución oral de sirolimus y 180 mg cada 12 hs de verapamilo en estado estacionario, a 26 voluntarios sanos, afectó significativamente la biodisponibilidad de sirolimus y verapamilo. La Cmáx y ABC de sirolimus se incrementaron 2,3 y 2,2 veces, respectivamente, sin cambio sustancial en la tmax. La Cmáx y el ABC del enantiómero S(-) farmacológicamente activo del verapamilo, aumentaron 1,5 veces y el tmax disminuyó 1,2 hs. Medicamentos que pueden ser coadministrados sin el ajuste de la dosis: No se observaron interacciones farmacocinéticas clínicamente significativas entre fármacos, en los estudios con los fármacos enumerados a continuación. Sirolimus y estos fármacos pueden ser coadministrados sin ajustes de dosis. Aciclovir. Atorvastatina. Digoxina. Gliburida. Nifedipina. Norgestrel/etinilestradiol. Prednisolona. Trimetoprima-sulfametoxazol. Otras interacciones fármaco - fármaco: La coadministración de Rapamune con otros inhibidores potentes conocidos de CYP3A4 y/o glicoproteína P (tales como voriconazol, itraconazol, telitromicina o claritromicina) u otros inductores potentes conocidos de CYP3A4 y / o P-gp (como rifabutina) no es recomendado (ver Advertencias e Interacciones). En pacientes en los que se indican potentes inhibidores o inductores de CYP3A4, se deben considerar agentes terapéuticos alternativos con menor potencial de inhibición o inducción de CYP3A4. Se debe tener cuidado cuando los fármacos u otras sustancias que son sustratos y/o inhibidores o inductores de CYP3A4, se administren concomitantemente con Rapamune. Otros fármacos que tienen el potencial de aumentar las concentraciones sanguíneas de sirolimus incluyen (pero no se limitan a): Bloqueadores de los canales de calcio: nicardipina. Agentes antifúngicos: clotrimazol, fluconazol. Antibióticos: troleandomicina. Agentes procinéticos gastrointestinales: cisaprida, metoclopramida. Otros fármacos: bromocriptina, cimetidina, danazol, inhibidores de la proteasa (ej. para VIH y hepatitis C que incluyen fármacos como ritonavir, indinavir, boceprevir, telaprevir. Otras drogas que tienen el potencial de disminuir la concentración de sirolimus (pero no se limitan a): Anticonvulsionantes: carbamazepina, fenobarbital, fenitoína. Antibióticos: rifapentina. Otras interacciones fármaco - alimentos: El jugo de pomelo reduce el metabolismo del fármaco mediado por CYP3A4. El jugo de pomelo no debe tomarse ni utilizarse para la dilución de Rapamune (ver Dosificación e Interacciones). Otras interacciones con hierbas: La hierba de San Juan (Hypericum perforatum) es un inductor del CYP3A4 y de la glicoproteína P. Dado que el sirolimus es un sustrato tanto para el citocromo CYP3A4 como para la glicoproteína P, existe el potencial de que el uso de la hierba de San Juan en pacientes que reciben Rapamune, podría reducir las concentraciones de sirolimus (ver Interacciones). Estudios clínicos: La seguridad y eficacia de Rapamune Solución Oral en la prevención del rechazo de órganos con posterioridad al trasplante renal fueron evaluadas en dos estudios multicéntricos, controlados, doble-ciegos y aleatorios. En estos estudios se compararon dos niveles de dosis de Rapamune Solución Oral (2 mg y 5 mg, una vez al día), con azatioprina (Estudio 1) o placebo (Estudio 2), administrados en combinación con CsA y corticosteroides. El Estudio 1 fue realizado en 38 centros de los Estados Unidos. Se reclutaron 719 pacientes que fueron asignados al azar a uno u otro grupo de tratamiento con posterioridad al trasplante: 284 pacientes fueron asignados al grupo con Rapamune Solución Oral 2 mg diarios, 274 fueron asignados al grupo con Rapamune Solución Oral 5 mg diarios y, 161, al grupo con azatioprina 2 a 3 mg/kg diarios. El Estudio 2 comparativo de Rapamune (2 mg y 5 mg una vez al día) se llevó a cabo en Australia, Canadá, Europa y los Estados Unidos, en un total de 34 centros. Se incorporaron en este estudio 576 pacientes, que se asignaron aleatoriamente a uno u otro grupo de tratamiento antes de producirse el trasplante: 227 fueron asignados al grupo con Rapamune Solución Oral 2 mg diarios, mientras que 219 fueron asignados al grupo con Rapamune Solución Oral 5 mg diarios y, 130 pacientes, al grupo con placebo. En ambos estudios, se prohibió el uso de terapia de inducción de anticuerpos anti-linfocitos. El fracaso del tratamiento fue definido como el primer episodio agudo de rechazo (confirmado por biopsia), pérdida del órgano o muerte. Las siguientes Tablas resumen los resultados de los análisis de la eficacia primaria en estos estudios. Rapamune Solución Oral, administrado en dosis de 2 mg/día y 5 mg/día, redujo significativamente la incidencia de fracaso al tratamiento (estadísticamente significativa al nivel de < 0,025; nivel de significación nominal ajustado para comparaciones de dosis múltiples) 6 meses después del trasplante, en comparación con la azatioprina y el placebo.
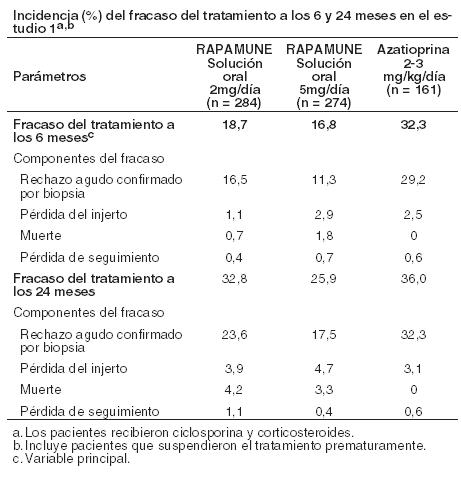
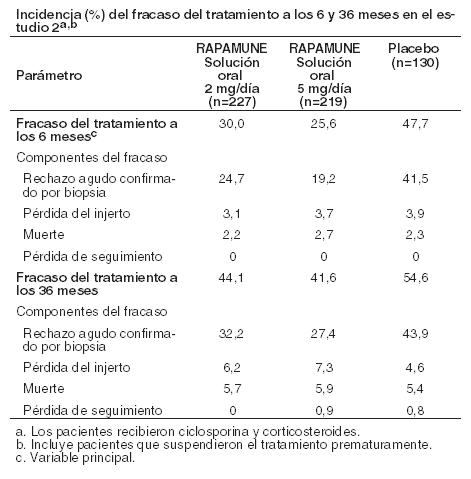
Los objetivos co-primarios fueron la sobrevida del paciente y del injerto al cabo de 1 año. La siguiente Tabla presenta la sobrevida del injerto y del paciente después de 1 y 2 años en el Estudio 1 y de 1 y 3 años en el Estudio 2. Los índices de sobrevida del injerto y del paciente fueron similares entre los pacientes tratados con Rapamune y los tratados con los agentes comparativos.
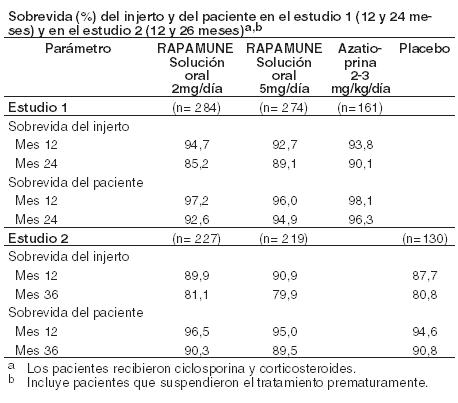
La reducción en la incidencia de episodios de primer rechazo agudo confirmado por biopsia en los pacientes tratados con Rapamune en comparación con los grupos de control incluyó una reducción en todos los grados de rechazo. En el estudio 1, que fue prospectivamente estratificado por raza dentro de cada centro, el índice de fracaso del tratamiento fue similar con Rapamune 2 mg/día e inferior con Rapamune 5 mg/día en comparación con la azatioprina en los pacientes de raza negra. En el estudio, que no fue prospectivamente estratificado por raza, el índice de fracaso del tratamiento fue similar con ambas dosis de Rapamune en comparación con el placebo en los pacientes de raza negra. La decisión de usar la dosis más alta de Rapamune Solución Oral en pacientes de raza negra debe ser comparada con el mayor riesgo de eventos adversos dependientes de la dosis que se observaron con la dosis de 5 mg de Rapamune Solución Oral (ver Reacciones Adversas).
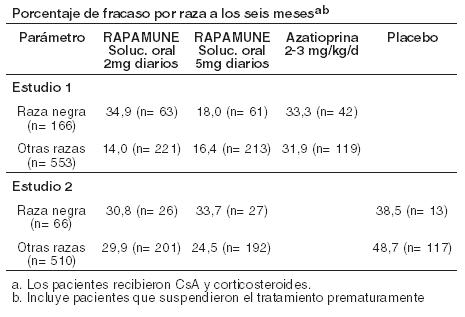
Los índices medios de filtración glomerular (IFG) un año después del trasplante se calcularon empleando la ecuación de Nankivell para todos los sujetos incluidos en cada estudio que contaban con una determinación de creatinina sérica a los 12 meses. En ambos estudios, el IFG medio al año fue inferior en los pacientes tratados con CsA y Rapamune que en los tratados con CsA y azatioprina o placebo.

Dentro de cada grupo de tratamiento en los Estudio 1 y 2, el IFG medio 1 año después del trasplante fue inferior en aquellos pacientes que presentaron por lo menos un episodio de rechazo agudo confirmado por biopsia que en los que no lo hicieron. La función renal debe ser controlada, y se debe considerar un apropiado ajuste de la terapia inmunosupresiva, en pacientes con niveles de creatinina sérica, elevados o en aumento (ver Advertencias). Rapamune comprimidos: Se demostró que la seguridad y la eficacia de Rapamune Solución Oral y Rapamune comprimidos para la prevención del rechazo de órganos tras el trasplante renal, eran clínicamente equivalentes en un ensayo controlado, aleatorizado y multicéntrico (ver Farmacología). Estudio de la suspensión de ciclosporina en pacientes con trasplante renal: Se evaluó la seguridad y la eficacia de Rapamune como régimen de mantenimiento, a partir de la suspensión de la CsA, a los tres y cuatro meses después del trasplante renal. El estudio 3 fue multicéntrico, controlado y aleatorio que se llevó a cabo en 57 centros de Australia, Canadá y Europa. Se incorporaron en el estudio 525 pacientes. Todos los pacientes recibieron Rapamune Comprimidos. En este estudio se comparó a los pacientes que recibieron Rapamune, CsA y corticosteroides en forma continua, con pacientes que recibieron el mismo tratamiento estandarizado durante los primeros tres meses posteriores al trasplante (período previo a la asignación al azar a uno de los tratamientos) y luego se les suspendió la administración de CsA. Durante el período de suspensión de la CsA, las dosis de Rapamune se ajustaron hasta alcanzar las concentraciones basales de sirolimus deseadas en sangre entera (16 a 24 ng/ml, hasta el mes 12, luego 12 a 20 ng/ml, expresados como valores de ensayo cromatográficos). A los tres meses, 430 pacientes fueron igualmente seleccionados al azar para recibir, o bien Rapamune con CsA, o bien Rapamune como régimen de mantenimiento posterior a la suspensión de la CsA. Los pacientes aptos para participar de la selección al azar no debían haber presentado ningún episodio agudo de rechazo (grado 3 de Banff) o rechazo vascular dentro de las cuatro semanas previas a la asignación aleatoria y debían contar con niveles de creatinina sérica ≤ 4,5 mg/dl y con una función renal adecuada (según la opinión del investigador) como para tolerar la suspensión de la CsA. La variable primaria de eficacia fue la sobrevida del órgano a los 12 meses del trasplante. Las variables secundarias de eficacia fueron el índice de episodios agudos de rechazo confirmados por biopsia, la sobrevida de los pacientes, la incidencia de fracaso del tratamiento (definido como el primer episodio agudo de rechazo confirmado por biopsia, pérdida del órgano o muerte) y fracaso terapéutico (definido como la primera aparición de abandono del tratamiento, rechazo agudo, pérdida del injerto o muerte). En el cuadro que se encuentra más abajo, se resumen los resultados de este estudio respecto de la sobrevida de los pacientes y de los órganos a los 12, 24, 36, 48 y 60 meses en este estudio. A los 12, 24 y 36 meses, la supervivencia del injerto y del paciente fue similar en ambos grupos.
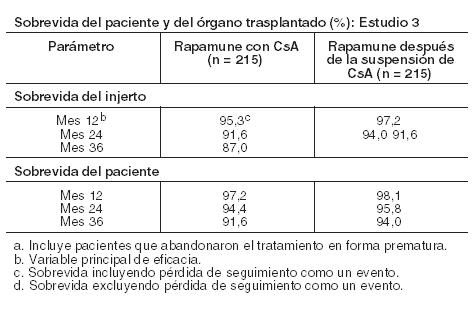
El siguiente cuadro resume los resultados del primer episodio de rechazo agudo comprobado por biopsia a los 12 y a los 60 meses. Respecto del primer episodio de rechazo agudo comprobado por biopsia, se observó una diferencia significativa entre los dos grupos del estudio, en el período que va desde la asignación al azar a uno u otro esquema de tratamiento hasta los 12 meses posteriores al trasplante. La mayoría de los episodios de rechazo agudo posteriores a la asignación a un esquema de tratamiento se produjeron dentro de los tres primeros meses posteriores a esta asignación al tratamiento.
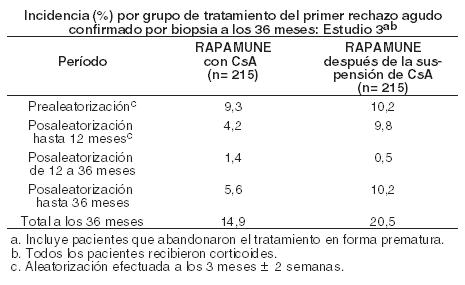
El siguiente cuadro resume el IFG calculado en el Estudio 3 (Estudio de la suspensión de CsA).
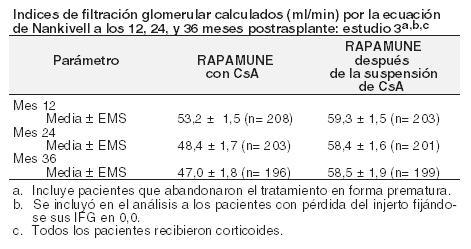
Los índices medios de filtración glomerular, a los 12, 24 y 36 meses, calculados por medio de la ecuación de Nankivell, fueron significativamente más altos en los pacientes que recibieron Rapamune como régimen de mantenimiento posterior a la suspensión de la CsA, que en el grupo de pacientes que recibió Rapamune y CsA. Los pacientes que presentaron un episodio agudo de rechazo en algún momento después del trasplante registraron un IFG más alto con posterioridad a la suspensión de la CsA, en comparación con los pacientes asignados al grupo con Rapamune y CsA. No hubo diferencias significativas en la IFG entre los grupos de pacientes que experimentaron rechazo agudo después de la aleatorización. Aunque el protocolo inicial fue diseñado para 36 meses, hubo una enmienda posterior para ampliar este estudio. Los resultados del grupo de la suspensión de la ciclosporina a los meses 48 y 60 fueron consistentes con los resultados al mes 36. El 52% (112/215) de los pacientes en el grupo de la suspensión de Rapamune con ciclosporina permaneció en terapia hasta el mes 60 y mostró un IFG sostenido. Pacientes de alto riesgo inmunológico con trasplante renal: Se evaluó Rapamune en un estudio clínico (Estudio 4) de 1 año de duración en pacientes de alto riesgo definidos como receptores de trasplante de raza negra y/o receptores de retrasplante renal por pérdida del aloinjerto anterior debido a razones inmunológicas y/o pacientes con alto panel de anticuerpos reactivos (PAR; nivel máximo de PAR > 80 %). Los pacientes recibieron sirolimus a una concentración-controlada y ciclosporina y corticosteroides según práctica local. La dosis de Rapamune se ajustó para alcanzar concentraciones de sirolimus de 10 a 15 ng/ml (método cromatográfico) a lo largo del período de estudio de 12 meses. La dosis de ciclosporina se ajustó para alcanzar concentraciones de referencia en sangre total de 200-300 ng/mL a lo largo de la semana 2, 150-200 ng/mL de la semana 2 a la semana 26 y 100-150 ng/mL de la semana 26 a la semana 52 para las concentraciones de concentraciones mínimas observadas. Se permitió inducción de anticuerpos por protocolo según lo definido prospectivamente en cada centro de trasplante, empleándose en el 88,4 % de los pacientes. El estudio se llevó a cabo en 35 centros de Estados Unidos. Un total de 224 pacientes recibió un trasplante y por lo menos una dosis de sirolimus y ciclosporina y comprendió 77,2 % de raza negra, 24,1 % con retrasplante renal y 13,5 % con alto PAR. La eficacia se evaluó con las siguientes variables, determinadas a los 12 meses: fracaso al tratamiento (definido como la primera aparición de rechazo agudo confirmado por biopsia, pérdida del injerto o muerte), primera aparición de pérdida del injerto o muerte, y función renal conforme a lo determinado por el IFG calculado con la fórmula de Nankivell. La Tabla a continuación resume los resultados de estas variables.

La sobrevida del paciente a los 12 meses fue del 94,6%. La incidencia de rechazo agudo confirmado por biopsia fue del 17,4 % y la mayoría de los episodios de rechazo agudo fueron de severidad leve. Conversión desde los inhibidores de calcineurina a Rapamune en pacientes con trasplante renal de mantenimiento: Se evaluó la conversión de inhibidores de la calcineurina (ICN) a Rapamune en pacientes con trasplante renal en mantenimiento desde los 6 meses hasta los 10 años postrasplante (Estudio 5). Este estudio fue multicéntrico, controlado y con asignación aleatoria llevado a cabo en 111 centros de Estados Unidos y Europa, y pretendía demostrar que la función renal se mejoró mediante la conversión de ICN a Rapamune. Se incluyeron y estratificaron por índice de filtración glomerular basal calculado (IFG 20-40 ml/min vs. mayor de 40 ml/min) 830 pacientes. En este ensayo no hubo ningún beneficio asociado con la conversión con respecto a la mejora de la función renal y una mayor incidencia de proteinuria en el grupo de conversión de Rapamune. La incorporación en el estrato de pacientes con índice de filtración glomerular basal calculado inferior a 40 ml/min se suspendió debido a un desequilibrio en los efectos secundarios, incluyendo neumonía, rechazo agudo, pérdida del injerto y muerte (ver Reacciones Adversas). El estudio comparó pacientes con trasplante renal (6-120 meses después del trasplante) cambiados de inhibidores de la calcineurina a Rapamune, con pacientes que continuaron recibiendo inhibidores de la calcineurina. Las medicaciones inmunosupresoras concomitantes incluyeron micofenolato mofetil (MMF), azatioprina (AZA) y corticoides. Se administró una única dosis inicial de carga de 12-20 mg de Rapamune, tras lo cual se ajustó la dosificación para alcanzar la concentración basal deseada de sirolimus en sangre de 8-20 ng/ml (método cromatográfico). La variable principal de eficacia fue el IFG calculado a los 12 meses después de la aleatorización. Las variables secundarias incluyeron rechazo agudo confirmado por biopsia, pérdida del injerto y muerte. Los hallazgos en el estrato de pacientes con IFG basal calculado mayor a 40 ml/min (conversión a Rapamune, n = 497; continuación con ICN, n = 246) se resumen a continuación. No se observó una mejoría clínica o estadísticamente significativa en el IFG de Nankivell en comparación con el basal.

El rango de la función renal y los índices de rechazo agudo, pérdida del injerto y muerte fueron similares al cabo de 1 y 2 años. Los eventos adversos emergentes del tratamiento se produjeron con mayor frecuencia durante los primeros 6 meses después de la conversión a Rapamune. Los índices de neumonía fueron significativamente superiores en el grupo de conversión a sirolimus. Mientras que los valores medios y medianas de la relación proteínas urinarias a creatinina fueron similares entre los grupos de tratamiento en la visita basal, se observaron valores medios y medianas de excreción de proteínas urinarias significativamente más elevados en el grupo de conversión a Rapamune al año y a los 2 años, como ilustra la Tabla a continuación (ver Advertencias). Además, en comparación con los pacientes que continuaron recibiendo inhibidores de la calcineurina, un mayor porcentaje de pacientes presentó una relación de proteínas urinarias a creatinina > 1 al cabo de 1 y 2 años de la conversión a sirolimus. Esta diferencia se observó tanto en pacientes que tenían una relación de proteínas urinarias a creatinina ≤ 1 como en aquellos cuya relación basal era > 1. Un mayor porcentaje de pacientes en el grupo de conversión a sirolimus desarrolló proteinuria nefrótica, de acuerdo con la relación proteínas urinarias a creatinina > 3,5 (46/482 [9,5 %] vs. 9/239 [3,8 %], aun cuando los pacientes con proteinuria nefrótica basal fueron excluidos. La incidencia de proteinuria nefrótica fue significativamente superior en el grupo de conversión al sirolimus en comparación con el grupo de continuación de inhibidores de la calcineurina con una relación basal de proteínas urinarias a creatinina > 1 (13/29 vs. 1/14), excluyéndose a los pacientes con proteinuria nefrótica basal.
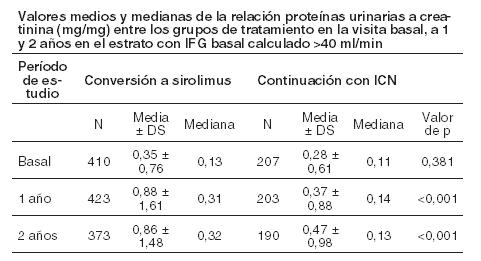
La información precedente debe tomarse en cuenta cuando se considere la conversión de inhibidores de la calcineurina a Rapamune en pacientes con trasplante renal estables debido a la falta de evidencia que demuestre que la función renal mejora luego de la conversión, al hallazgo de un mayor incremento en la excreción de proteínas urinarias y a una mayor incidencia de proteinuria nefrótica emergente del tratamiento después de la conversión a Rapamune. Esto pudo comprobarse entre los pacientes con excreción anormal existente de proteínas urinarias antes de la conversión. Conversión desde un régimen basado en ICN a un régimen basado en sirolimus en pacientes con trasplante hepático: Se evaluó en pacientes con trasplante hepático estable. El estudio clínico fue 2:1, aleatorizado, multicéntrico y controlado; realizado en 82 centros en todo el mundo, incluidos los EE.UU. y Europa, y tenía la intención de demostrar que la función renal se mejoró mediante la conversión de un CNI a Rapamune sin afectar negativamente la eficacia o la seguridad. Un total de 607 pacientes fueron inscritos. El estudio no demostró la superioridad de la conversión a un régimen basado en Rapamune en comparación con la continuación de un régimen basado en ICN en el IFG ajustado al inicio, estimada por Cockcroft-Gault, a los 12 meses (62 mL/min en el grupo de conversión Rapamune y 63 ml/min en el grupo de continuación de ICN). El estudio no demostró tampoco inferioridad en el grupo de conversión de Rapamune en comparación con el grupo de continuación de CNI (6,6% frente a 5,6%), con respecto a la variable principal de eficacia que consiste en la pérdida del injerto y la muerte (incluidos los pacientes con datos de supervivencia faltantes). Los casos de muertes en el grupo de conversión de Rapamune (15/393, 3,8%) fueron más elevados que en el grupo de continuación con ICN (3/214, 1,4%), aunque la diferencia no fue estadísticamente significativa. Los índices de suspensión prematura del estudio (principalmente debido a eventos adversos o falta de eficacia), los eventos adversos en general (infecciones, específicamente) y rechazo agudo del injerto hepático confirmado por biopsia a los 12 meses fueron significativamente superiores en el grupo de conversión Rapamune versus el grupo de continuación con ICN. Pacientes pediátricos con trasplante renal: Un estudio clínico abierto, controlado y aleatorizado de 36 meses de duración, llevado a cabo en 14 centros norteamericanos, evaluó Rapamune en receptores pediátricos (de 3 a < 18 años) de trasplante renal considerados de alto riesgo inmunológico de desarrollar nefropatía crónica por aloinjerto, definido como antecedentes de uno o más episodios de rechazo agudo del aloinjerto y/o presencia de nefropatía crónica por aloinjerto en una biopsia renal. Se distribuyeron al azar 78 sujetos en una relación de 2:1 para recibir Rapamune (concentración deseada de sirolimus de 5 a 15 ng/ml, por cromatografía, n = 53) en combinación con un inhibidor de la calcineurina y corticoides o para continuar con el tratamiento inmunosupresor basado en inhibidores de la calcineurina (n = 25). La variable principal del estudio fue el fracaso al tratamiento, definido como la primera aparición de ya sea rechazo agudo confirmado por biopsia, pérdida del injerto o muerte, y el estudio fue diseñado para demostrar la superioridad de Rapamune agregado a un régimen inmunosupresor basado en inhibidores de la calcineurina en comparación con un régimen basado en inhibidores de la calcineurina. La incidencia acumulada del fracaso al tratamiento hasta los 36 meses fue del 45,3 % en el grupo de Rapamune versus el 44,0% en el grupo de control, no demostrando superioridad. Se produjo un deceso en cada grupo. Se asoció el empleo de Rapamune en combinación con inhibidores de la calcineurina y corticoides con un mayor riesgo de deterioro de la función renal, anormalidades en los lípidos séricos (que incluyeron, entre otros, aumento del colesterol y triglicéridos séricos), e infecciones urinarias (ver Advertencias). Este estudio no avala el agregado de Rapamune al tratamiento inmunosupresor con inhibidores de la calcineurina en esta subpoblación de pacientes pediátricos con trasplante renal. Pacientes con Linfangioleiomiomatosis: Se evaluaron la seguridad y la eficacia de Rapamune para el tratamiento de la linfangioleiomiomatosis (LAM) en un estudio aleatorizado, doble ciego, multicéntrico y controlado. En este estudio se comparó Rapamune (con dosis ajustada para mantener las concentraciones mínimas en sangre entre 5-15 ng/ml) con placebo durante un período de tratamiento de 12 meses, seguido de un período de observación de 12 meses. Se enroló a ochenta y nueve (89) pacientes; 43 pacientes fueron aleatorizados para recibir placebo y 46 pacientes para recibir Rapamune. El criterio de valoración primario fue la diferencia entre los grupos en el índice de cambio (pendiente) por mes en el volumen espiratorio forzado en 1 segundo (VEF1). Durante el período de tratamiento, la pendiente VEF1 fue de -12 ± 2 mL por mes en el grupo placebo y 1 ± 2 mL por mes en el grupo Rapamune (diferencia de tratamiento = 13 mL (IC del 95%: 7, 18). La diferencia absoluta entre grupos en el cambio medio en el VEF1 durante el período de tratamiento de 12 meses fue 153 ml, o aproximadamente, el 11% del VEF1 medio en el enrolamiento. Se observaron mejoras similares respecto a la capacidad vital forzada (CVF). Después de la discontinuación de Rapamune, el deterioro en la función pulmonar se reanudó en el grupo de Rapamune, y se asemejó a la del grupo placebo (ver la Figura 1).
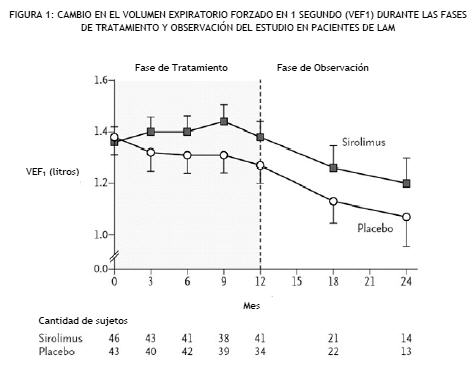
El índice de cambio durante 12 meses del factor D de crecimiento endotelial vascular (vascular endothelial growth factor D, VEGF-D), un factor de crecimiento linfangiogénico, que se ha demostrado que está elevado en pacientes con LAM, fue significativamente diferente en el grupo tratado con Rapamune (-88,0 ± 16,6 pg/mL/mes) en comparación con placebo (-2,42 ± 17,2 pg/mL/mes) con una diferencia en función del tratamiento de -86 pg/mL/mes (IC del 95%: 133, -39). La diferencia absoluta entre grupos en el cambio medio en VEGF-D durante el período de tratamiento de 12 meses fue -1017,2 o, aproximadamente 50% del VEGF-D medio en el enrolamiento.
Indicaciones.
Rapamune (sirolimus) está indicado para la profilaxis del rechazo de órganos en pacientes a partir de los 13 años de edad que reciben trasplantes renales. En los pacientes con riesgo inmunológico leve a moderado: Se recomienda utilizar Rapamune inicialmente en un esquema con CsA y corticosteroides; se suspenderá la CsA entre los dos y los cuatro meses después del trasplante (ver Dosificación). En pacientes de alto riesgo inmunológico (definidos como receptores de trasplante de raza negra y/o receptores de retrasplante renal por pérdida del aloinjerto anterior debido a razones inmunológicas y/o pacientes con alto panel de anticuerpos reactivos [PAR; nivel máximo de PAR > 80 %]), se recomienda emplear Rapamune en combinación con ciclosporina y corticoides durante el primer año después del trasplante (ver Dosificación y Estudios Clínicos). Limitaciones de uso en trasplante renal: No se ha evaluado el retiro de la ciclosporina en pacientes con rechazo agudo grado III de Banff 93 o rechazo vascular antes del retiro de la ciclosporina, pacientes dializados o con creatinina sérica > 4,5 mg/dl, pacientes de raza negra, pacientes con retrasplante renal, con multitrasplante de órganos o en pacientes con alto panel de anticuerpos reactivos (ver Estudios Clínicos). En pacientes de alto riesgo inmunológico: No se ha evaluado la seguridad y eficacia de estas combinaciones en pacientes de alto riesgo por un período superior a 1 año; por lo tanto, después del primer año postrasplante, se deberá considerar el ajuste al régimen inmunosupresor en base al estado clínico del paciente (ver Estudios Clínicos). En pacientes pediátricos: la seguridad y eficacia de Rapamune no ha sido establecida en pacientes < 13 años de edad, o en pacientes pediátricos ( < 18 años de edad), con trasplante renal, considerados de alto riesgo inmunológico (ver Reacciones adversas y Estudios Clínicos). La seguridad y eficacia del uso de novo de Rapamune sin ciclosporinas, no ha sido establecida en pacientes con trasplante renal (ver Advertencias). La seguridad y eficacia de los inhibidores conversores de calcineurina de Rapamune en el mantenimiento de los pacientes trasplantados, no ha sido establecida (ver Estudios Clínicos). Tratamiento de pacientes con linfangioleiomiomatosis: Rapamune (sirolimus) está indicado para el tratamiento de pacientes con linfangioleiomiomatosis (LAM).
Dosificación.
Rapamune debe administrarse únicamente por vía oral 1 vez al día, ya sea con o sin comida. Los comprimidos no deben ser triturados, masticados o partidos. En pacientes que no puedan tomar los comprimidos, deberá recetarse la solución instruyéndolos en el modo de administración. Guía para posología general en pacientes con trasplante renal: La dosis inicial de Rapamune debe administrarse tan pronto como sea posible después del trasplante. Se recomienda que se tome Rapamune 4 horas después de la administración de la solución oral y/o cápsulas de ciclosporina (ver Interacciones). Los ajustes frecuentes de dosis de Rapamune basados en concentraciones de sirolimus no estacionarias pueden conducir a una sobredosis o una subdosificación porque el sirolimus tiene una semivida larga. Una vez ajustada la dosis de mantenimiento de Rapamune, los pacientes deben continuar con la nueva dosis de mantenimiento durante al menos 7 a 14 días antes de un ajuste posológico adicional con monitorización de la concentración. En la mayoría de los pacientes, los ajustes de la dosis pueden basarse en una proporción simple: nueva dosis de Rapamune = dosis actual x (concentración objetivo/ concentración actual). Se debe considerar una dosis de carga además de una nueva dosis de mantenimiento cuando sea necesario aumentar las concentraciones mínimas de sirolimus: dosis de carga de Rapamune = 3 x (nueva dosis de mantenimiento - dosis de mantenimiento actual). La dosis máxima de Rapamune administrada en cualquier día no debe exceder de 40 mg. Si una dosis diaria estimada supera los 40 mg a causa de la adición de una dosis de carga, la dosis de carga debe administrarse durante 2 días. Las concentraciones mínimas de sirolimus deben ser monitoreadas al menos 3 a 4 días después de una(s) dosis de carga. Dos miligramos (2 mg) de Rapamune Solución Oral han demostrado ser clínicamente equivalentes a 2 mg de Rapamune Comprimidos; por consiguiente, estas dos formulaciones son intercambiables. Sin embargo, no se ha demostrado si dosis más altas de Rapamune Solución Oral son clínicamente equivalentes a dosis más altas de Rapamune Comprimidos sobre la base de mg a mg. Pacientes de riesgo inmunológico reducido a moderado: Terapia combinada de Rapamune con ciclosporinas: En pacientes con trasplante renal de novo, se recomienda administrar Rapamune Solución Oral y Comprimidos en esquemas con CsA y corticosteroides. Se deberá administrar una dosis de carga de Rapamune tres veces la dosis de mantenimiento, por ejemplo una dosis de mantenimiento diaria de 2 mg, debe ser precedida por una dosis de carga de 6 mg. Se debe llevar a cabo un monitoreo terapéutico del fármaco, para mantener la concentración de sirolimus dentro del rango de referencia (ver Dosificación). Rapamune después de la suspensión de la CsA: Entre los dos y los cuatro meses después del trasplante, la CsA se discontinuará en forma progresiva durante un período de cuatro a ocho semanas y la dosis de Rapamune se irá ajustando, hasta obtener concentraciones plasmáticas de sirolimus dentro del rango de referencia. La CsA inhibe el metabolismo y transporte del sirolimus y, consecuentemente, las concentraciones de sirolimus disminuirán a medida que se discontinúe la CsA, salvo que se aumente la dosis de Rapamune (ver Farmacología). Pacientes de alto riesgo inmunológico: En pacientes de alto riesgo inmunológico, se recomienda emplear Rapamune en combinación con ciclosporina y corticoides durante el primer año después del trasplante (ver Estudios Clínicos). No se ha evaluado la seguridad y eficacia de esta combinación por un período superior a 1 año en pacientes de alto riesgo. Por lo tanto, después del primer año postrasplante, se deberá considerar el ajuste del régimen inmunosupresor en base al estado clínico del paciente. En pacientes que reciban Rapamune con ciclosporina, el tratamiento con Rapamune deberá iniciarse con una dosis de carga de hasta 15 mg el primer día después del trasplante. A partir del día 2, deberá administrarse una dosis inicial de mantenimiento de 5 mg/día. Deberá obtenerse el nivel mínimo entre los días 5 y 7 y la dosis diaria de Rapamune debe ajustarse consecuentemente (ver Dosificación). La dosis inicial de ciclosporina debe ser de hasta 7 mg/kg/día administrada en dosis divididas y ajustándose luego para alcanzar concentraciones sanguíneas mínimas de referencia en sangre entera (ver Dosificación). La prednisona debe administrarse a una dosis mínima de 5 mg/día. Podrá emplearse tratamiento inductor de anticuerpos. Posología en pacientes con linfangioleiomiomatosis: En pacientes con linfangioleiomiomatosis, la dosis inicial de Rapamune debe ser de 2 mg/día. Las concentraciones mínimas de sirolimus en sangre entera deben medirse en 10-20 días, con ajuste de la dosis a fin de mantener las concentraciones entre 5-15 ng/mL (ver Dosificación). En la mayoría de los pacientes, los ajustes de la dosis pueden basarse en una proporción sencilla: nueva dosis de Rapamune = dosis actual x (concentración ideal/concentración actual). Los ajustes frecuentes basados en concentraciones de sirolimus en estado no estacionario pueden dar lugar a sobredosis o subdosis, debido a que el sirolimus tiene una vida media larga. Una vez que se ajusta la dosis de mantenimiento de Rapamune, los pacientes deben continuar con la nueva dosis de mantenimiento durante, al menos, 7 a 14 días antes de un nuevo ajuste de la dosis con monitorización de la concentración. Una vez que se alcance una dosis estable, se debe realizar una monitorización terapéutica, al menos cada tres meses. Monitoreo de las concentraciones sanguíneas mínimas de sirolimus: Deberán controlarse las concentraciones sanguíneas mínimas de sirolimus en todos los pacientes, especialmente en aquellos pacientes con alteraciones en el metabolismo de fármacos, en pacientes ≥ 13 años que pesen menos de 40 kg, en pacientes con disfunción hepática, cuando se realiza un cambio en la forma de dosificación de Rapamune y durante la administración concurrente de inductores e inhibidores potentes del CYP3A4 (ver Interacciones). El monitoreo de los niveles terapéuticos de la droga no debe constituir la base exclusiva para ajustar el tratamiento con sirolimus. Deberá prestarse especial atención a los signos/síntomas, biopsias de tejido y parámetros de laboratorio. Cuando se usan en combinación con ciclosporina, las concentraciones mínimas de sirolimus deben mantenerse dentro del rango de referencia (ver Estudios Clínicos y Farmacología). Después de la discontinuación de la ciclosporina en pacientes trasplantados con riesgo inmunológico bajo o moderado, las concentraciones mínimas de referencia de sirolimus deberían ser de 16 a 24 ng/mL durante el primer año después del trasplante. A partir de entonces, las concentraciones de sirolimus de referencia deben ser de 12 a 20 ng/mL. Los rangos recomendados de concentración mínima de 24 horas para sirolimus se basan en métodos cromatográficos. En la práctica clínica actual, las concentraciones sanguíneas de sirolimus se determinan por cromatografía y por inmunoensayo. Dado que las concentraciones medidas de sangre entera de sirolimus dependen del tipo de ensayo utilizado, las concentraciones obtenidas por estas diferentes metodologías no son recíprocas (ver Advertencias y Farmacología). Deberán realizarse ajustes al rango de referencia de acuerdo con el ensayo utilizado para determinar la concentración mínima de sirolimus. Dado que los resultados son analíticos y dependientes del laboratorio, y los resultados pueden cambiar con el tiempo, los ajustes al rango terapéutico deben hacerse con un conocimiento detallado del ensayo específico empleado en cada centro. Por lo tanto, la comunicación debe mantenerse con el laboratorio que realiza el ensayo. Pacientes con bajo peso corporal: La dosificación inicial en pacientes ≥ 13 años de edad que pesen menos de 40 kg deberá ajustarse en función de la superficie corporal (1 mg/m2 diarios). La dosis inicial de carga será de 3 mg/m2. Pacientes con disfunción hepática: Se recomienda reducir la dosis de mantenimiento de Rapamune en aproximadamente un tercio a un medio en pacientes con deterioro de la función hepática. Sin embargo, en estos casos, no será necesario modificar la dosis de carga de Rapamune. Pacientes con disfunción renal: En base a datos farmacocinéticos clínicos no se requiere ajuste de la dosis en pacientes con deterioro de la función renal.
Contraindicaciones.
Rapamune está contraindicado en pacientes con hipersensibilidad a sirolimus.
Reacciones adversas.
Las siguientes reacciones adversas se discuten con mayor detalle en otras secciones del prospecto: Aumento de la susceptibilidad a infecciones, linfoma y malignidades (ver Advertencias). Mortalidad excesiva, pérdida del injerto y trombosis de la arteria hepática, en pacientes con trasplante de hígado (ver Advertencias). Dehiscencia de la anastomosis bronquial en pacientes con trasplante de pulmón (ver Advertencias). Reacciones de Hipersensibilidad (ver Advertencias). Dermatitis exfoliativa (ver Advertencias). Angioedema (ver Advertencias). Cicatrización de heridas y retención hídrica (ver Advertencias). Hipertrigliceridemia, hipercolesterolemia (ver Advertencias). Deterioro de la función renal en terapias a largo plazo de Ciclosporina combinada con Rapamune (ver Advertencias). Proteinuria (ver Advertencias). Enfermedad intersticial pulmonar (ver Advertencias). Aumento del riesgo de SUH/PT/MAT inducido por inhibidores de la calcineurina: Las reacciones adversas más frecuentes (≥ 30%) observadas con Rapamune en los estudios clínicos de profilaxis de rechazo de órganos en receptores de trasplante renal son: edema periférico, hipertrigliceridemia, hipertensión, hipercolesterolemia, aumento de creatinina, estreñimiento, dolor abdominal, diarrea, infección del tracto urinario, anemia, náuseas, artralgia, dolor y trombocitopenia. Las reacciones adversas más frecuentes (≥ 20%) observadas con Rapamune en los estudios clínicos para el tratamiento de la LAM son: estomatitis, diarrea, dolor abdominal, náuseas, nasofaringitis, acné, dolor torácico, edema periférico, mareos, mialgia e hipercolesterolemia. Las siguientes reacciones adversas resultaron en una tasa de discontinuación > 5% en los estudios clínicos de profilaxis de rechazo de trasplante renal: aumento de la creatinina, hipertrigliceridemia y PT. En pacientes con LAM, el 11% de los sujetos interrumpieron la terapia debido a reacciones adversas, sin una única reacción adversa que condujo a la interrupción de la terapia en más de un paciente tratado con Rapamune. Experiencia en estudios clínicos en la profilaxis del rechazo de órganos tras el trasplante renal: La seguridad y eficacia de Rapamune Solución Oral para la prevención del rechazo de órganos tras el trasplante renal se evaluaron en dos ensayos controlados aleatorios, doble ciego, multicéntricos (ver Estudios Clínicos). Los perfiles de seguridad en los dos estudios fueron similares. La incidencia de reacciones adversas en el
estudio aleatorizado, doble ciego, multicéntrico, controlado con placebo (Estudio 2), en el que 219 pacientes con trasplante renal recibieron Rapamune Solución Oral 2 mg/día, 208 recibieron Rapamune Solución Oral 5 mg/día y 124 recibieron placebo; se presenta en la Tabla a continuación. La población del estudio tenía una edad media de 46 años (rango de edad 15 a 71 años), la distribución era del 67% masculino y la composición por raza era: caucásico (78%), raza negra (11%), asiático (3%), hispanos (2%) y otras razas (5%). Todos los pacientes fueron tratados con ciclosporina y corticosteroides. Los datos (≥ 12 meses después del trasplante) presentados en la siguiente Tabla muestran las reacciones adversas que ocurrieron en al menos uno de los grupos de tratamiento con Rapamune con una incidencia ≥ 20%. El perfil de seguridad del comprimido no difirió del de la formulación en solución oral (ver Estudios Clínicos). En general, las reacciones adversas relacionadas con la administración de Rapamune dependían de la dosis/concentración. Aunque se demostró que una dosis diaria de mantenimiento de 5 mg, con una dosis de carga de 15 mg, era segura y efectiva, no se pudo establecer una ventaja de eficacia sobre la dosis de 2 mg para los pacientes con trasplante renal. Los pacientes que recibieron 2 mg de Rapamune Solución Oral por día demostraron un mejor perfil de seguridad global que los pacientes que recibieron 5 mg de Rapamune Solución Oral por día. Debido a que los estudios clínicos se realizan bajo condiciones muy diversas, las tasas de reacción adversa observadas en un estudio clínico de un fármaco no pueden compararse directamente con las tasas en los estudios clínicos del mismo o de otro fármaco y pueden no reflejar las tasas observadas en la práctica.
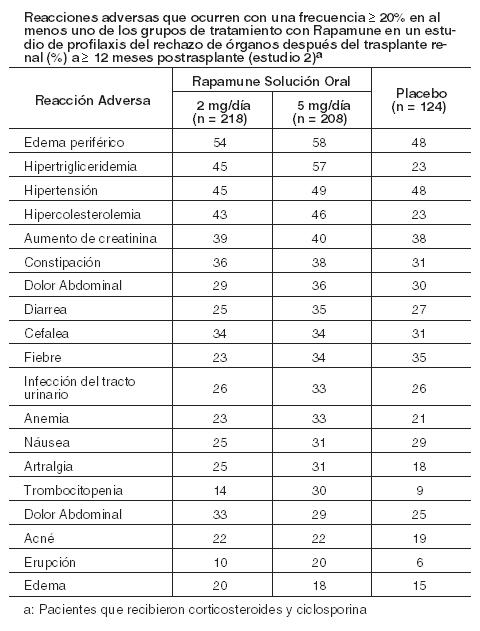
Las siguientes reacciones adversas se notificaron con menos frecuencia (≥ 3%, pero < 20%): General: Sepsis, linfocele, Herpes zóster, Herpes simplex. Cardiovascular: Tromboembolismo venoso (incluyendo embolia pulmonar, trombosis venosa profunda), taquicardia. Sistema digestivo: Estomatitis. Sistema hematológico y linfático: Trombocitopenia trombótica. Metabolismo/nutrición: Cicatrización anormal, aumento de la dehidrogenasa láctica, hipopotasemia, diabetes mellitus. Sistema músculo-esquelético: Necrosis del hueso. Sistema respiratorio: Neumonía, epistaxis. Piel: Melanoma, carcinoma de células escamosas, carcinoma de células basales. Sistema urogenital: Pielonefritis, deterioro de la función renal (aumento de creatinina) en terapias a largo plazo de Ciclosporina combinada con Rapamune (ver Advertencias), quistes ováricos, trastornos menstruales (incluyendo amenorrea y menorragia). Con menos frecuencia ( < 3%) ocurrieron las siguientes reacciones adversas: linfoma/trastorno linfoproliferativo postrasplante, infecciones micobacterianas (incluyendo M. tuberculosis), pancreatitis, citomegalovirus (CMV) y virus de Epstein-Barr. Aumento del colesterol sérico y los triglicéridos: El uso de Rapamune en pacientes con trasplante renal se asoció con un aumento del colesterol sérico y triglicéridos que pueden requerir tratamiento. En los Estudios 1 y 2, en pacientes con trasplante renal de novo, que iniciaron el estudio con colesterol sérico total < 200 mg/dl o triglicéridos séricos totales < 200 mg/dl con ayuno, hubo un aumento de la incidencia de hipercolesterolemia (colesterol en ayunas > 240 mg/dL) o hipertrigliceridemia (triglicéridos sérico en ayunas > 500 mg/dL), respectivamente, en pacientes que recibieron Rapamune 2 mg y Rapamune 5 mg en comparación con los controles de azatioprina y placebo. El tratamiento de la hipercolesterolemia de nueva aparición con agentes hipolipemiantes, fue necesario en el 42- 52% de los pacientes incluidos en los grupos de Rapamune de los Estudios 1 y 2, en comparación con el 16% de los pacientes del grupo placebo y el 22% de los pacientes del grupo de azatioprina. En otros estudios de trasplante renal con Rapamune, hasta el 90% de los pacientes requirieron tratamiento para hiperlipidemia e hipercolesterolemia con terapia hipolipemiante (ej. estatinas, fibratos). A pesar del manejo hipolipemiante, hasta el 50% de los pacientes tenían niveles séricos de colesterol en ayunas > 240 mg/dl y triglicéridos por encima de los niveles recomendados (ver Advertencias). Cicatrización anormal: Los eventos de cicatrización anormal después de la cirugía de trasplante incluyen dehiscencia fascial, hernia incisional y disrupción de anastomosis (ej. herida, vascular, vía aérea, ureteral, biliar). Malignidades: La siguiente Tabla resume la incidencia de neoplasias malignas en los dos ensayos controlados (Estudios 1 y 2) para la prevención del rechazo agudo (ver Estudios Clínicos). A los 24 meses (Estudio 1) y 36 meses (Estudio 2) postrasplante, no hubo diferencias significativas entre los grupos de tratamiento.
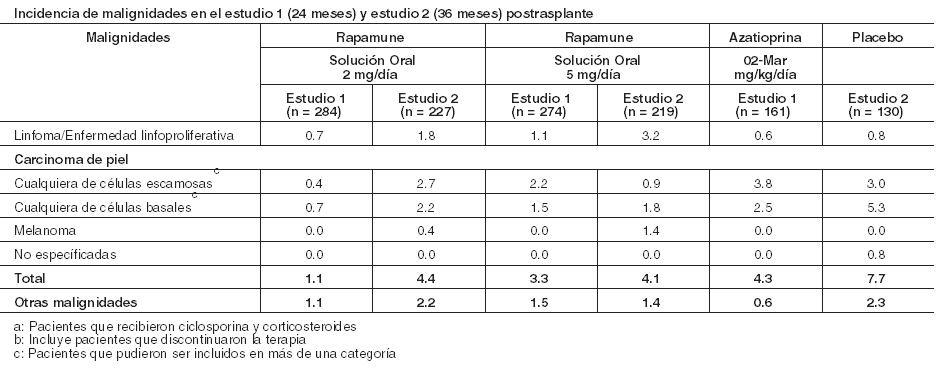
Rapamune luego de la discontinuación de ciclosporina: La incidencia de reacciones adversas se determinó a través de un ensayo aleatorizado, multicéntrico, controlado (Estudio 3) a 36 meses, en el que 215 pacientes con trasplante renal recibieron Rapamune con un régimen de mantenimiento después de la discontinuación de la ciclosporina y 215 pacientes recibieron Rapamune con ciclosporina (ver Estudios Clínicos). Todos los pacientes fueron tratados con corticosteroides. El perfil de seguridad antes de la aleatorización (comienzo de la discontinuación de la ciclosporina) fue similar al de los grupos de Rapamune de 2 mg en los Estudios 1 y 2. Después de la aleatorización (a los 3 meses), los pacientes que habían discontinuado la ciclosporina de su terapia, experimentaron mayores incidencias de las siguientes reacciones adversas: pruebas anormales de la función hepática (incluyendo aumento de AST/SGOT y aumento de ALT/SGPT), hipopotasemia, trombocitopenia y cicatrización anormal. Por el contrario, la incidencia de los siguientes eventos adversos fue mayor en pacientes que permanecieron con ciclosporina que aquellos que habían discontinuado la ciclosporina del tratamiento: hipertensión, toxicidad por ciclosporina, aumento de creatinina, función renal anormal, nefropatía tóxica, edema, hiperpotasemia, hiperuricemia e hiperplasia de las encías. La presión arterial sistólica y diastólica media mejoró significativamente después de la discontinuación de la ciclosporina. Malignidades: La incidencia de malignidades en el Estudio 3 (ver Estudios Clínicos) se presenta en la siguiente Tabla. En el Estudio 3, la incidencia de linfoma/enfermedad linfoproliferativa fue similar en todos los grupos de tratamiento. La incidencia global de malignidad fue mayor en los pacientes que recibieron Rapamune más ciclosporina en comparación con los pacientes que habían discontinuado la ciclosporina. No se pudo sacar conclusiones sobre estas diferencias en la incidencia de malignidades, porque el Estudio 3 no fue diseñado para considerar los factores de riesgo de malignidad o para la búsqueda sistemática de malignidades en sujetos. Además, más pacientes en el grupo de Rapamune con ciclosporina, tuvieron antecedentes de carcinoma de piel.
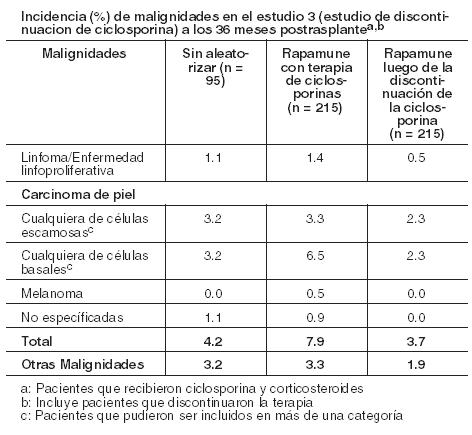
Pacientes con trasplante del alto riesgo inmunológico: La seguridad se evaluó en 224 pacientes que recibieron al menos una dosis de sirolimus con ciclosporina (ver Estudios Clínicos). En general, la incidencia y la naturaleza de las reacciones adversas fueron similares a las observadas en estudios anteriores de combinación con Rapamune. La incidencia de malignidad fue del 1,3% a los 12 meses. Conversión desde los Inhibidores de Calcineurina a Rapamune en el mantenimiento de la población con trasplante renal: No se ha establecido la seguridad y la eficacia de la conversión desde los inhibidores de la calcineurina a Rapamune en el mantenimiento de la población con trasplante renal (ver Estudios Clínicos). En un estudio que evaluó la seguridad y la eficacia de la conversión desde los inhibidores de la calcineurina a Rapamune (concentraciones iniciales de sirolimus de referencia de 12-20 ng/mL y luego de 8-20 ng/mL, por ensayo cromatográfico) en pacientes en mantenimiento de trasplante renal, se detuvo la inscripción en el subgrupo de pacientes (n = 87) con una tasa de filtración glomerular basal menor a 40 mL/min. Hubo una mayor tasa de eventos adversos graves, incluyendo neumonía, rechazo agudo, pérdida de injerto y muerte, en este estrato del grupo de tratamiento con Rapamune. El subgrupo de pacientes con una tasa de filtración glomerular basal menor a 40 mL/min, tuvo 2 años de seguimiento después de la aleatorización. En esta población, la tasa de neumonía fue del 25,9% (15/58) frente al 13,8% (4/29), la pérdida del injerto (excluyendo la muerte con pérdida funcional del injerto) fue del 22,4% (13/58) frente al 31,0% (9/29) y la muerte fue del 15,5% (9/58) frente al 3,4% (1/29) en el grupo de conversión a sirolimus y en el grupo de continuación de ICN, respectivamente. En el subgrupo de pacientes con una tasa de filtración glomerular basal mayor a 40 mL/min, no hubo beneficio asociado con la conversión, con respecto a la mejora de la función renal y una mayor incidencia de proteinuria en el grupo de conversión a Rapamune. En general, en este estudio, se observó un aumento de 5 veces, en los informes de tuberculosis entre los grupos de tratamiento con sirolimus 2,0% (11/551) y el comparador 0,4% (1/273) con un esquema de asignación al azar 2:1. Pacientes pediátricos con trasplante renal: La seguridad se evaluó en un estudio clínico controlado en pacientes pediátricos con trasplante renal ( < 18 años de edad) considerados de alto riesgo inmunológico, definido como historia de uno o más episodios de rechazo agudo de aloinjerto y/o presencia de nefropatía crónica de aloinjerto en una biopsia renal (ver Estudios Clínicos). El uso de Rapamune en combinación con inhibidores de la calcineurina y corticosteroides se asoció con una mayor incidencia del deterioro de la función renal (aumento de la creatinina) en comparación con la terapia basada en inhibidores de la calcineurina, anomalías de los lípidos en el suero (incluyendo pero no limitado a triglicéridos séricos y colesterol), e infecciones del tracto urinario. Pacientes con Linfangioleiomiomatosis: Se evaluó la seguridad en un estudio controlado en que se inscribió a 89 pacientes con linfangioleiomiomatosis, 46 de los cuales recibieron tratamiento con Rapamune (ver Estudios clínicos). Las reacciones medicamentosas adversas observadas en este estudio concordaron con el perfil de seguridad respecto de pacientes con trasplante renal que recibieron Rapamune, con la incorporación de la disminución de peso que se informó con una mayor incidencia con Rapamune en comparación con el placebo. Las reacciones adversas que se produjeron con una frecuencia ≥ 20% en el grupo tratamiento con Rapamune, y mayor que con placebo incluyeron estomatitis, diarrea, dolor abdominal, náuseas, nasofaringitis, acné, dolor torácico, edema periférico, infección de las vías respiratorias altas, cefalea, mareos, mialgia e hipercolesterolemia. Experiencia post-marketing: Las siguientes reacciones adversas se han identificado durante el uso posterior a la aprobación de Rapamune en pacientes con trasplante. Debido a que estas reacciones se informan voluntariamente en una población de tamaño incierto, no siempre es posible estimar con fiabilidad su frecuencia o establecer una relación causal con la exposición al fármaco. General: linfedema. Cardiovascular: Efusión del pericardio (incluyendo efusiones hemodinámicas significativas y taponamientos, que requirieron intervención en niños y adultos) y acumulación de fluidos. Sistema digestivo: Ascitis. Sistema hematológico y linfático: Pancitopenia, neutropenia. Trastornos hepatobiliares: Hepatotoxicidad, incluyendo necrosis hepática fatal, con concentraciones mínimas elevadas de sirolimus. Sistema inmune: Reacciones de hipersensibilidad, incluyendo reacciones anafilácticas/anafilactoideas, angioedema y vasculitis hipersensible (ver Advertencias). Infecciones: Tuberculosis. Se ha observado nefropatía asociada al virus BK en pacientes que recibieron inmunosupresores, incluyendo Rapamune. Esta infección puede estar asociada con resultados graves, incluyendo el deterioro de la función renal y la pérdida del injerto renal. Se han notificado casos de leucoencefalopatía multifocal progresiva (LMP), a veces fatal, en pacientes tratados con inmunosupresores, incluyendo Rapamune (ver Advertencias). Enterocolitis por Clostridium difficile. Metabolismo/nutrición: Pruebas hepáticas anormales, aumento de AST/SGOT, aumento de ALT/SGPT, hipofosfatemia, hiperglicemia, diabetes mellitus. Sistema Nervioso: Síndrome de encefalopatía posterior reversible. Respiratorio: Se han producido casos de enfermedad pulmonar intersticial (incluyendo neumonitis, bronquiolitis obliterante con neumonía organizante y fibrosis pulmonar), algunos fatales, sin etiología infecciosa identificada en pacientes que recibieron regímenes inmunosupresores incluyendo Rapamune. En algunos casos, la enfermedad intersticial pulmonar se ha resuelto al suspender o reducir la dosis de Rapamune. El riesgo puede aumentar a medida que aumenta la concentración mínima de sirolimus (ver Advertencias); hemorragia pulmonar; derrame pleural; proteinosis alveolar. Piel: Carcinoma de piel neuroendócrino (carcinoma de células de Merkel), dermatitis exfoliativa (ver Advertencias). Urogenital: Síndrome nefrótico, proteinuria, glomeruloesclerosis segmentaria focal, quistes ováricos, trastornos menstruales (incluyendo amenorrea y menorragia). Azoospermia se ha informado con el uso de Rapamune y ha sido reversible en la interrupción de Rapamune en la mayoría de los casos.
Advertencias.
Advertencia especial: el uso de inmunosupresores no se recomienda en pacientes con trasplante de hígado o pulmón. La inmunosupresión puede dar como resultado un aumento de la susceptibilidad a las infecciones y un posible desarrollo de linfoma u otras malignidades. La inmunosupresión puede tener como resultado el aumento de la susceptibilidad a las infecciones y el posible desarrollo de linfomas. Sólo podrán prescribir Rapamune aquellos médicos que posean experiencia en tratamientos inmunosupresores y manejo de pacientes con trasplante renal. Los pacientes que reciban este fármaco deben ser tratados en instituciones que cuenten con recursos de equipo, personal de laboratorio y apoyo médico adecuados. El médico responsable del tratamiento de mantenimiento deberá contar con la información completa requerida para el seguimiento del paciente. La seguridad y eficacia de Rapamune (sirolimus) como terapia inmunosupresora no ha sido establecida en pacientes con trasplante de hígado o pulmón, por lo tanto no se recomienda su uso. Trasplante de hígado - Mortalidad excesiva, pérdida del injerto y Trombosis hepática arterial (TAH): El uso de Rapamune en combinación con tacrolimus se asoció con mortalidad excesiva y pérdida del injerto en un estudio en pacientes de trasplante de hígado de novo. Muchos de estos pacientes tenían evidencia de infección o estaban en estado terminal. En el estudio anterior y en otro estudio de trasplante de hígado de novo, el uso de Rapamune en combinación con ciclosporina o tacrolimus, se asoció a un aumento del TAH; la mayoría de los casos de TAH ocurrieron 30 días post-trasplante y la mayoría concluyó con pérdida del injerto y muerte. Trasplante de pulmón - Dehiscencia de la anastomosis bronquial: Se han reportado casos, la mayoría fatales, de dehiscencia de la anastomosis bronquial, en trasplantes de pulmón de novo, cuando se utilizó Rapamune, como parte de una terapia inmunosupresiva. Linfoma: La inmunosupresión puede resultar en una mayor susceptibilidad a las infecciones y en el posible desarrollo de linfomas y otras enfermedades malignas, particularmente enfermedades de la piel. Las tasas de linfoma/enfermedad linfoproliferativa observadas en los Estudios 1 y 2 fueron 0,7-3,2% (para los pacientes tratados con Rapamune) versus 0,6-0,8% (azatioprina y placebo) (ver Reacciones adversas). La sobreinmunosupresión también puede aumentar la susceptibilidad a las infecciones, incluso a la aparición de infecciones oportunistas, infecciones fatales y sepsis. Sólo deberán utilizar Rapamune aquellos médicos con experiencia en inmunosupresión y en el tratamiento de pacientes con trasplantes de órganos. Los pacientes que reciban esta droga deberán ser tratados en instituciones que cuenten con equipos, personal de laboratorio y apoyo médico adecuados. El médico responsable del tratamiento de mantenimiento deberá poseer un profundo conocimiento del producto, necesario para el adecuado control del paciente. Trasplante de hígado - Mayor mortalidad, Pérdida del injerto y Trombosis Arterial Hepática: La seguridad y la eficacia de Rapamune como terapia inmunosupresora no se han establecido en los pacientes con trasplante de hígado; por lo tanto, tal uso no se recomienda. El uso de Rapamune se ha asociado con resultados adversos en pacientes luego de un trasplante de hígado, incluyendo exceso de mortalidad, pérdida de injerto y trombosis de la arteria hepática (TAH). En un estudio en receptores de trasplante de hígado de novo se asoció la administración de Rapamune en combinación con tacrolimus con mayor mortalidad y pérdida del injerto. Muchos de estos pacientes presentaban infección en el momento o poco antes del deceso. En éste y otro estudio en receptores de trasplante hepático de novo se asoció la combinación de Rapamune y CsA o tacrolimus con una mayor incidencia de trombosis arterial hepática (7% en combinación versus 2% en el grupo control); la mayoría de los casos se produjo en los 30 días posteriores al trasplante y la mayoría derivó en pérdida del injerto o fallecimiento. Un estudio clínico en pacientes con trasplante hepático aleatorizados a la conversión a un régimen con sirolimus versus continuación de un régimen con inhibidores de la calcineurina (ICN) 6-144 meses después del trasplante de hígado demostró mayor casos de muerte en el grupo de conversión a sirolimus en comparación con el grupo de continuación de ICN, si bien la diferencia no fue estadísticamente significativa (3,8% versus 1,4%) (ver Estudios clínicos). Trasplante de Pulmón - Dehiscencia de la anastomosis bronquial: Se han comunicado casos de dehiscencia de la anastomosis bronquial, la mayoría fatales, en pacientes con trasplante pulmonar de novo cuando se administró sirolimus como parte de un régimen inmunosupresor. La seguridad y eficacia de Rapamune como terapia inmunosupresora no se han establecido en pacientes de trasplante de pulmón; por lo tanto, tal uso no se recomienda. Reacciones de hipersensibilidad: Las reacciones de hipersensibilidad, entre ellas las reacciones anafilácticas/anafilactoides, angioedema, dermatitis exfoliativa y vasculitis de hipersensibilidad se han visto asociadas a la administración de sirolimus (ver Reacciones adversas). Angioedema: Rapamune se ha asociado con el desarrollo de angioedema. El uso concomitante de Rapamune con otros fármacos que se sabe causan angioedema, como los inhibidores de la enzima convertidora de angiotensina (ECA), puede aumentar el riesgo de desarrollar angioedema. Los niveles elevados de sirolimus (con o sin inhibidores de la ECA concomitantes) también pueden potenciar el angioedema (ver Interacciones). En algunos casos, el angioedema se ha resuelto al suspender o reducir la dosis de Rapamune. Cicatrización de heridas y retención hídrica: Se ha informado de cicatrización retardada o deficiente en pacientes que recibieron Rapamune, incluido linfocele y dehiscencia de la herida (ver Reacciones adversas). Los inhibidores de mTOR tales como sirolimus han demostrado in vitro inhibición de la producción de ciertos factores de crecimiento que pueden afectar a la angiogénesis, la proliferación de fibroblastos y la permeabilidad vascular. El linfocele, una complicación quirúrgica conocida del trasplante renal, se ha registrado con una frecuencia significativamente mayor y en relación con la dosis administrada en pacientes tratados con Rapamune (ver Reacciones adversas). En consecuencia, deberán considerarse las medidas adecuadas para minimizar esta complicación. De acuerdo con la literatura médica, los pacientes con IMC superior a 30 kg/m2 pueden presentar mayor riesgo de cicatrización anormal de la herida. Asimismo se ha informado de acumulación de líquido, tales como edema periférico, linfedema, derrame pleural y derrames pericárdicos (que incluyeron derrames hemodinámicamente significativos en niños y adultos), en pacientes que recibieron Rapamune. Hiperlipidemia: El aumento del colesterol sérico y de los triglicéridos que requieren tratamiento se produjo con mayor frecuencia en los pacientes tratados con Rapamune en comparación con los controles de azatioprina o placebo en los estudios 1 y 2 (ver Reacciones adversas). Hubo una mayor incidencia de hipercolesterolemia (43-46%) y/o hipertrigliceridemia (45-57%) en los pacientes que recibieron Rapamune en comparación con los controles con placebo (cada uno 23%). El riesgo/beneficio debe ser cuidadosamente considerado en pacientes con hiperlipidemia establecida antes de iniciar un régimen inmunosupresor incluyendo Rapamune. Cualquier paciente que se administre Rapamune debe ser monitorizado para la hiperlipidemia. Si se detecta, deben iniciarse intervenciones como la dieta, el ejercicio y los agentes hipolipemiantes, como se indica en las directrices del Programa Nacional de Educación del Colesterol. En ensayos clínicos de pacientes que recibieron Rapamune más ciclosporina o Rapamune después de la suspensión de la ciclosporina, hasta el 90% de los pacientes requirieron tratamiento para hiperlipidemia e hipercolesterolemia con terapia hipolipemiante (por ejemplo, estatinas, fibratos). A pesar del tratamiento hipolipemiante, hasta el 50% de los pacientes tenían niveles de colesterol sérico en ayunas > 240 mg/dl y triglicéridos por encima de los niveles recomendados. La administración concomitante de Rapamune e inhibidores de la HMG-CoA reductasa resultó en reacciones adversas como elevaciones de CPK (3%), mialgia (6,7%) y rabdomiólisis ( < 1%). En estos ensayos, el número de pacientes era demasiado pequeño y la duración del seguimiento era demasiado corta para evaluar el impacto a largo plazo de Rapamune sobre la mortalidad cardiovascular. Deterioro de la función renal: La función renal debe monitorearse estrechamente durante la coadministración de Rapamune con ciclosporina, ya que la administración a largo plazo de esta combinación se ha asociado con el deterioro de la función renal. En los pacientes tratados con CsA y Rapamune, se observaron niveles de creatinina sérica más altos e índices de filtración glomerular más bajos, que los registrados en los pacientes tratados con CsA y placebo o CsA y azatioprina. El índice de deterioro de la función renal en estos estudios fue superior en el grupo de pacientes que recibían Rapamune y CsA, en comparación con los grupos que recibían el tratamiento control (Estudios 1 y 2). Por lo tanto, se deberá controlar la función renal y considerar ajustes adecuados del régimen inmunosupresor, incluyendo medidas como discontinuación de Rapamune y/o ciclosporinas y/o tacrolimus, en pacientes con niveles elevados de creatinina sérica. En pacientes con riesgo inmunológico leve a moderado, la continuación de la terapia de combinación con ciclosporina más allá de los 4 meses después del trasplante sólo debe considerarse cuando los beneficios superan los riesgos de esta combinación para los pacientes individuales. Se debe tener cuidado al usar agentes (por ejemplo, aminoglucósidos y anfotericina B) que se sabe que tienen un efecto de deterioro sobre la función renal. En pacientes con retraso en la función del injerto, Rapamune puede retrasar la recuperación de la función renal. Proteinuria: Se recomiendan controles periódicos cuantitativos de la excreción urinaria de proteínas. En un estudio que evaluó la conversión de inhibidores de la calcineurina (ICN) a Rapamune en pacientes con trasplante renal en mantenimiento 6 - 120 meses después del trasplante, se observó mayor excreción urinaria de proteínas por lo regular entre los 6 y 24 meses después de la conversión a Rapamune en comparación con la continuación de ICN (ver Reacciones adversas y Estudios clínicos). Los pacientes en el cuartil más elevado de excreción urinaria de proteínas antes de la conversión a Rapamune fueron aquellos con mayor aumento de excreción proteica después de la conversión. En el 2,2 % de los pacientes del grupo de conversión a Rapamune versus el 0,4% del grupo de pacientes con continuación de ICN se comunicó nefrosis de reciente comienzo (síndrome nefrótico). También se informó proteinuria de rango nefrótico (definida como proporción de proteína urinaria a creatinina > 3,5) en el 9,2% en el grupo de pacientes de conversión a Rapamune en comparación con el 3,7% en el grupo de pacientes con continuación de CNI. Se observó una reducción del grado de excreción urinaria de proteínas en casos individuales después de suspender Rapamune. No se ha establecido la seguridad y eficacia de la conversión de inhibidores de la calcineurina a sirolimus en pacientes con trasplante renal en mantenimiento. Infecciones virales latentes: Los pacientes tratados con inmunosupresores, incluido Rapamune, presentan mayor riesgo de desarrollar infecciones oportunistas, así como también activación de infecciones virales latentes. Entre estas infecciones se encuentran la nefropatía asociada al virus BK, que se ha observado en pacientes con trasplante renal que reciben inmunosupresores, incluyendo Rapamune. Esta infección puede estar asociada con resultados graves, como el deterioro de la función renal y la pérdida del injerto (ver Reacciones adversas). La monitorización del paciente puede ayudar a detectar riesgo de nefropatía asociada al virus BK. Se debe considerar la reducción de la inmunosupresión en los pacientes que desarrollan evidencia de nefropatía asociada al virus BK. Se han reportado casos de leucoencefalopatía multifocal progresiva (PML) en pacientes que reciben inmunosupresores, incluyendo Rapamune. PML se presenta comúnmente con hemiparesia, apatía, confusión, deficiencias cognitivas y ataxia. Los factores de riesgo para la PML incluyen el tratamiento con terapias inmunosupresoras y el deterioro de la función inmune. En los pacientes inmunosuprimidos, los médicos deben considerar la PML en el diagnóstico diferencial en pacientes que informan de síntomas neurológicos y la consulta con un neurólogo debe considerarse como clínicamente indicado. Se debe considerar la posibilidad de reducir la cantidad de inmunosupresión en pacientes que desarrollan PML. En los pacientes con trasplante, los médicos también deben considerar el riesgo para el injerto, de reducción de la inmunosupresión. Enfermedad pulmonar intersticial: Se han producido casos de enfermedad pulmonar intersticial (neumonitis, bronquiolitis obliterante con neumonía organizante y fibrosis pulmonar), en algunos casos fatales, sin etiología infecciosa identificada en pacientes que recibieron regímenes inmunosupresores incluyendo Rapamune. En algunos casos, la enfermedad intersticial pulmonar se informó con hipertensión pulmonar (incluida la hipertensión arterial pulmonar) como un evento secundario. En algunos casos, la enfermedad intersticial pulmonar se ha resuelto tras la interrupción o reducción de la dosis de Rapamune. El riesgo puede incrementarse a medida que aumenta la concentración de sirolimus (ver Reacciones adversas). Uso de novo sin Ciclosporinas: La seguridad y la eficacia del uso de novo de Rapamune sin ciclosporina no están establecidas en pacientes con trasplante renal. En un estudio clínico multicéntrico, los pacientes con trasplante renal de novo tratados con Rapamune, micofenolato mofetilo (MMF), esteroides y un antagonista del receptor de IL-2, tuvieron tasas de rechazo agudo significativamente más altas y tasas de mortalidad numéricamente más altas en comparación con los pacientes tratados con ciclosporina, esteroides y antagonistas del receptor de IL-2. Un beneficio, en términos de mejor función renal, no fue evidente en el grupo de tratamiento con el uso de novo de Rapamune sin ciclosporina. Estos hallazgos también se observaron en un grupo de tratamiento similar de otro ensayo clínico. Síndrome urémico hemolítico/púrpura trombocitopénica trombótica/microangiopatía trombótica, inducidos por inhibidores de la calcineurina: La administración concomitante de sirolimus y un inhibidor de la calcineurina puede aumentar el riesgo de síndrome urémico hemolítico/púrpura trombocitopénica trombótica/microangiopatía trombótica (SUH/PTT/MAT) inducidos por los inhibidores de la calcineurina (ver Reacciones adversas). Profilaxis antimicrobiana: Se han registrado casos de neumonía por Pneumocystis carinii en pacientes que no recibían profilaxis antimicrobiana. Por lo tanto, deberá administrarse antibioticoterapia preventiva frente a neumonía por Pneumocystis carinii durante un período de 1 año después del trasplante. Se recomienda efectuar un tratamiento profiláctico contra el citomegalovirus (CMV) durante los tres meses posteriores al trasplante, particularmente en aquellos pacientes que presenten un mayor riesgo de enfermedad por CMV. Diferentes concentraciones mínimas de Sirolimus reportadas entre metodologías cromatográficas e inmunoensayo: Actualmente, en la práctica clínica, las concentraciones en sangre entera de sirolimus se miden mediante diversas metodologías cromatográficas e inmunoensayos. Los valores de concentración de la muestra del paciente de diferentes ensayos pueden no ser intercambiables (ver Dosificación). Carcinomas de piel: Los pacientes con terapia inmunosupresora tienen un mayor riesgo de cáncer de piel. La exposición a la luz solar y rayos UV debe limitarse mediante el empleo de ropa protectora y una crema pantalla solar con alto factor de protección (ver Reacciones adversas). Interacción con Inhibidores Fuertes e Inductores de CYP3A4 y / o P-gp: Evite el uso concomitante de Rapamune con fuertes inhibidores de CYP3A4 y/o glicoproteína P (como ketoconazol, voriconazol, itraconazol, eritromicina, telitromicina o claritromicina) o fuertes inductores de CYP3A4 y/o glicoproteína P, como rifampina o rifabutina (ver Interacciones). Carcinogénesis, mutagénesis y deterioro de la fertilidad: Se realizaron estudios de carcinogenicidad en ratones y ratas. En un estudio con ratones hembra de 86 semanas con dosis de sirolimus 30 a 120 veces la dosis clínica diaria de 2 mg (ajustada para la superficie corporal), hubo un aumento estadísticamente significativo de linfoma maligno en todos los niveles de dosis en comparación con los controles. En un segundo estudio en ratones con dosis que fueron aproximadamente de 3 a 16 veces la dosis clínica (ajustada para la superficie corporal), se consideró relación con el sirolimus, adenomas hepatocelulares y carcinomas en machos. En el estudio con ratas de 104 semanas, con dosis iguales o inferiores a la dosis clínica de 2 mg diarios (ajustada por superficie corporal), no hubo hallazgos significativos. El sirolimus no fue genotóxico en el ensayo de mutación reversa bacteriana in vitro, en el ensayo de aberración cromosómica de células de ovario de hámster chino, en el ensayo de mutación directa de células de linfoma de ratón o en el ensayo de micronúcleo de ratón in vivo. La fertilidad disminuyó levemente en ratas machos y hembras después de la administración oral de sirolimus en dosis aproximadamente 10 o 2 veces, respectivamente, la dosis clínica de 2 mg diarios (ajustada para la superficie corporal). En ratas machos se observó atrofia de testículos, epidídimo, próstata, túbulos seminíferos y/o reducción en el recuento espermático. En ratas hembras, se observó tamaño reducido de ovarios y útero. La reducción del recuento de espermatozoides en ratas macho fue reversible al cesar la dosificación en un estudio. La degeneración tubular testicular también se observó en un estudio intravenoso de 4 semanas de sirolimus en monos a dosis que eran aproximadamente iguales a la dosis clínica (ajustada para la superficie corporal). Embarazo: Sirolimus resultó embrio/fetotóxico en ratas, con dosis aproximadamente 0,2 a 0,5 veces la dosis clínica en humanos ajustada según la superficie corporal. La toxicidad embrionaria/fetal se manifestó como mortalidad y reducción del peso fetal (con retrasos asociados en la osificación del esqueleto). Sin embargo, no se registraron evidencias de teratogénesis. En combinación con la CsA, las ratas registraron una mayor mortalidad embrionaria/fetal que con Rapamune administrado como agente único. No se registraron alteraciones en el desarrollo del conejo con una dosificación maternalmente tóxica con dosis aproximadamente 0,3 a 0,8 veces la dosis clínica ajustada según la superficie corporal. No se dispone de estudios adecuados y bien controlados en mujeres embarazadas. Deberá utilizarse un método anticonceptivo eficaz antes de iniciar el tratamiento con Rapamune, durante el tratamiento y hasta 12 semanas después de haberse interrumpido la medicación. Se prescribirá Rapamune durante el embarazo sólo en aquellos casos en que el beneficio potencial de la paciente supere el riesgo potencial del embrión/feto. Utilización durante la lactancia: El sirolimus se excreta en mínima cantidad en la leche de ratas en período de lactancia. Sin embargo, no se sabe si el sirolimus se excreta en la leche humana. Se desconocen los perfiles farmacocinético y de seguridad del sirolimus en lactantes. Dado que son muchas las drogas que se excretan en la leche humana y dada la posibilidad de que se produzcan reacciones adversas secundarias al sirolimus en lactantes alimentados al pecho materno, deberá tomarse la decisión de interrumpir la alimentación al pecho o de interrumpir el tratamiento, teniendo en cuenta la importancia que éste pudiera tener para la madre. Utilización en Pediatría: Trasplante renal: No se ha establecido la seguridad y la eficacia de Rapamune en pacientes por debajo de los 13 años de edad. Se ha evaluado la seguridad y eficacia de Rapamune Solución oral y Rapamune Comprimidos en niños de 13 años o mayores considerados de riesgo inmunológico reducido a moderado. El empleo de Rapamune Solución oral y Rapamune Comprimidos en esta subpoblación de niños de 13 años o mayores se encuentra avalado por los resultados de estudios clínicos adecuados y bien controlados con Rapamune Solución oral en adultos y datos farmacocinéticos adicionales en receptores pediátricos de trasplante renal. La información de seguridad y eficacia de un estudio clínico controlado en receptores pediátricos y adolescentes ( < 18 años) de trasplante renal considerados de alto riesgo inmunológico, determinado por antecedentes de uno o más episodios de rechazo agudo y/o por la presencia de nefropatía crónica por aloinjerto, no avalan el uso crónico de Rapamune Solución oral o comprimidos en combinación con inhibidores de la calcineurina y corticosteroides, debido al mayor riesgo de anormalidades lipídicas y deterioro de la función renal asociado con estos regímenes inmunosupresores, sin mayores beneficios con respecto al rechazo agudo, sobrevida del injerto o del paciente. Linfangioleiomiomatosis: La seguridad y eficacia de Rapamune en pacientes pediátricos < 18 años de edad no ha sido establecida. Utilización en Geriatría: Los estudios clínicos con Rapamune Solución Oral o Rapamune Comprimidos Recubiertos no incluyeron un número suficiente de pacientes mayores de 65 años o más como para determinar si la seguridad y la eficacia en esta población difieren respecto de la eficacia y la seguridad en pacientes más jóvenes. La información respecto de las concentraciones basales de sirolimus indican que no es necesario realizar ajustes en la dosificación, en función de la edad, en pacientes geriátricos con trasplante renal. En general, la selección de dosis para un paciente de edad avanzada debe ser prudente, normalmente comenzando en el extremo inferior del rango de dosificación, lo que refleja la mayor frecuencia de disminución de la función hepática o cardiaca y de la enfermedad concomitante u otro tratamiento farmacológico. Pacientes con disfunción hepática: La dosis de mantenimiento de Rapamune debe ser reducida en pacientes con disfunción hepática (ver Dosificación). Pacientes con disfunción renal: No se requiere ajuste de la dosis en pacientes con disfunción renal (ver Dosificación).
Interacciones.
Se sabe que el sirolimus constituye un sustrato adecuado, tanto para el citocromo CYP3A4, como para la glucoproteína P. Más abajo se detallan las interacciones farmacocinéticas que pueden producirse entre el sirolimus y los medicamentos que se administren en forma concomitante. Sólo se han realizado estudios de interacción entre drogas con los medicamentos que se describen más abajo. Ciclosporina: Se demostró que la ciclosporina, un sustrato e inhibidor de CYP3A4 y de la glicoproteína P, aumentaba las concentraciones de sirolimus cuando se administraba con este mismo. Para disminuir el efecto de esta interacción con la ciclosporina, se recomienda tomar Rapamune 4 horas después de la administración de la solución oral y/o cápsulas de ciclosporina. Si se suspende la ciclosporina de la terapia combinada con Rapamune, se necesitan dosis más elevadas de Rapamune para mantener los rangos de concentración recomendados de sirolimus (ver Dosificación y Farmacología). Inductores e inhibidores potentes de la CYP3A4 y la glicoproteína P: Evite el uso concomitante de sirolimus con inductores potentes (ej., Rifampina, rifabutina) e inhibidores potentes (ej. ketoconazol, voriconazol, itraconazol, eritromicina, telitromicina, claritromicina) de CYP3A4 y glicoproteína P. Se deben considerar agentes alternativos con menor potencial de interacción con sirolimus (ver Advertencias y Farmacología). Jugo de pomelo: Debido a que el jugo de pomelo inhibe el metabolismo del sirolimus mediado por CYP3A4, no debe tomarse ni utilizarse para la dilución de Rapamune (ver Dosificación, Interacciones y Farmacología). Inductores débiles y moderados o inhibidores de CYP3A4 y glicoproteína P: Tenga precaución al usar sirolimus con fármacos o agentes que son moduladores de CYP3A4 y glicoproteína P. Se puede necesitar un ajuste en la dosis de Rapamune y/o del fármaco coadministrado (ver Farmacología). Fármacos que aumentan la concentración de sirolimus: Bromocriptina, cimetidina, cisaprida, clotrimazol, danazol, diltiazem, fluconazol, inhibidores de proteasa (por ejemplo, VIH y hepatitis C que incluyen fármacos como ritonavir, indinavir, boceprevir y telaprevir), metoclopramida, nicardipina, troleandomicina, verapamilo. Fármacos u otros agentes que puede disminuir la concentración de sirolimus: Carbamazepina, fenobarbital, fenitoína, rifapentina, hierba de San Juan (Hypericum perforatum). Fármacos cuya concentración pueda ser aumentada cuando se utiliza Rapamune: Verapamilo. Vacunas: Los inmunosupresores pueden afectar la respuesta a la vacunación. Por lo tanto, durante el tratamiento con Rapamune, l
a vacunación puede ser menos eficaz. Debe evitarse el uso de vacunas vivas; las vacunas vivas pueden incluir, pero no se limitan a las siguientes: sarampión, paperas, rubéola, polio oral, BCG, fiebre amarilla, varicela y tifoidea TY21a.
Conservación.
Conservar en heladera entre 2°C y 8°C. No congelar. Proteger de la luz.
Sobredosificación.
La experiencia existente con sobredosificación es limitada. En términos generales, los efectos adversos de la sobredosis guardan relación con los que se detallan en la sección Reacciones adversas (ver Reacciones adversas). En todos los casos de sobredosis, se tomarán las medidas de apoyo habituales. Sobre la base de la limitada solubilidad en líquidos y la alta capacidad de unión a las proteínas plasmáticas y a los eritrocitos que tiene Rapamune, es posible deducir que Rapamune no responderá a la diálisis en grado significativo. En ratones y ratas, la dosis letal aguda por vía oral fue superior a los 800 mg/kg. Ante la eventualidad de una sobredosificación, concurrir al Hospital más cercano o comunicarse con alguno de los Centros de Toxicología del país. Entre otros: Hospital de Pediatría Ricardo Gutiérrez: Tel. (011) 4962-6666/2247. Hospital A. Posadas: Tel. (011) 4654-6648/4658-7777. Hospital de Pediatría "Dr. Garrahan": (011) 4943-1455. Información para los pacientes: Los pacientes deben recibir instrucciones completas sobre la dosificación. Deberá informarse a las mujeres potencialmente fértiles respecto de los riesgos que pueden producirse durante el embarazo y deberá indicárseles la necesidad de utilizar medidas anticonceptivas eficaces antes de iniciar un tratamiento con Rapamune, durante el tratamiento y hasta 12 semanas después de haber interrumpido el tratamiento. Será necesario informar a los pacientes que deberán limitar la exposición al sol y a los rayos UV, usando ropa que los proteja y utilizando pantallas protectoras con alto factor de protección, dado el mayor riesgo de padecer cáncer de piel.
Presentación.
Estuche conteniendo 1 frasco con 60 ml de solución oral, 30 jeringas dosificadoras, 1 adaptador para la jeringa, 1 estuche de viaje.
Revisión.
Abril-2018. LPD: 06/SEP/16.
Laboratorio que comercializa Rapamune
PFIZER →

