MabThera® s.c.
ROCHE
Rituximab.
Agente antineoplásico, anticuerpo monoclonal.
Composición.
Cada vial de 15 ml contiene 1.400 mg de rituximab en una solución de 11,7 ml (120 mg/ml). Excipientes: hialuronidasa humana recombinante (rHuPH20) 2.000 U/ml, L-histidina y clorhidrato de L-histidina monohidrato 20 mM, a, a-trehalosa, dihidrato 210 mM, L-metionina 10 mM, polisorbato 80: 0,06% (p/v) y volumen total ajustado con agua para preparaciones inyectables (WFI) c.s.
Farmacología.
Código ATC: L01XC02. Grupo farmacoterapéutico: Agentes antineoplásicos - Anticuerpos monoclonales. Propiedades farmacodinámicas: Mecanismo de acción: MabThera formulación subcutánea contiene hialuronidasa humana recombinante (rHuPH20), una enzima que se utiliza para incrementar la dispersión y la absorción de sustancias concomitantes, al administrarlas por vía subcutánea. Rituximab es un anticuerpo monoclonal quimérico murino/humano que se une específicamente al antígeno CD20, una fosfoproteína transmembranaria no-glucosilada, expresada en los linfocitos pre-B y B maduros. El antígeno se expresa en más del 95% de todos los linfomas no-Hodgkin (LNH) de células B. CD20 se expresa tanto en células B normales como en tumorales, pero no en células madre hematopoyéticas, células pro-B, células plasmáticas normales ni en otros tejidos normales. Este antígeno no se internaliza tras la unión del anticuerpo ni se elimina de la superficie celular. CD20 no circula en el plasma como antígeno libre y, por esta razón, no compite por la unión con los anticuerpos. El dominio Fab de rituximab se une al antígeno CD20 en la superficie de los linfocitos B, mientras que el dominio Fc puede incorporar efectores de la respuesta inmune para mediar la lisis de las células B. Los mecanismos posibles de la lisis celular mediada por efector incluyen la citotoxicidad dependiente del complemento (CDC), como resultado de la unión de Clq y la citotoxicidad celular dependiente de anticuerpos (ADCC) mediada por uno o más receptores Fcc de la superficie de los granulocitos, macrófagos y células NK (natural killer). También se ha demostrado que la unión de rituximab al antígeno CD20 de los linfocitos B induce la muerte celular por apoptosis. Después de completarse la administración de la primera dosis de MabThera, los recuentos de células B periféricas disminuyeron por debajo de lo normal. En los pacientes tratados de neoplasias hematológicas, la recuperación de células B comenzó a los 6 meses de tratamiento y en general, los niveles normales se lograron en 12 meses después de finalizado el mismo, aunque en algunos pacientes se requirió un lapso más prolongado (hasta un tiempo medio de recuperación de 23 meses después de la terapia de inducción). En pacientes con artritis reumatoidea, se observa una depleción inmediata de células B en sangre periférica después de las dos infusiones de 1.000 mg de MabThera separadas por un intervalo de 14 días. El recuento de células B en sangre periférica empieza a aumentar desde la semana 24 y la evidencia de repoblación se observa, en la mayoría de los pacientes, en la semana 40, independientemente de que MabThera se administre en monoterapia o en combinación con metotrexato. En los pacientes con granulomatosis con poliangeítis (GP) y poliangeítis microscópica (PM), las células B de sangre periférica CD19 se redujeron a menos de 10 células/ml después de las dos primeras infusiones de rituximab y se mantuvieron en ese nivel en la mayoría de los pacientes durante 6 meses. Experiencia clínica de MabThera formulación subcutánea en Linfoma No-Hodgkin: La experiencia clínica de MabThera formulación subcutánea en Linfoma No-Hodgkin se basa en los datos recolectados en un estudio clínico Fase III (SABRINA BO22334) en pacientes con Linfoma Folicular (LF) y otro Fase Ib de búsqueda/confirmación de dosis (SparkThera BP22333) en pacientes con LF. En Propiedades farmacocinéticas se presentan los resultados de este último estudio. Estudio BO22334 (SABRINA): Se realizó un estudio Fase III, de dos etapas, internacional, multicéntrico, aleatorizado, controlado, abierto, en pacientes con linfoma folicular sin tratamiento previo, para investigar la no inferioridad del perfil farmacocinético, junto con la eficacia y la seguridad, de MabThera formulación subcutánea en combinación con CHOP o CVP, comparado con MabThera formulación intravenosa en asociación con CHOP o CVP. El objetivo de la primera etapa consistió en establecer la dosis subcutánea de rituximab que alcanzó niveles séricos de la Cvalle con la formulación subcutánea de MabThera similares a los de MabThera formulación intravenosa, al administrarlo como parte de un tratamiento de inducción cada 3 semanas (ver Farmacología, Propiedades farmacocinéticas). En la etapa 1 se incorporaron pacientes sin tratamiento previo (n=127) y con Linfoma Folicular (LF) CD20 positivo, Grados 1, 2 o 3a. El objetivo de la etapa 2 fue proveer información de seguridad y eficacia adicional para rituximab subcutáneo en comparación con rituximab IV utilizando la dosis subcutánea de 1.400 mg establecida en la etapa 1. En la etapa 2 se incorporaron pacientes sin tratamiento previo (n=283) y con Linfoma Folicular (LF) CD20 positivo, Grados 1, 2 o 3. El diseño global del ensayo fue idéntico entre ambas etapas y los pacientes fueron aleatorizados a uno de los dos grupos de tratamiento: MabThera formulación subcutánea (n=205): primer ciclo con MabThera formulación intravenosa más 7 ciclos de MabThera formulación subcutánea en combinación con hasta 8 ciclos de quimioterapia CHOP o CVP, administrado cada 3 semanas. MabThera formulación intravenosa fue administrado con la dosis estándar de 375 mg/m2 del área de superficie corporal. MabThera formulación subcutánea fue administrado con una dosis fija de 1.400 mg. Los pacientes que alcanzaron al menos una respuesta parcial (RP) recibieron la terapia de mantenimiento con MabThera formulación subcutánea administrado una vez cada 8 semanas durante 24 meses. MabThera formulación intravenosa (n=205): 8 ciclos de MabThera formulación intravenosa en combinación con hasta 8 ciclos de quimioterapia CHOP o CVP, administrado cada 3 semanas. MabThera formulación intravenosa fue administrado con la dosis estándar de 375 mg/m2 del área de superficie corporal. Los pacientes que alcanzaron al menos una respuesta parcial recibieron la terapia de mantenimiento con MabThera formulación intravenosa administrado una vez cada 8 semanas durante 24 meses. En el análisis combinado de 410 pacientes las estimaciones puntuales de tasas de respuesta global fueron 84,4% (IC del 95%: 78,7; 89,1) y 83,4% (IC del 95%: 77,6; 88,2) en los grupos MabThera IV y SC, respectivamente. Las estimaciones puntuales de tasa de respuesta completa fueron 31,7% (IC del 95%: 25,4; 38,6) y 32,7% (IC del 95%: 26,3; 39,6) en los grupos MabThera IV y SC, respectivamente. Los análisis exploratorios mostraron que las tasas de respuesta entre los subgrupos ASC, quimioterapia y sexo no fueron notablemente diferentes de la población con intención de tratar. Las estimaciones globales puntuales de la tasa de respuesta para el análisis combinado de 410 pacientes en SABRINA etapas 1 y 2 se muestran en la Tabla 1.
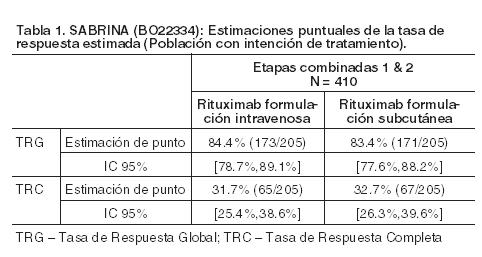
Los análisis exploratorios mostraron que las tasas de respuesta entre los subgrupos BSA, quimioterapia y sexo no fueron notablemente diferentes de la población ITT. Inmunogenicidad: Los datos del programa de desarrollo de la formulación subcutánea de MabThera indican que la formación de anticuerpos contra rituximab (HACAs) luego de la administración subcutánea es similar a la observada luego de la aplicación intravenosa. En el ensayo SABRINA (BO22334) la incidencia de anticuerpos anti-rituximab potenciados/inducidos por el tratamiento en el grupo subcutáneo fue baja y similar a la observada en el grupo IV (2% frente a 1%, respectivamente). La incidencia de anticuerpos anti-rHuPH20 potenciados/inducidos por el tratamiento fue del 6% en el grupo IV en comparación con el 9% en el grupo subcutáneo, y ninguno de los pacientes con resultado positivo para los anticuerpos anti-rHuPH20 dio positivo para anticuerpos neutralizantes. No hubo impacto aparente de la presencia de anticuerpos anti-rituximab o anti-rHuPH20 sobre la seguridad y eficacia. En el estudio SAWYER (BO25341), en pacientes con Leucemia Linfocítica Crónica con la formulación subcutánea de MabThera 1.600 mg, la incidencia de los anticuerpos anti-rituximab inducidos/incrementados por el tratamiento fue similar en los dos grupos de tratamiento; 6,7% IV vs. 2,4% SC. La incidencia de los anticuerpos anti rHuPH20 inducidos/incrementados por el tratamiento sólo se midió en pacientes en el grupo SC y fue 10,6%. Ninguno de los pacientes con resultado positivo para anticuerpos anti rHuPH20 fue positivo para anticuerpos neutralizantes. La proporción general de pacientes con anticuerpos contra rHuPH20 se mantuvo constante en general durante el período de seguimiento en ambas cohortes. Se desconoce la relevancia clínica del desarrollo de HACAs o anticuerpos contra rHuPH20 después del tratamiento con MabThera formulación subcutánea. No hubo impacto aparente de la presencia de anticuerpos anti-rituximab o anti-rHuPH20 sobre la seguridad o la eficacia [SABRINA]. Experiencia clínica de MabThera concentrado para solución para infusión intravenosa en Linfoma No-Hodgkin: Linfoma folicular: Tratamiento inicial en combinación con quimioterapia: En un ensayo abierto, aleatorizado, un total de 322 pacientes con linfoma folicular no tratados previamente recibieron quimioterapia CVP (ciclofosfamida: 750 mg/m2; vincristina: 1,4 mg/m2 hasta un máximo de 2 mg el día 1, y prednisolona: 40 mg/m2/día desde el día 1 hasta el día 5) cada 3 semanas, durante 8 ciclos, o bien MabThera (375 mg/m2) en combinación con CVP (R-CVP). MabThera fue administrado el primer día de cada ciclo de tratamiento. Se determinó la eficacia terapéutica en 321 pacientes tratados (162 del grupo R-CVP y 159 del grupo CVP). La mediana de la duración del seguimiento de los pacientes fue de 53 meses. El grupo que recibió R-CVP obtuvo un beneficio significativo sobre el tratado con CVP en lo que respecta a la variable principal de eficacia, el tiempo hasta el fracaso del tratamiento (TFT) (27 meses comparado con 6,6 meses; p < 0,0001; log rank test). La proporción de pacientes con respuesta antitumoral (RC, respuesta completa no confirmada RCnc, RP) fue significativamente superior (p < 0,0001 test Chi-cuadrado) en el grupo R-CVP (80,9%) que en el grupo CVP (57,2%). El tratamiento con R-CVP prolongó significativamente el tiempo hasta progresión de la enfermedad o fallecimiento en comparación con CVP, 33,6 meses y 14,7 meses, respectivamente (p < 0,0001; log rank test). La mediana de duración de la respuesta fue de 37,7 meses en el grupo R-CVP y de 13,5 meses en el grupo CVP (p < 0,0001; log rank test). La diferencia entre los grupos de tratamiento con respecto a la sobrevida global fue clínicamente significativa (p = 0,029; log rank test estratificado por centros): la tasa de sobrevida a los 53 meses fue del 80,9% para pacientes del grupo R-CVP comparada con el 71,1% para los del grupo CVP. Los resultados de otros tres ensayos aleatorizados en los que se utilizó MabThera en combinación con un régimen de quimioterapia distinto de CVP (CHOP, MCP, CHVP/interferón alfa) han demostrado también mejorías significativas en las tasas de respuesta, en parámetros dependientes del tiempo, así como en sobrevida global. La Tabla 2 resume los resultados clave de los cuatro ensayos.

Terapia de mantenimiento: Linfoma folicular previamente no tratado: En un ensayo de Fase III, prospectivo, abierto, internacional y multicéntrico, a 1.193 pacientes con linfoma folicular avanzado no tratados previamente se les administró terapia de inducción con R-CHOP (n = 881); R-CVP (n = 268) o R-FCM (n = 44) a criterio del Investigador. Un total de 1.078 respondió a la terapia de inducción, de los cuales 1.018 fueron aleatorizados a mantenimiento con MabThera (n = 505) u observación (n = 513). Los dos grupos estuvieron bien equilibrados en cuanto a las características basales y el estado de la enfermedad. El tratamiento consistió en una infusión de 375 mg/m2 de superficie corporal de MabThera administrada cada 2 meses hasta progresión de la enfermedad o durante un período máximo de 2 años. Después de una mediana de tiempo de observación de 25 meses desde la aleatorización, la terapia de mantenimiento con MabThera arrojó resultados clínicamente relevantes y estadísticamente significativos en la variable principal sobrevida libre de progresión (SLP) evaluada por el Investigador, comparado con los pacientes en observación con linfoma folicular previamente no tratados (Tabla 3). Esta mejora en la SLP fue confirmado por un Comité independiente de revisión (CIR) (Tabla 3). También se observó beneficio significativo del mantenimiento con MabThera en las variables secundarias sobrevida libre de evento (SLE), tiempo hasta nuevo tratamiento de linfoma, (TNTL), tiempo hasta nuevo tratamiento de quimioterapia (TNTQ) y tasa de respuestas global (TRG) (Tabla 3). Los resultados del análisis primario se confirmaron con un lapso de seguimiento más prolongado (mediana de tiempo de observación: 73 meses desde la distribución al azar).
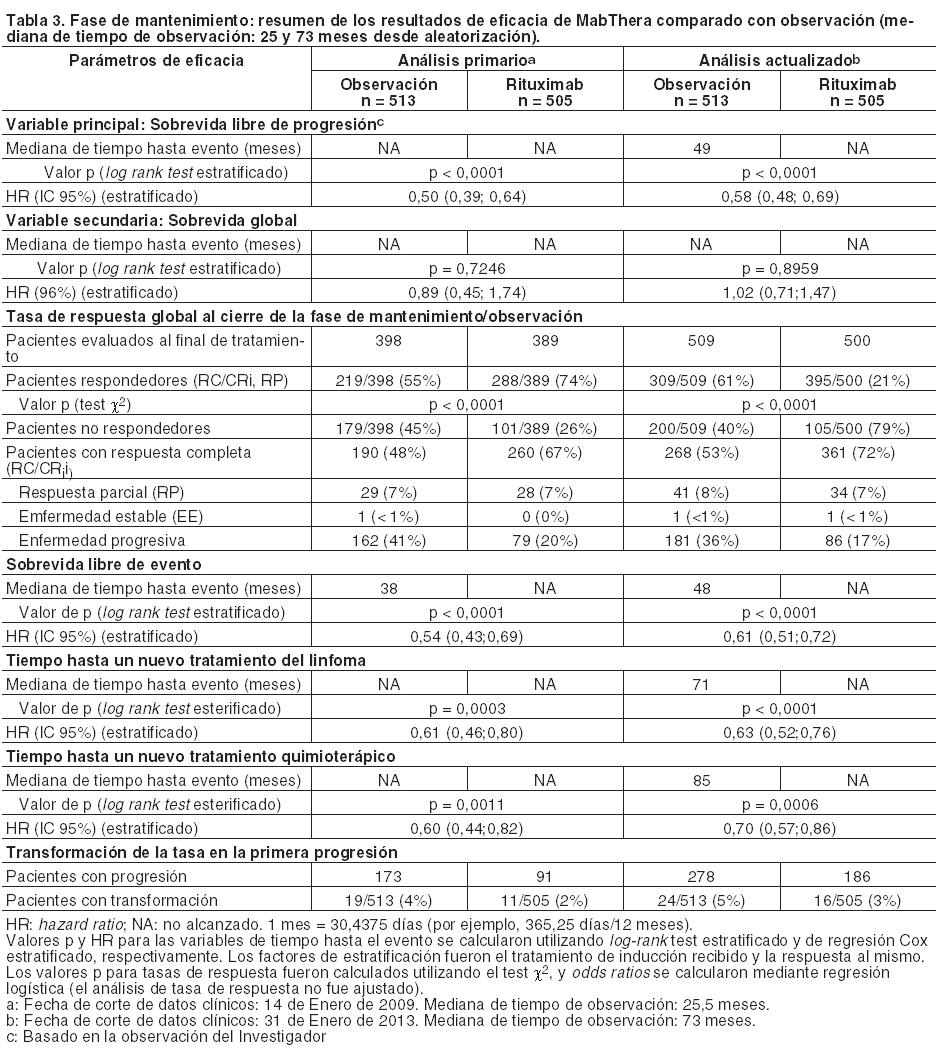
El tratamiento de mantenimiento con MabThera ha supuesto un beneficio en todos los subgrupos predefinidos evaluados: sexo (hombre, mujer), edad ( < 60 años, ≥ 60 años), escala FLIPI (≤ 1,2 ó ≥ 3), terapia de inducción (R-CHOP, R-CVP, R-FCM), y sin tener en cuenta la calidad de la respuesta a la inducción (CRi, RC o RP). Análisis exploratorios sobre el beneficio del tratamiento de mantenimiento, mostraron un efecto menos pronunciado en pacientes de edad avanzada ( > 70 años); sin embargo, los tamaños de muestra fueron pequeños. Linfoma folicular en recaída o refractario: En un ensayo de Fase III, prospectivo, abierto, internacional y multicéntrico, en la primera fase se distribuyeron aleatoriamente, 465 pacientes con linfoma folicular en recidiva o refractario para recibir un tratamiento de inducción con CHOP (ciclofosfamida, doxorrubicina, vincristina, prednisona; n = 231) o bien MabThera más CHOP (R-CHOP, n = 234). Ambos grupos se hallaban bien equilibrados en cuanto a características basales y el estado de la enfermedad. En la segunda fase los 334 pacientes que habían logrado una remisión parcial o completa luego de la terapia de inducción fueron distribuidos aleatoriamente, para recibir mantenimiento con MabThera (n = 167) u observación (n = 167). La terapia de mantenimiento con MabThera consistió en una infusión única de 375 mg/m2 de superficie corporal, administrada cada tres meses durante un período máximo de dos años o hasta la progresión de la enfermedad. El análisis de eficacia final incluyó a todos los pacientes distribuidos al azar en ambas fases del ensayo. Después de una mediana de tiempo de observación de 31 meses, el resultado de aquéllos con linfoma folicular en recidiva o refractario incluidos en la fase de inducción, con R-CHOP mejoró significativamente comparado con CHOP (Tabla 4).
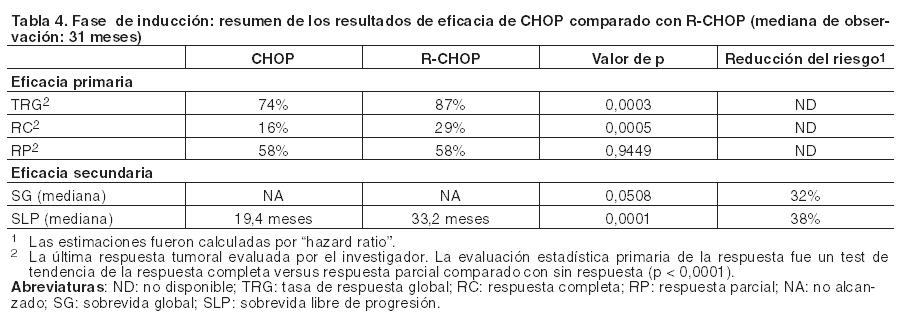
Para los pacientes aleatorizados en la fase de mantenimiento del estudio, la mediana de observación fue 28 meses desde la distribución al azar. El mantenimiento con MabThera condujo a una mejoría significativa y clínicamente relevante de la variable principal de eficacia, la sobrevida libre de progresión o SLP (tiempo desde la aleatorización al tratamiento de mantenimiento hasta la recidiva, la progresión de la enfermedad o el fallecimiento) en comparación con los pacientes en observación (p < 0,0001, log rank test). La mediana de la SLP fue de 42,2 meses en el grupo de mantenimiento con MabThera en comparación con los 14,3 meses del grupo en observación. El análisis de regresión de Cox indicó que el mantenimiento con MabThera redujo el riesgo de progresión de la enfermedad o fallecimiento en 61% en comparación con el grupo en observación (IC95%: 45% - 72%). Según una estimación de las curvas de Kaplan-Meier, la sobrevida libre de eventos a los 12 meses fue de 78% para la terapia de mantenimiento con MabThera comparado con 57% en el grupo en observación. Un análisis de la sobrevida global confirmó el beneficio significativo del tratamiento de mantenimiento con MabThera comparado con observación (p = 0,0039, log rank test), dado que el primero redujo el riesgo de muerte en un 56% (IC95%: 22% - 75%). La mediana del tiempo transcurrido hasta un nuevo tratamiento del linfoma fue significativamente más prolongada con la terapia de mantenimiento con MabThera que con el grupo en observación (38,8 meses comparado con 20,1 meses, p < 0,0001, log rank test). El riesgo de comenzar un nuevo tratamiento se redujo en 50% (IC95%: 30% - 64%). En pacientes que lograron una respuesta completa/respuesta completa no confirmada, como la mejor respuesta durante el tratamiento de inducción, el mantenimiento con MabThera prolongó significativamente la mediana de la sobrevida libre de enfermedad comparada con el grupo en observación (53,7 versus 16,5 meses, p = 0,0003, log rank test) (Tabla 5). El riesgo de recaída en los pacientes con respuesta completa disminuyó en un 67% (IC95%: 39% - 82%).

El mantenimiento con MabThera prolongó en forma significativa la mediana de la SLP en los pacientes respondedores a la terapia de inducción con CHOP (mediana de SLP: 37,5 meses comparado con 11,6 meses, p < 0,0001) y también en aquellos respondedores a la terapia de inducción con R-CHOP (mediana de SLP: 51,9 meses comparado con 22,1 meses, p = 0,0071). Si bien los subgrupos fueron reducidos, el mantenimiento con MabThera proporcionó un beneficio significativo respecto de la sobrevida global tanto en los pacientes respondedores a CHOP como para aquellos respondedores a R-CHOP; aunque se necesita un seguimiento más prolongado para confirmar estos hallazgos. La terapia de mantenimiento con MabThera proporcionó beneficios consistentes en todos los subgrupos testeados: sexo, edad (≤ 60 años, > 60 años), estadios (III, IV), estados de desempeño de la OMS (0 versus > 0), síntomas B (ausente, presente), afectación de la médula ósea (no versus sí), Índice de Pronóstico Internacional [IPI] (0 - 2 versus 3 - 5), Índice Pronóstico Internacional de Linfoma Folicular [FLIPI] (0 - 1, versus 2 versus 3 - 5), número de sitios extranodales (0 - 1 versus > 1), número de sitios nodales ( < 5 versus ≥ 5), número de regímenes previos (1 versus 2), mejor respuesta al tratamiento previo (respuesta completa/respuesta parcial versus NC/PD), hemoglobina ( < 12 g/dl versus ≥ 12 g/dl), microglobulina b2 ( < 3 mg/l versus ≥ 3 mg/l), LDH (elevado, no elevado), excepto para el pequeño grupo de pacientes con enfermedad voluminosa o bulky. Linfoma No-Hodgkin difuso de células B grandes: En un ensayo abierto, aleatorizado, un total de 399 pacientes de edad avanzada previamente no tratados (edad entre 60 y 80 años) que padecían linfoma difuso de células B grandes recibieron quimioterapia CHOP estándar (750 mg/m2 de ciclofosfamida, 50 mg/m2 de doxorrubicina, 1,4 mg/m2 de vincristina hasta un máximo de 2 g el día 1 y 40 mg/m2/día de prednisolona en los días 1 a 5), cada 3 semanas, durante 8 ciclos, o bien MabThera (375 mg/m2) más CHOP (R-CHOP). MabThera se administró el primer día de cada ciclo de tratamiento. El análisis final de eficacia incluyó todos los pacientes aleatorizados (197 CHOP, 202 R-CHOP) y comprendió una mediana de seguimiento de aproximadamente 31 meses. Ambos grupos estuvieron bien equilibrados en cuanto a las características basales y el estado de la enfermedad. El análisis final confirmó que el tratamiento con R-CHOP estaba asociado con una mejoría clínicamente relevante y estadísticamente significativa en la duración de la sobrevida libre de eventos (variable principal de eficacia, donde los eventos fueron fallecimiento, recidiva o progresión del linfoma o inicio de un nuevo tratamiento anti-linfoma) (p = 0,0001). La estimación de la duración media de la sobrevida libre de eventos fue de 35 meses según las curvas de Kaplan-Meier en el grupo tratado con R-CHOP en comparación con 13 meses en el grupo con CHOP, lo cual representa una reducción del riesgo del 41%. Al cabo de 24 meses, la estimación de la sobrevida global fue de 68,2% en el grupo con R-CHOP en comparación con 57,4% en el grupo con CHOP. Un análisis posterior de la duración de la sobrevida global, durante un período de seguimiento de 60 meses de mediana, confirmó el beneficio del tratamiento de R-CHOP respecto del CHOP (p = 0,0071), equivalente a una disminución del riesgo del 32%. El análisis de todas las variables secundarias (índice de respuesta, sobrevida libre de progresión, sobrevida libre de enfermedad, duración de la respuesta) confirmó la ventaja terapéutica de R-CHOP respecto del régimen CHOP. El índice de respuestas completas después del octavo ciclo de tratamiento fue de 76,2% en el grupo con R-CHOP y de 62,4% en el grupo con CHOP (p = 0,0028). El riesgo de progresión de la enfermedad disminuyó en un 46% y el de recidiva en un 51%. En todos los subgrupos de pacientes (sexo, edad, Índice de Pronóstico Internacional [IPI] ajustado por edad, estadio Ann Arbor, ECOG, microglobulina-b2, LDH, albúmina, síntomas B, carga tumoral elevada, enfermedad extranodular, compromiso de la médula ósea), las relaciones de riesgo para la sobrevida libre de eventos y la sobrevida global, (R-CHOP comparado con CHOP) fueron menos de 0,83 y 0,95, respectivamente. R-CHOP se asoció con mejoría en el resultado del tratamiento tanto de pacientes de alto como de bajo riesgo, de acuerdo con IPI ajustado por edad. Alteraciones de laboratorio: No se apreciaron respuestas en los 67 pacientes en los que se evaluó el anticuerpo antimurino humano HAMA. De 356 pacientes en los que se estimó el HACA, el 1,1% fueron positivos (4 pacientes). Población pediátrica: La Agencia Europea de Medicamentos ha eximido al titular de la obligación de presentar los resultados de los ensayos realizados con MabThera en los diferentes grupos de la población pediátrica en Linfoma Folicular (ver Dosificación, Población pediátrica). Propiedades farmacocinéticas: Absorción: En pacientes con linfoma folicular se compararon las farmacocinéticas de rituximab luego de la administración de una dosis única de 375 mg/m2, 625 mg/m2 y 800 mg/m2 de MabThera formulación subcutánea con 375 mg/m2 de MabThera formulación intravenosa. La absorción de rituximab es lenta, alcanzando las concentraciones máximas aproximadamente 3 días después de la administración subcutánea. Se estimó una biodisponibilidad absoluta de 71% (95% IC: 70,0 - 72,1) sobre la base de un análisis farmacocinético poblacional. La exposición a rituximab se incrementó sobre el rango de la dosis subcutánea proporcional de 375 mg/m2 a 800 mg/m2. Los parámetros farmacocinéticos tales como, clearance, volumen de distribución y vida media de eliminación fueron comparables para ambas formulaciones. Estudio BP22333 (SparkThera): Se ha realizado un estudio Fase Ib, de dos etapas, para investigar la farmacocinética, la seguridad y la tolerabilidad de la formulación subcutánea de MabThera en pacientes con Linfoma Folicular (LF) como parte de un tratamiento de mantenimiento. En la segunda etapa se administró la formulación subcutánea de MabThera con una dosis fija de 1.400 mg como inyección subcutánea durante el tratamiento de mantenimiento, luego de al menos un ciclo de la formulación intravenosa de MabThera a pacientes con linfoma folicular que presentaron respuesta previa a la misma en la inducción. La comparación de los datos estimados de la mediana de la Cmáx para MabThera formulación subcutánea y formulación intravenosa se resume en la Tabla 6.

La mediana del Tmáx en la formulación subcutánea de MabThera fue de aproximadamente 3 días, en comparación con el Tmáx que ocurrió al final o próximo a la terminación de la infusión intravenosa. Estudio BO22334 (SABRINA): MabThera formulación subcutánea se administró con una dosis fija de 1.400 mg durante 6 ciclos por vía subcutánea durante la inducción en intervalos de 3 semanas, luego del primer ciclo de MabThera formulación intravenosa, en pacientes con linfoma folicular sin tratamiento previo, en combinación con quimioterapia. Los niveles séricos de la Cmáx de rituximab en el ciclo 7 fueron similares entre los dos grupos de tratamiento, con valores de la media geométrica (CV%) de 250,63 (19,01) mg/ml y 236,82 (29,41) mg/ml para las formulaciones intravenosa (i.v.) y subcutánea (s.c.), respectivamente, con la proporción consecuente de la media geométrica (Cmáx, s.c./Cmáx, i.v.) de 0,941 (IC 90%: 0,872, 1,015). Distribución/Eliminación: Los valores estimados de la media geométrica de Cvalle y ABCt de los estudios BP22333 y BO22334 se resumen en la Tabla 7.

En un análisis farmacocinético poblacional en 403 pacientes con linfoma folicular que recibieron MabThera subcutáneo y/o intravenoso, infusiones únicas o múltiples de MabThera como agente único o en combinación con quimioterapia, las estimaciones de la población para el clearance no específico (CL1), el clearance específico inicial (CL2), posiblemente inducido por los linfocitos B o la carga tumoral, y el volumen de distribución del compartimiento central (V1) fueron 0,194 l/día, 0,535 l/día y 4,37 l/día, respectivamente. La mediana calculada de vida media de eliminación terminal de MabThera formulación subcutánea fue de 29,7 días (rango, 9,9 a 91,2 días). El conjunto de datos de análisis contenía 6.003 muestras cuantificables de 403 pacientes que recibieron rituximab subcutáneo y/o intravenoso en los estudios BP22333 (3.736 muestras de 277 pacientes) y BO22334 (2.267 muestras de 126 pacientes). El peso y el área de superficie corporal media (rango) fueron de 74,4 kg (43,9 a 130 kg) y 1,83 m2 (1,34 a 2,48 m2), respectivamente. La edad media (rango) fue 57,4 años (23 a 87 años). No hubo diferencias entre los parámetros demográficos y de laboratorio de los dos estudios. Sin embargo, 29 muestras (0,48%) observadas después de la dosis, todas del ensayo BP22333, estaban por debajo del límite de cuantificación, ya que los pacientes en el estudio BP22333 entraron al mismo después de haber recibido un mínimo de cuatro ciclos de MabThera IV en la inducción y al menos un ciclo de mantenimiento con MabThera IV, mientras que los del Estudio BO22334 no habían sido tratados con MabThera antes de su incorporación en el estudio. No hubo valores faltantes de covariables, excepto el recuento de células B basal. La carga tumoral basal sólo estaba disponible en el estudio BO22334. Poblaciones especiales: En el estudio BO22334 se observó un efecto entre la proporción del tamaño corporal y la exposición reportada en el ciclo 7, entre 1.400 mg de rituximab formulación subcutánea administrado cada 3 semanas y 375 mg/m2 de rituximab formulación intravenosa administrado cada 3 semanas con proporciones de Cvalle de 2,29, 1,31 y 1,41 en los pacientes con área de la superficie corporal (ASC) baja, media y alta, respectivamente (ASC baja ≤ 1,70 m2; 1,70 m2 < ASC media < 1,90 m2; ASC alta ≥ 1,90 m2). Las proporciones correspondientes de ABCt fueron 1,66, 1,17 y 1,32. No se registró evidencia de dependencia clínicamente relevante de la farmacocinética de rituximab sobre la edad y el sexo. Se detectaron anticuerpos anti-rituximab en sólo 13 pacientes y no resultaron en un incremento clínicamente significativo en el clearance en estado estacionario. Datos preclínicos sobre seguridad: Se ha demostrado que rituximab posee una alta especificidad para el antígeno CD20 de las células B. Durante los ensayos de toxicidad en monos cinomolgos no se observó ningún otro efecto además de la depleción de células B en la sangre periférica y en el tejido linfático, previsible por el mecanismo farmacológico. Se han realizado estudios de toxicidad en el desarrollo en monos cinomolgos que recibieron dosis de hasta 100 mg/kg (tratamiento desde el día 20 hasta el día 50 de la gestación); no se apreciaron evidencias de toxicidad fetal debidas a rituximab. No obstante, se observó, en forma dosis-dependiente y mediada por el mecanismo farmacológico, una depleción de células B en los órganos linfáticos de los fetos, que persistió después del nacimiento y se acompañó de una disminución de los niveles de IgG de los animales recién nacidos afectados. El recuento de células B de estos animales se normalizó en los 6 primeros meses de vida y no afectó negativamente a la reacción a la vacunación. No se han llevado a cabo pruebas estándares para investigar la mutagenicidad, ya que éstas no son relevantes en el caso concreto de esta molécula. No se han realizado estudios a largo plazo en animales para establecer el potencial carcinogénico de rituximab. No se han efectuado estudios específicos para determinar los efectos de rituximab o rHuPH20 sobre la fertilidad. En general, no se observaron efectos nocivos en los órganos reproductores de machos o hembras en los estudios de toxicidad en monos cinomolgos. Adicionalmente, no se demostraron efectos de rHuPH20 sobre la calidad del semen. En estudios de desarrollo embriofetal en ratones, rHuPH20 produce reducción del peso fetal y pérdida de implantaciones a exposiciones sistémicas suficientemente superiores a la exposición terapéutica humana. No existe evidencia de dismorfogénesis (es decir, teratogénesis) derivada de la exposición sistémica a rHuPH20.
Indicaciones.
MabThera 1400 mg formulación subcutánea está indicado en pacientes adultos con Linfoma No-Hodgkin (LNH): MabThera está indicado en combinación con quimioterapia en el tratamiento de pacientes con Linfoma folicular estadios III-IV que no hayan sido tratados previamente. MabThera está indicado en el tratamiento de mantenimiento de pacientes con linfoma folicular que hayan respondido a la terapia de inducción. MabThera está indicado en combinación con quimioterapia CHOP (ciclofosfamida, doxorrubicina, vincristina, prednisolona) en el tratamiento de pacientes con Linfoma No-Hodgkin difuso de células B grandes CD20 positivas.
Dosificación.
El reemplazo por cualquier otro agente biológico requiere el consentimiento del médico prescriptor. La formulación subcutánea de MabThera debe ser administrada bajo la estrecha supervisión de un médico experto y en un entorno que disponga en forma inmediata de un equipo completo de reanimación (véase Precauciones). Antes de cada administración de MabThera, siempre se debe suministrar premedicación consistente en un antipirético y un antihistamínico, por ejemplo paracetamol y difenhidramina. Se debe considerar la premedicación con glucocorticoides si MabThera no se va a administrar en combinación con quimioterapia que los incluya para el tratamiento del Linfoma No-Hodgkin. MabThera SC 1.400 mg es para uso en linfoma no Hodgkin (LNH) solamente. Posología: La dosis recomendada de MabThera formulación subcutánea utilizada en pacientes adultos es una inyección subcutánea con una dosis fija de 1.400 mg, independientemente del área de superficie corporal del paciente. Antes de comenzar con las inyecciones subcutáneas de MabThera, todos los pacientes deben recibir siempre previamente, una dosis completa de MabThera por infusión intravenosa, utilizando MabThera formulación intravenosa (véase Precauciones). Por lo tanto, el cambio a MabThera formulación subcutánea sólo puede ocurrir en el segundo ciclo o en los ciclos posteriores de tratamiento (véase subsecciones "Primera administración intravenosa" y "Administraciones subcutáneas subsiguientes", a continuación). Primera administración intravenosa: La primera administración de MabThera siempre debe ser dada por infusión intravenosa a una dosis de 375 mg/m2 de superficie corporal. La velocidad de infusión inicial recomendada es de 50 mg/h; posteriormente, la tasa puede escalarse en incrementos 50 mg/h cada 30 minutos hasta un máximo de 400 mg/h. Administraciones subcutáneas subsiguientes: Si los pacientes no pudieron recibir una dosis completa de la infusión intravenosa de MabThera antes del cambio, deben continuar recibiendo los ciclos posteriores con MabThera formulación intravenosa hasta que se administre correctamente una dosis intravenosa completa. En los pacientes que son capaces de recibir la dosis completa de la infusión de MabThera IV, se pueden administrar por vía subcutánea los ciclos de MabThera posteriores mediante formulación MabThera SC (véase Precauciones). La inyección de MabThera SC debe administrarse durante aproximadamente 5 minutos. Es importante verificar las etiquetas del medicamento a fin de garantizar que se está administrando al paciente la formulación (intravenosa o subcutánea) y la dosis apropiada, según la indicación clínica. La formulación subcutánea de MabThera no debe administrarse por vía intravenosa, únicamente por inyección subcutánea. Linfoma folicular No-Hodgkin: Terapia combinada: La dosis recomendada de MabThera en combinación con la quimioterapia para el tratamiento de inducción en pacientes con linfoma folicular sin tratamiento previo es: primer ciclo con MabThera formulación intravenosa 375 mg/m2 por área de superficie corporal, seguido por ciclos posteriores con MabThera formulación subcutánea inyectados con una dosis fija de 1.400 mg por ciclo, independientemente del área de superficie corporal del paciente, por un total de 8 ciclos. MabThera debe ser administrado el día 1 de cada ciclo de quimioterapia, después del componente glucocorticoide de la quimioterapia, si corresponde. Terapia de mantenimiento: Linfoma folicular previamente no tratado: La posología recomendada de MabThera formulación subcutánea, cuando se utiliza para el tratamiento de mantenimiento en pacientes con linfoma folicular no tratados previamente que han respondido a la terapia de inducción es de 1.400 mg una vez cada 2 meses (empezando dos meses después de la última dosis de la terapia de inducción) hasta progresión de la enfermedad o hasta un período máximo de dos años (12 administraciones). Linfoma folicular en recaída o refractario: La posología recomendada de MabThera formulación subcutánea, cuando se utiliza para el tratamiento de mantenimiento en pacientes con linfoma folicular que están en recaída o son refractarios, que han respondido a la terapia de inducción es de 1.400 mg una vez cada 3 meses (empezando 3 meses después de la última dosis de la terapia de inducción) hasta progresión de la enfermedad o hasta un período máximo de dos años. Linfoma No-Hodgkin difuso de células B grandes: MabThera debe usarse en combinación con quimioterapia CHOP. La posología recomendada es: primer ciclo, MabThera formulación intravenosa de 375 mg/m2 de superficie corporal, seguido por ciclos posteriores con MabThera formulación subcutánea inyectado con una dosis fija de 1.400 mg por ciclo. En total: durante 8 ciclos. MabThera se administra en el primer día de cada ciclo de quimioterapia, después de la infusión intravenosa del componente glucocorticoide del CHOP. No se han establecido la seguridad y eficacia de la combinación de MabThera con otras quimioterapias en Linfoma No-Hodgkin difuso de células B grandes. Ajustes de la dosis durante el tratamiento: No se recomienda disminuir la dosis de MabThera. Cuando se administra MabThera en combinación con quimioterapia, se deben realizar las reducciones estándares de la dosis para medicamentos quimioterapéuticos (véase Reacciones adversas). Poblaciones especiales: Población pediátrica: No se ha establecido la seguridad y eficacia de MabThera en niños menores de 18 años. No existen datos disponibles. Pacientes de edad avanzada: No se requiere ajustar la dosis en los pacientes de edad avanzada ( > 65 años de edad). Forma de administración: Inyecciones subcutáneas: MabThera formulación subcutánea debe ser administrado únicamente como inyección subcutánea, durante aproximadamente 5 minutos. La aguja hipodérmica para inyección debe introducirse en la jeringa inmediatamente antes de la administración para evitar el riesgo de coagulación de la aguja. MabThera formulación subcutánea debe ser inyectado subcutáneamente en la pared abdominal y nunca se deben utilizar áreas en las que la piel presente irritación, hematomas, sensibilidad, durezas o en zonas con lunares o cicatrices. No se dispone de datos si la inyección se lleva a cabo en otras partes del cuerpo; por lo tanto, la aplicación debe limitarse a la pared abdominal. Durante el curso de tratamiento con MabThera formulación subcutánea, se recomienda utilizar sitios diferentes para administrar otros medicamentos por vía subcutánea. En caso de interrumpir una inyección, se puede reutilizar el mismo sitio u otro distinto, según corresponda. Administración de la infusión intravenosa: Consulte el Prospecto Información para Profesionales y el Prospecto Información para el Paciente del producto para esta formulación (MabThera 100 mg y 500 mg, concentrado de solución para infusión) para conocer en detalle las instrucciones y métodos para administrar esta forma de presentación.
Contraindicaciones.
Hipersensibilidad al principio activo, a cualquiera de sus excipientes, a las proteínas murinas o a la hialuronidasa. Infecciones graves y activas (véase Precauciones). Pacientes en un estado inmunocomprometido grave.
Reacciones adversas.
La información proporcionada a continuación se refiere al uso de MabThera en oncología. Para información relacionada con las indicaciones autoinmunes, consultar el Prospecto Información para Profesionales y el Prospecto Información para el Paciente de MabThera formulación intravenosa. Resumen del perfil de seguridad: Durante el programa de desarrollo, el perfil de seguridad de MabThera formulación subcutánea fue similar al de la formulación intravenosa, excepto por las reacciones cutáneas locales. Dichas reacciones, incluyendo las que se presentan en el sitio de inyección, fueron muy frecuentes en pacientes que recibieron MabThera formulación subcutánea. En la fase 3 del ensayo SABRINA (BO22334), las reacciones cutáneas locales se reportaron en hasta el 20% de los pacientes que recibieron MabThera SC. Las reacciones cutáneas locales más frecuentes en el grupo de MabThera SC fueron eritema en el sitio de inyección (13%), dolor en el sitio de inyección (7%), y edema en el sitio de inyección (4%). Se observaron eventos similares en el estudi
o SAWYER (BO25341) en pacientes con Leucemia Linfocítica Crónica con la formulación subcutánea de MabThera 1.600 mg y se informaron en hasta el 42% de los pacientes en el grupo MabThera SC. La mayoría de las reacciones cutáneas locales frecuentes fueron eritema en el sitio de inyección (26%), dolor en el sitio de inyección (16%) e hinchazón en el sitio de inyección (5%). Los eventos observados luego de la administración subcutánea fueron leves o moderados, con excepción de un paciente en el estudio SABRINA que informó una reacción cutánea local de intensidad de Grado 3 (erupción en el sitio de inyección) después de la primera administración de MabThera SC (Ciclo 2) y dos pacientes en el estudio SAWYER que experimentaron reacciones cutáneas locales de Grado 3 (eritema, dolor e inflamación en el sitio de inyección). Las reacciones cutáneas locales de cualquier grado en el grupo de MabThera SC fueron más frecuentes durante el primer ciclo subcutáneo (Ciclo 2), seguido por el segundo, y la incidencia disminuyó con inyecciones posteriores. Reacciones adversas reportadas con el uso de MabThera formulación subcutánea: El riesgo de reacciones agudas relacionadas con la administración asociado con la formulación subcutánea de MabThera fue evaluado en tres estudios clínicos. En SABRINA, se notificaron casos de reacciones graves relacionadas con la administración (Grado ≥ 3) en dos pacientes (2%) luego de la administración de MabThera formulación subcutánea. Estos eventos fueron erupción en el sitio de inyección de Grado 3 y sequedad bucal. En el ensayo SparkThera, no se informaron reacciones graves relacionadas con la administración. En el estudio SAWYER (BO25341), en pacientes con Leucemia Linfocítica Crónica con la formulación subcutánea de MabThera 1.600 mg, reacciones graves relacionadas con la administración (Grado ≥ 3) se comunicaron en cuatro pacientes (5%) después de la administración MabThera SC. Estos eventos fueron trombocitopenia de Grado 4 y ansiedad de Grado 3, eritema en el sitio de inyección y urticaria. Reacciones adversas reportadas con el uso de MabThera formulación intravenosa: Experiencia en Linfoma No-Hodgkin y Leucemia Linfática Crónica: El perfil de seguridad global de MabThera en Linfoma No-Hodgkin (LNH) y en Leucemia Linfática Crónica (LLC) se basa en los datos de pacientes de los ensayos clínicos y del seguimiento poscomercialización. Estos fueron tratados ya sea con MabThera como monoterapia (como tratamiento de inducción o de mantenimiento después de la inducción) o en combinación con quimioterapia. En pacientes que recibieron MabThera, las reacciones adversas al medicamento observadas con mayor frecuencia fueron las relacionadas con la infusión y en la mayoría ocurrieron durante la primera infusión. La incidencia de los síntomas relacionados con la infusión disminuyó sustancialmente con las posteriores infusiones y fue menor que el 1% después de ocho dosis de MabThera. Los eventos infecciosos (predominantemente bacterianos y virales) se presentaron en aproximadamente el 30 - 55% de los pacientes con LNH y en el 30 - 50% de aquéllos con LLC durante los estudios clínicos. Las reacciones adversas graves al medicamento, notificadas u observadas con mayor frecuencia fueron: Reacciones relacionadas con la infusión (incluyendo síndrome de liberación de citoquinas, síndrome de lisis tumoral) (véase Precauciones). Infecciones (véase Precauciones). Trastornos cardiovasculares (véase Precauciones). Otras reacciones adversas graves al medicamento incluyen reactivación de la hepatitis B y LMP (véase Precauciones). En la Tabla 8 están incluidas las frecuencias de las reacciones adversas al medicamento informadas con MabThera tanto solo como en combinación con quimioterapia. Las reacciones adversas se enumeran en orden decreciente de gravedad dentro de cada intervalo de frecuencia. Las frecuencias se definen como muy frecuentes (≥ 1/10); frecuentes (≥ 1/100 a < 1/10); poco frecuentes (≥ 1/1.000 a < 1/100), raras (≥ 1/10.000 a < 1/1.000); muy raras ( < 1/10.000) y frecuencia no conocida (no puede ser estimada con los datos disponibles). Las reacciones adversas al medicamento identificadas sólo durante el seguimiento poscomercialización, y cuya frecuencia no puede ser estimada, se definen como "frecuencia no conocida". Lista tabulada de reacciones adversas:
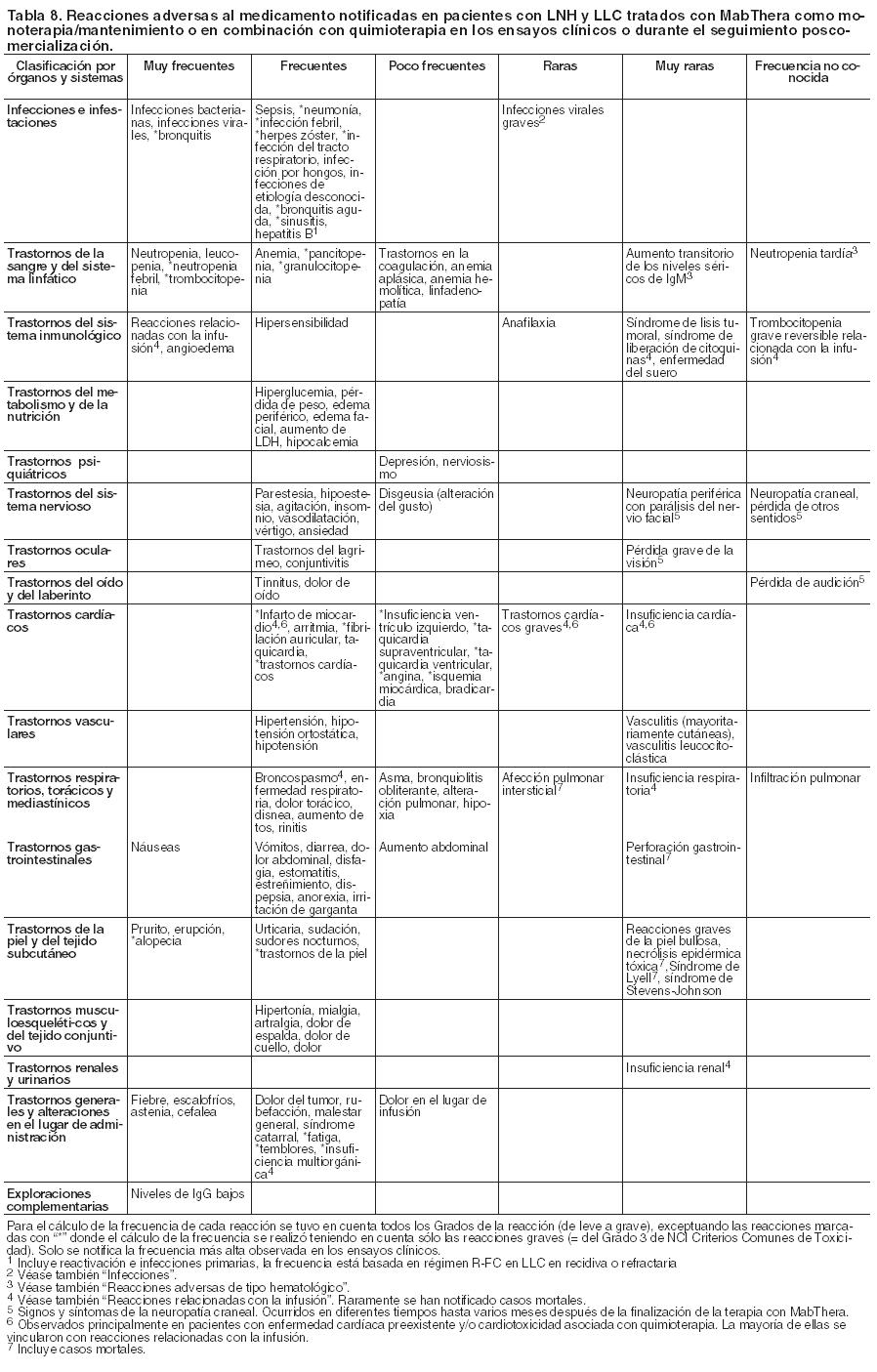
Los siguientes términos han sido comunicados como eventos adversos durante los ensayos clínicos; sin embargo, fueron reportados con una incidencia menor o similar ( < 2% de diferencia entre los grupos) en el grupo de MabThera comparado con el grupo control: hematotoxicidad, infección neutropénica, infección en el tracto urinario, trastorno sensorial, fiebre, shock séptico, superinfección pulmonar, infección de implante, septicemia por estafilococo, infección pulmonar, rinorrea, edema pulmonar, insuficiencia cardiaca, trombosis venosa, edema de miembros inferiores, fracción de eyección anormal, deterioro general de la salud física, caída, insuficiencia multiorgánica, trombosis venosa profunda de las extremidades, hemocultivo positivo, control inadecuado de la diabetes mellitus. El perfil de seguridad de MabThera en combinación con otras quimioterapias (por ejemplo MCP, CHIP-IN) es comparable con el que se describe para la combinación de MabThera y CVP, CHOP o FC en poblaciones equivalentes. Los signos y síntomas que sugieren una reacción relacionada con la infusión fueron reportados en más del 50% de los pacientes en los ensayos clínicos que involucraron MabThera formulación intravenosa, y fueron predominantemente observados durante la primera infusión, generalmente en las primeras dos horas. Estos síntomas consistieron principalmente en fiebre, escalofríos y rigidez. El perfil de seguridad de MabThera SC era por lo demás comparable a la de la formulación IV. No se han observado casos de anafilaxia o reacciones graves de hipersensibilidad, síndrome de liberación de citoquinas o síndrome de lisis tumoral después de la administración SC durante el programa de desarrollo subcutáneo. Otros síntomas incluyeron rubor, angioedema, broncospasmo, vómitos, náuseas, urticaria/rash, fatiga, cefalea, irritación de garganta, rinitis, prurito, dolor, taquicardia, hipertensión, hipotensión, disnea, dispepsia, astenia y características del síndrome de lisis tumoral. Las reacciones graves relacionadas con la infusión (tales como broncospasmo, hipotensión) ocurrieron en hasta el 12% de los pacientes al momento del primer ciclo del tratamiento con rituximab en combinación con quimioterapia. Reacciones adicionales informadas en algunos casos fueron: infarto de miocardio, fibrilación auricular, edema pulmonar y trombocitopenia aguda reversible. Se comunicaron con menor frecuencia o frecuencia desconocida, exacerbación de las patologías cardíacas preexistentes, tales como angina de pecho o insuficiencia cardíaca congestiva o trastornos cardíacos graves (insuficiencia cardíaca, infarto de miocardio, fibrilación auricular), edema pulmonar, insuficiencia multiorgánica, características del síndrome de lisis tumoral, síndrome de liberación de citoquinas, insuficiencia renal e insuficiencia respiratoria, dispepsia, rash, hipertensión, taquicardia y trombocitopenia aguda reversible. La incidencia de síntomas relacionados con la infusión disminuye considerablemente en las infusiones intravenosas siguientes y es menor al 1% de los pacientes en el octavo ciclo del tratamiento con MabThera. Descripción de reacciones adversas seleccionadas: Infecciones e Infestaciones: MabThera indujo la depleción de células B en aproximadamente el 70 - 80% de los pacientes, pero solamente en una minoría de ellos se asoció con una disminución de las inmunoglobulinas séricas. En los ensayos aleatorizados en el grupo de MabThera se notificó una mayor incidencia en las infecciones localizadas de Candida, así como de herpes zóster. Se informaron infecciones graves en aproximadamente el 4% de los pacientes tratados con MabThera como monoterapia. Comparando un tratamiento de mantenimiento con MabThera de hasta dos años de duración con el grupo en observación, se registraron frecuencias más elevadas de las infecciones globales, incluyendo algunas de Grados 3 o 4. No se observó toxicidad acumulada en las infecciones que se manifestaron durante los dos años del período de mantenimiento. Además, en los pacientes tratados con MabThera, se han comunicado otras infecciones virales graves, ya sean nuevas, reactivaciones o exacerbaciones, algunas de las cuales fueron mortales. La mayoría había recibido MabThera en combinación con quimioterapia o como parte de un trasplante de células madre hematopoyéticas. Ejemplos de estas infecciones virales graves son las causadas por los virus de la familia herpes (Citomegalovirus, Virus de la Varicela Zóster y Virus Herpes Simple), virus JC (Leucoencefalopatía Multifocal Progresiva [LMP]) y el virus de la hepatitis C. Se han informado en ensayos clínicos, casos de muerte por LMP después de progresión de la enfermedad y retratamiento. Se han notificado casos de reactivación de la hepatitis B, la mayoría de los cuales aparecieron en pacientes que recibieron MabThera en combinación con quimioterapia citotóxica. No se observó aumento en la frecuencia de las infecciones o infestaciones. Las infecciones más frecuentes fueron las referidas a las vías respiratorias superiores que se informaron en el 12.3% de los pacientes en R-CVP y 16,4% de los que recibieron CVP. Las infecciones graves se registraron en el 4,3% de los pacientes tratados con R-CVP y en el 4,4% a los que se administró CVP. No se informaron infecciones potencialmente mortales durante este estudio. En el estudio de R-CHOP la incidencia global de infecciones de Grados 2 a 4 fue del 45,5% en el grupo R-CHOP y del 42,3% en el grupo CHOP. Las infecciones de Grados 2 a 4 por hongos fueron más frecuentes en el grupo de R-CHOP (4,5% versus 2,6% en el grupo CHOP); esta diferencia se debió a una mayor incidencia de las infecciones por Candida localizadas durante el período de tratamiento. La incidencia de herpes zóster Grados 2 a 4 fue mayor en el grupo de R-CHOP (4,5%) que en el grupo CHOP (1,5%). La proporción de pacientes con infecciones Grados 2 a 4 y/o neutropenia febril fue del 55,4% en el grupo R-CHOP y del 51,5% en el grupo CHOP. Se ha observado una progresión del sarcoma de Kaposi en pacientes expuestos a MabThera con esta enfermedad preexistente. Estos casos ocurrieron en indicaciones no aprobadas y la mayoría de los pacientes eran VIH positivos. Trastornos de la sangre y del sistema linfático: En los ensayos clínicos con MabThera como monoterapia administrado durante 4 semanas, las anomalías hematológicas que aparecieron en una minoría de pacientes fueron, en general, leves y reversibles. Se notificaron casos graves de neutropenia (Grados 3/4) en un 4,2%, anemia en un 1,1% y trombocitopenia en el 1,7 % de los pacientes. Durante el tratamiento de mantenimiento con MabThera de hasta dos años se informó una mayor incidencia de casos de leucopenia (Grados 3/4, 5% vs 2%) y neutropenia (Grados 3/4, 10% vs 4%) comparado con el grupo en observación. La incidencia de trombocitopenia fue baja (Grados 3/4, < 1%) y no hubo diferencias entre los grupos del tratamiento. En aproximadamente la mitad de los pacientes con información disponible para la recuperación de células B después de la finalización del tratamiento de inducción con MabThera, transcurrieron 12 meses o más para que los niveles de células B volvieran a los valores normales. Durante los ciclos de tratamiento en los ensayos con MabThera en combinación con quimioterapia, leucopenia (Grados 3/4, R-CHOP 88% vs CHOP 79%) y neutropenia (R-CVP 24% vs CVP 14%; R-CHOP 97% vs CHOP 88%), generalmente se notificaron con mayor frecuencia comparada con la quimioterapia sola. Sin embargo, este aumento de los valores de neutropenia en pacientes tratados con MabThera y quimioterapia no se asoció con un mayor porcentaje de infecciones e infestaciones en comparación con aquellos tratados sólo con quimioterapia. No se observaron diferencias para la incidencia de anemia. Se informaron algunos casos de neutropenia tardía ocurridos después de más de 4 semanas posteriores a la última infusión con MabThera. Trastornos cardiovasculares: Durante los ensayos clínicos con MabThera como monoterapia, se informaron reacciones cardiovasculares en el 18,8% de los pacientes, siendo hipotensión e hipertensión las más frecuentes. Se notificaron casos de arritmia de Grados 3 o 4 (incluyendo taquicardia ventricular y supraventricular) y de angina de pecho durante la infusión. Durante el tratamiento de mantenimiento, la incidencia de los trastornos cardíacos de Grados 3/4 fue comparable entre los pacientes tratados con MabThera y el grupo en observación. Los eventos cardíacos fueron reportados como reacciones adversas graves (incluyendo fibrilación auricular (1%), infarto de miocardio (1%), insuficiencia del ventrículo izquierdo ( < 1%), isquemia miocárdica ( < 1%)) en el 3% de los pacientes tratados con MabThera en comparación con < 1% de los del grupo en observación. En los ensayos que evalúan MabThera en combinación con quimioterapia, la incidencia de arritmias cardíacas de Grados 3/4, predominantemente arritmias supraventriculares, tales como taquicardia y flutter/fibrilación auricular, fue mayor en el grupo de R-CHOP (14 pacientes, 6,9%) comparado con el grupo de CHOP (3 pacientes, 1,5%). Todas estas arritmias ocurrieron en el contexto de la infusión de MabThera o se asociaron con condiciones propensas como fiebre, infección, infarto agudo de miocardio o enfermedad preexistente respiratoria y cardiovascular (véase Precauciones). No se observaron diferencias entre los grupos de R-CHOP y CHOP en la incidencia de otras reacciones cardíacas de Grados 3 y 4, incluidas insuficiencia cardíaca, trastorno miocárdico y de las arterias coronarias. Trastornos respiratorios, torácicos y mediastínicos: Insuficiencia respiratoria / insuficiencia e infiltración pulmonar en el contexto de reacciones relacionadas con la infusión (ver Precauciones). En adición a los eventos pulmonares asociados con las infusiones, se han comunicado casos de enfermedad pulmonar intersticial, algunos con desenlace fatal. Trastornos neurológicos: Durante el período de tratamiento (fase del tratamiento de inducción que consta de R-CHOP como mínimo durante más de ocho ciclos), cuatro pacientes (2%) tratados con R-CHOP, todos con factores de riesgo cardiovascular, sufrieron accidentes cerebrovasculares tromboembólicos durante el primer ciclo. No hubo diferencias en la incidencia de otros eventos tromboembólicos entre los grupos de tratamiento. En contraste, tres pacientes (1,5%) tuvieron eventos cerebrovasculares en el grupo de CHOP, todos ellos ocurridos durante el período de seguimiento. Se han informado casos de Síndrome de Encefalopatía Posterior Reversible (SEPR)/Síndrome Leucoencefalopatía Posterior Reversible (SLPR). Los signos y síntomas incluyen alteraciones en la visión, dolor de cabeza, convulsiones y alteración del estado mental, con o sin hipertensión asociada. El diagnóstico de SEPR/SLPR debe confirmarse mediante técnicas de imagen cerebral. En estos casos se han reconocido factores de riesgo para SEPR/SLPR, incluyendo enfermedad subyacente, hipertensión, terapia inmunosupresora y/o quimioterapia. Raramente se notificaron casos de neuropatía craneal, como pérdida severa de la visión, pérdida de la audición, pérdida de otros sentidos como parálisis del nervio facial, que acaecieron en diferentes tiempos durante muchos meses después de la finalización de la terapia con MabThera. Trastornos gastrointestinales: En pacientes con Linfoma No-Hodgkin tratados con MabThera, se han observado casos de perforación gastrointestinal, que en algunos casos causaron la muerte. En la mayoría se administró MabThera en combinación con quimioterapia. Exploraciones complementarias: Niveles de IgG: En los ensayos clínicos que evaluaban el tratamiento de mantenimiento con MabThera en pacientes con linfoma folicular en recaída o refractario, la mediana de los niveles de IgG estaba por debajo del límite inferior de la normalidad (LIN) ( < 7g/l) después del tratamiento de inducción, en ambos grupos, tanto en el de observación como en el de MabThera. En el grupo en observación, la mediana del nivel de IgG aumentó posteriormente por encima de LIN, pero se mantuvo constante en el grupo de MabThera. La proporción de pacientes con niveles IgG por debajo de LIN fue aproximadamente del 60% en el grupo de MabThera durante los 2 años de tratamiento, mientras que en el grupo en observación descendió (36% después de 2 años). En pacientes pediátricos tratados con MabThera se ha observado un número pequeño de casos, espontáneos y en la bibliografía, de hipogammaglobulinemia, en algunas circunstancias grave y que requirió terapia prolongada de reemplazo de inmunoglobulina. No se conocen las consecuencias de la depleción prolongada de células B en esta población. Trastornos de la piel y del tejido subcutáneo: Se han notificado muy raramente casos de Necrólisis Epidérmica Tóxica (Síndrome de Lyell) y Síndrome de Stevens-Johnson, alguno con desenlace mortal. Terapia de combinación: Pacientes de edad avanzada (≥ 65 años): La incidencia de reacciones adversas sanguíneas y linfáticas de Grados 3/4 fue más elevada en pacientes de edad avanzada (≥ 65 años de edad) comparado con los más jóvenes, con LLC en recidiva o refractaria no tratados previamente. Enfermedad voluminosa o bulky: Los pacientes con enfermedad voluminosa o bulky tienen una incidencia mayor de reacciones adversas de Grados 3 y 4 que aquellos sin esta característica (25,6% versus 15,4%). La incidencia de cualquier reacción adversa fue similar en estos dos grupos (92,3% en pacientes con enfermedad voluminosa o bulky versus 89,2% en los que no la tienen.) Retratamiento con monoterapia: El porcentaje de pacientes que reportaron cualquier reacción adversa de Grados 3 y 4 y reacciones adversas después del retratamiento con más ciclos de MabThera fue similar al de aquellos que informaron cualquier reacción adversa y reacciones adversas de Grados 3 y 4 después de la exposición inicial (95,0% versus 89,7% para cualquier evento adverso y 13,3% versus 14,8% para reacciones adversas de Grados 3 y 4). Comunicación de reportes de reacciones adversas: Es importante comunicar las presuntas reacciones adversas después de la autorización del medicamento. Esto permite la monitorización continua de la relación riesgo/beneficio. Se solicita a los profesionales de la salud informar de cualquier sospecha de efectos adversos severos asociados con el uso de MabThera® al Área de Farmacovigilancia de Roche al siguiente teléfono 0800-77-ROCHE (76243). En forma alternativa, esta información puede ser reportada ante ANMAT. Ante cualquier inconveniente con el producto, el paciente puede llenar la ficha que está en la Página Web de la ANMAT: http://www.anmat.gov.ar/farmacovigilancia/Notificar.asp o llamar a ANMAT responde al 0800-333-1234.
Precauciones.
Para mejorar la trazabilidad de los medicamentos biológicos, el nombre del producto debe estar claramente registrado (o mencionado) en la historia clínica del paciente. La información proporcionada en Precauciones corresponde para el uso de MabThera formulación subcutánea en la indicación aprobada "Tratamiento de Linfoma No-Hodgkin". Para datos relacionados con otras indicaciones, referirse al Prospecto Información para Profesionales y al Prospecto Información para el Paciente de MabThera formulación intravenosa. El uso de MabThera formulación subcutánea como monoterapia en pacientes con Linfoma folicular estadios III-IV que son quimiorresistentes o están en su segunda o subsecuente recaída después de quimioterapia no puede ser recomendado, debido a que la seguridad de la administración subcutánea semanal no ha sido establecida. Leucoencefalopatía Multifocal Progresiva: El uso de MabThera puede asociarse con un mayor riesgo de Leucoencefalopatía Multifocal Progresiva (LMP). Los pacientes deben ser monitorizados a intervalos regulares para detectar cualquier nuevo signo o síntoma neurológico, así como cualquier empeoramiento que pueda indicar LMP. Se han reportado casos de Leucoencefalopatía Multifocal Progresiva (LMP) durante el uso de MabThera en NHL y LLC (ver Reacciones adversas). La mayoría de los pacientes lo habían recibido en combinación con quimioterapia o como parte de un trasplante de células madre hematopoyéticas. Si se sospechase que el paciente sufre LMP, debe suspenderse la administración de MabThera hasta que se haya descartado dicha posibilidad. El médico debe evaluar a los pacientes para determinar si los síntomas constituyen señales de alteración neurológica, y si es así, si son indicativos de LMP. Se debe considerar si está clínicamente indicada la consulta con un neurólogo. Si existe alguna duda, además de la evaluación, deberá considerarse un estudio de imagen de resonancia magnética preferiblemente con contraste, un análisis del LCR para detectar ADN del virus JC y la repetición de las evaluaciones neurológicas. El médico debe estar especialmente alerta a los síntomas indicativos de LMP, que el paciente pueda no advertir (por ejemplo, manifestaciones cognitivas, neurológicas o psiquiátricas). Se le debe aconsejar que informe a su pareja o a la persona que lo cuide, acerca de su tratamiento, ya que ellos pueden detectar síntomas de los cuales el paciente no es consciente. Si el paciente desarrolla LMP, se debe suspender el tratamiento con MabThera permanentemente. En pacientes inmunocomprometidos con LMP, se ha observado la estabilización o mejora del desenlace clínico después de la reconstitución del sistema inmune. Se desconoce si la detección precoz de LMP y la suspensión del tratamiento con MabThera pueden llevar a una estabilización similar o a una mejoría del desenlace clínico. Reacciones relacionadas con la administración: MabThera está asociado con reacciones relacionadas con la infusión/administración, que pueden vincularse con la liberación de citoquinas y/u otros mediadores químicos. El síndrome de liberación de citoquinas puede no diferenciarse clínicamente de las reacciones agudas de hipersensibilidad. Este conjunto de manifestaciones que incluyen el síndrome de liberación de citoquinas, síndrome de lisis tumoral y reacciones anafilácticas e hipersensibilidad se describen a continuación. Estas no están específicamente relacionadas con la vía de administración de MabThera y pueden ser observadas con ambas formulaciones. Se han comunicado reacciones severas relacionadas con la infusión con desenlace fatal durante la etapa de poscomercialización de MabThera formulación intravenosa, con un inicio que oscila dentro de 30 minutos a 2 horas después de comenzar la primera infusión de MabThera formulación intravenosa. Estas incluyen eventos pulmonares y en algunos casos lisis tumoral rápida y las características del síndrome de lisis tumoral, además de fiebre, escalofríos, rigidez, hipotensión, urticaria, angioedema y otros síntomas (véase Reacciones adversas). El síndrome de liberación de citoquinas grave se reconoce por presentar disnea grave, frecuentemente acompañada de broncospasmo e hipoxia, además de fiebre, escalofríos, rigidez, urticaria y angioedema. Este síndrome puede estar relacionado con algunas características del síndrome de lisis tumoral, tales como hiperuricemia, hiperpotasemia, hipocalcemia, hiperfosfatemia, insuficiencia renal aguda, elevación de la lactato dehidrogenasa (LDH) y también con insuficiencia respiratoria aguda y muerte. La insuficiencia respiratoria aguda puede estar acompañada por eventos tales como, infiltración intersticial o edema pulmonar, visibles a la exploración radiológica torácica. El síndrome se manifiesta frecuentemente dentro de la primera o segunda hora después de iniciar la primera infusión. Los pacientes con antecedentes de insuficiencia pulmonar o con infiltración tumoral pulmonar, pueden tener un riesgo mayor de mal pronóstico y deben aumentarse las precauciones durante su tratamiento. En aquéllos que desarrollen síndrome de liberación de citoquinas grave se debe interrumpir la infusión inmediatamente (véase Dosificación) y deben recibir medicación sintomática de choque. Dado que a la mejoría inicial de los síntomas clínicos puede seguir una recidiva, se debe monitorizar estrechamente a estos pacientes hasta que el síndrome de lisis tumoral y la infiltración pulmonar se hayan resuelto o hayan sido descartados. Una vez solucionados completamente los signos y síntomas, raramente se repite el síndrome de liberación de citoquinas en tratamientos posteriores. Los pacientes con gran masa tumoral como los pacientes con LLC y linfoma de células del manto o con un elevado número de células tumorales circulantes (≥ 25 x 109/l), que pueden tener un riesgo mayor de desarrollar un síndrome de liberación de citoquinas muy grave, deben tratarse, extremando las precauciones durante el tratamiento. Estos pacientes deben monitorizarse muy estrechamente durante la primera infusión y en ellos se debe considerar reducir la velocidad de la primera infusión o un fraccionamiento de la dosis durante más de dos días en el primer ciclo y algún ciclo posterior si el recuento de linfocitos es aún > 25 x 109/l. Se han notificado casos de reacciones de hipersensibilidad, incluyendo anafilácticas, después de la administración intravenosa de proteínas. A diferencia del síndrome de liberación de citoquinas, los episodios verdaderos de hipersensibilidad se presentan generalmente durante los primeros minutos de la infusión. Conviene disponer para uso inmediato de medicamentos utilizados para combatirlos, es decir, adrenalina, antihistamínicos y glucocorticoides, por si ocurriera una reacción alérgica durante la administración de MabThera. Las manifestaciones clínicas de anafilaxia pueden parecerse a las del síndrome de liberación de citoquinas anteriormente descripto. Las reacciones atribuibles a la hipersensibilidad se han informado menos frecuentemente que las vinculadas con la liberación de citoquinas. Además de las reacciones mencionadas, se informaron algunos casos de infarto de miocardio, fibrilación auricular, edema pulmonar y trombocitopenia reversible aguda. Dado que se puede producir hipotensión durante la administración de MabThera, se debe considerar interrumpir los tratamientos antihipertensivos 12 horas antes de la misma. En el 77% de los pacientes tratados con MabThera formulación intravenosa se han observado reacciones adversas relacionadas con la infusión (incluyendo el síndrome de liberación de citoquinas acompañado de hipotensión y broncospasmo en el 10% de los pacientes) (véase Reacciones adversas). Generalmente, estos síntomas son reversibles después de la interrupción de la infusión de MabThera y la administración de un antipirético, un antihistamínico y ocasionalmente oxígeno, solución salina intravenosa o broncodilatadores, y, en caso de necesidad, glucocorticoides. Para reacciones graves, véase "Síndrome de liberación de citoquinas". En pacientes que recibieron MabThera subcutáneo en los estudios clínicos, se han observado reacciones relacionadas con la administración en hasta el 50% de los pacientes. Estas ocurrieron dentro de las 24 horas después de la inyección subcutánea, consistiendo principalmente en eritema, prurito, erupción y reacciones relacionadas con la administración, tales como dolor, hinchazón, hemorragia y enrojecimiento y fueron generalmente de naturaleza leve a moderada (Grados 1 o 2) y transitorias. Las reacciones cutáneas locales fueron muy frecuentes en los ensayos clínicos en los pacientes que recibieron MabThera subcutáneo. Los síntomas incluyeron dolor, hinchazón, induración, hemorragia, eritema, prurito y erupción (véase Reacciones adversas). Algunas reacciones cutáneas locales se produjeron más de 24 horas después de la administración subcutánea de MabThera. La mayoría de las observadas después de la aplicación subcutánea fueron leves o moderadas y se resolvieron sin necesidad de tratamiento específico. Antes de comenzar con las inyecciones subcutáneas de MabThera, todos los pacientes deben recibir siempre previamente, una dosis completa de MabThera por infusión intravenosa, utilizando MabThera formulación intravenosa. El mayor riesgo de experimentar una reacción relacionada con la administración es generalmente observado en el ciclo 1. El inicio del tratamiento con MabThera formulación intravenosa permite demorar o detener la infusión intravenosa y un mejor manejo de las reacciones relacionadas con la administración. Si los pacientes no pudieron recibir una dosis completa de MabThera infusión intravenosa previa al cambio, deben continuar los ciclos posteriores con MabThera formulación intravenosa hasta que una dosis intravenosa completa sea administrada exitosamente. Por lo tanto, el cambio a MabThera formulación subcutánea sólo puede ocurrir en el ciclo 2 o en los siguientes. Como con la formulación intravenosa, MabThera formulación subcutánea debe ser administrada en un contexto en el que los equipos completos de reanimación estén inmediatamente disponibles y bajo la supervisión estricta de un profesional de la salud con experiencia. La premedicación, que incluye un analgésico/antipirético y un antihistamínico, siempre debe ser administrada antes de cada dosis de MabThera formulación subcutánea. También debe ser considerada la premedicación con glucocorticoides. Los pacientes deben ser observados durante por lo menos 15 minutos después de la administración subcutánea de MabThera. Un período más prolongado puede ser apropiado en aquéllos con un riesgo mayor de reacciones de hipersensibilidad. Se debe advertir a los pacientes que se comuniquen inmediatamente con su médico si se presentan síntomas que sugieren reacciones de hipersensibilidad severas o síndrome de liberación de citoquinas en cualquier momento después de la administración del medicamento. Eventos pulmonares: Los eventos pulmonares incluyen hipoxia, infiltración pulmonar e insuficiencia respiratoria aguda. Algunas de estas manifestaciones han sido precedidas por broncoespasmo severo y disnea. En algunos casos, los síntomas empeoran con el tiempo, mientras que en otros la mejoría inicial es seguida por un deterioro clínico. Por lo tanto, los pacientes que experimentaron eventos pulmonares u otros síntomas graves relacionados con la infusión deben ser estrechamente vigilados hasta que se produzca la resolución completa de sus síntomas. Los pacientes con antecedentes de insuficiencia pulmonar o con infiltración tumoral pulmonar pueden estar en mayor riesgo de mala evolución y deben ser tratados con mayor precaución. La insuficiencia respiratoria aguda puede estar acompañada de eventos tales como la infiltración intersticial pulmonar o edema, visible en una radiografía de tórax. El síndrome se manifiesta generalmente dentro de una o dos horas de iniciar la primera infusión. Los pacientes que experimentan eventos pulmonares graves deben interrumpir la administración de MabThera inmediatamente (véase Dosificación) y recibir tratamiento sintomático agresivo. Lisis tumoral rápida: MabThera media la rápida lisis de las células benignas y malignas CD20 positivas. Se ha informado que los signos y síntomas (por ejemplo, hiperuricemia, hiperpotasemia, hipocalcemia, hiperfosfatemia, insuficiencia renal aguda, elevación de la LDH), concordantes con el síndrome de lisis tumoral (SLT) se produjeron después de la primera infusión intravenosa de MabThera en pacientes con un alto número de linfocitos malignos circulantes. Se debe considerar la profilaxis para SLT para quienes estén en riesgo de desarrollar lisis tumoral rápida (por ejemplo, los que tienen una alta carga tumoral o un número alto ( > 25 x 109/l) de células malignas circulantes, como los pacientes con LLC y linfoma de células del manto). Estos pacientes deben ser seguidos de cerca y realizarse monitoreos de laboratorio adecuados. Debe proporcionarse una terapia médica apropiada a aquellos que desarrollan signos y síntomas compatibles con lisis tumoral rápida. Después del tratamiento y para la resolución completa de los signos y síntomas, la posterior terapia con MabThera IV se ha administrado en combinación con la profilaxis para SLT en un número limitado de casos. Trastornos cardíacos: Se han informado casos de angina de pecho, arritmias cardíacas, tales como flutter/aleteo y fibrilación auricular, insuficiencia cardíaca y/o infarto de miocardio en pacientes tratados con MabThera. Por lo tanto, se deben monitorizar cuidadosamente a quienes tengan antecedentes de enfermedad cardíaca y/o cardiotoxicidad asociada con la quimioterapia. Toxicidad hematológica: Aunque MabThera en monoterapia no tiene efecto mielosupresor, se recomienda prudencia antes de tratar a pacientes con un recuento de neutrófilos < 1,5 x 109/l y/o plaquetas < 75 x 109/l, puesto que la experiencia clínica en esta población es limitada. La formulación intravenosa de MabThera se ha utilizado en 21 pacientes sometidos a trasplante autólogo de médula ósea y en otros grupos de riesgo con función de la médula ósea presumiblemente reducida, sin que haya inducido mielotoxicidad. Se deben realizar recuentos de sangre total en forma regular, incluyendo recuento de neutrófilos y plaquetas, durante el tratamiento con MabThera. Cuando MabThera se administra en combinación con quimioterapia, deben realizarse hemogramas completos regulares de acuerdo con la práctica médica habitual. Infecciones: Durante el tratamiento con MabThera pueden producirse infecciones graves e incluso mortales (véase Reacciones adversas). MabThera no debe ser administrado a pacientes con infecciones graves activas (por ejemplo, tuberculosis, sepsis e infecciones oportunistas, véase Contraindicaciones). El médico debe tener especial precaución cuando considere el uso de MabThera en pacientes con antecedentes de infecciones crónicas o recurrentes o en condiciones subyacentes que puedan provocar una mayor predisposición a infecciones (véase Reacciones adversas). Se han informado casos de reactivación de hepatitis B, en pacientes tratados con la formulación intravenosa de MabThera, que incluyeron casos de hepatitis fulminante con fallecimiento. La mayoría de estos pacientes habían estado expuestos también a quimioterapia citotóxica. Los informes son confusos tanto por el estado de la enfermedad subyacente como por la quimioterapia citotóxica. En todos los pacientes se debe llevar a cabo la detección del virus de la hepatitis B (VHB) antes de iniciar el tratamiento con MabThera. Al menos debe incluir HBsAg y HBcAc. Esto puede ser complementado con otros marcadores apropiados de acuerdo con las normativas locales. Los pacientes con hepatitis B activa no deben ser tratados con MabThera. En aquéllos con serología positiva de hepatitis B (bien HBsAg o HBcAc), se debe consultar con un especialista en enfermedades hepáticas antes de iniciar el tratamiento y deben ser monitorizados y tratados siguiendo las normativas médicas locales para prevenir la reactivación de la hepatitis B. Se han notificado casos muy raros de Leucoencefalopatía Multifocal Progresiva (LMP), durante el uso poscomercialización de MabThera formulación intravenosa en LNH y LLC (véase Reacciones adversas). La mayoría de los pacientes habían recibido MabThera en combinación con quimioterapia o como parte de un trasplante de células madre hematopoyéticas. Los médicos que tratan a pacientes con LNH o LLC deben considerar la LMP en el diagnóstico diferencial de pacientes que informaron síntomas neurológicos y la consulta con un neurólogo debe considerarse como clínicamente indicada. Inmunizaciones: En pacientes con LNH no se ha estudiado la seguridad de la inmunización con vacunas de virus vivos después de recibir tratamiento con MabThera; por tanto, no se recomiendan estas vacunas. Los pacientes tratados con MabThera pueden recibir vacunas inactivadas; sin embargo, con éstas los porcentajes de respuesta pueden ser menores. En un estudio no aleatorizado de pacientes con LNH de bajo Grado con recidivas, que recibieron la formulación intravenosa de MabThera en monoterapia cuando se comparó con el grupo control no tratado sano, el porcentaje de respuesta a la vacunación fue menor con el antígeno de recuerdo del tétanos (16% comparado con 81%), y con neoantígeno Keyhole Limpet Haemocyanin (KLH) (4% comparado con 76% cuando se determinó un incremento > de 2 en el título de anticuerpo). Esto implicó que los títulos de anticuerpos medidos antes del tratamiento frente a antígenos como Streptococcus pneumoniae, gripe A, paperas, rubéola, y varicela, se mantuvieron hasta al menos 6 meses después del tratamiento con MabThera Reacciones cutáneas: Se han reportado casos de reacciones cutáneas graves, tales como necrólisis epidérmica tóxica (Síndrome de Lyell) y Síndrome de Stevens-Johnson, algunas con desenlace fatal (véase Reacción adversas). En caso de un evento de este tipo, con presunta relación con MabThera, el tratamiento debe suspenderse en forma permanente. Efectos sobre la capacidad para conducir y utilizar máquinas: No se han realizado estudios de los efectos de MabThera sobre la capacidad para conducir y utilizar máquinas, aunque la actividad farmacológica y las reacciones adversas notificadas hasta la fecha sugieren que MabThera podría tener un efecto nulo o insignificante sobre esta habilidad. Fertilidad, embarazo y lactancia: Anticoncepción en hombres y mujeres: Debido al largo tiempo de permanencia de rituximab en el organismo en pacientes con depleción de células B, las mujeres en edad fértil deben usar métodos contraceptivos eficaces durante y hasta 12 meses después del tratamiento con MabThera. Embarazo: Se sabe que las inmunoglobulinas IgG atraviesan la barrera placentaria. No se han determinado los niveles de linfocitos B en recién nacidos de madres expuestas a MabThera en ensayos clínicos. No existen datos suficientes ni controlados de los estudios en mujeres embarazadas; sin embargo, se han notificado depleción transitoria de células B y linfocitopenia en algunos niños nacidos de madres expuestas a MabThera durante el embarazo. Similares efectos han sido observados en estudios en animales (véase Farmacología, Datos preclínicos sobre seguridad). Por estos motivos, MabThera no debe administrarse a mujeres embarazadas, a menos que el beneficio esperado supere el riesgo potencial. En los ensayos de toxicidad del desarrollo llevados a cabo en monos cinomolgos, no se han hallado indicios de embriotoxicidad intrauterina. Las crías de animales nacidas de madres expuestas a MabThera presentaron una depleción de las poblaciones de linfocitos B durante el período posnatal. La formulación SC contiene hialuronidasa humana recombinante (rHuPH20) (véase Composición). Los estudios farmacocinéticos y toxicológicos en animales demuestran reducción en el peso fetal y aumento en el número de reabsorciones después de la inyección de rHuPH20, a niveles de exposición sistémica materna comparables a los que podrían manifestarse después de la administración en bolo accidental IV de un solo vial de la formulación MabThera SC en los seres humanos, con base en los supuestos más conservadores posibles. Además, durante el programa de desarrollo rituximab SC, se encontró un paciente con
niveles mensurables de rHuPH20 en muestras de sangre tomadas después de la administración SC, sin que se observaran efectos adversos. Con el fin de reducir el riesgo potencial adicional de toxicidad embriofetal resultante de la exposición a rHuPH20, las pacientes que conciban mientras estén siendo tratadas con MabThera SC deben discontinuar el tratamiento con la formulación SC. Lactancia: Se desconoce si rituximab se excreta en la leche materna. Sin embargo, teniendo en cuenta que la IgG se elimina en la leche materna y que se ha detectado rituximab en la leche de monas en período de lactancia, las mujeres no deben amamantar a sus hijos durante el tratamiento con MabThera ni durante los 12 meses siguientes. Fertilidad: Los estudios en animales no han revelado efectos deletéreos de rituximab o hialuronidasa humana recombinante (rHuPH20) en los órganos reproductores.
Interacciones.
Actualmente existen datos limitados sobre las posibles interacciones medicamentosas con MabThera. La administración conjunta con MabThera no parece influir sobre la farmacocinética de fludarabina o ciclofosfamida. Además, no se registró ningún efecto aparente de fludarabina y ciclofosfamida sobre la farmacocinética de MabThera. La administración concomitante con metotrexato no tuvo ningún efecto sobre la farmacocinética de MabThera en pacientes con artritis reumatoidea. Los pacientes con títulos de anticuerpos humanos antimurinos o antiquiméricos (HAMA/HACA) pueden sufrir reacciones alérgicas o de hipersensibilidad al ser tratados con otros anticuerpos monoclonales terapéuticos o de diagnóstico.
Incompatibilidades.
No se han observado incompatibilidades entre la formulación subcutánea de MabThera y el material de polipropileno o policarbonato de la jeringa, o las agujas para transferencia e inyección de acero inoxidable, y los tapones cónicos Luer de polietileno.
Conservación.
Los viales deben conservarse en heladera entre 2°C y 8°C. No congelar. Conservar los viales en el embalaje exterior para proteger su contenido de la luz. Para las condiciones de conservación después de abrir por primera vez, véase "Período de validez". Precauciones especiales de eliminación y otras manipulaciones: MabThera se suministra en viales monodosis, apirógenos, estériles, sin conservantes. Se deben cumplir estrictamente las siguientes instrucciones referentes al uso y a la eliminación de jeringas y otros objetos medicinales punzantes: Nunca reutilizar agujas y jeringas. Colocar todas las agujas y jeringas en un recipiente descartable para objetos punzantes. La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él se realizará de acuerdo con la normativa local. Este medicamento no debe ser utilizado después de la fecha de vencimiento indicada en el envase. Este medicamento debe ser usado exclusivamente bajo prescripción y vigilancia médica y no puede repetirse sin nueva receta médica. Mantenga los medicamentos fuera del alcance de los niños. Período de validez: Una vez transferida del vial a la jeringa, la solución de MabThera formulación subcutánea se mantiene física y químicamente estable durante 48 horas a 2°C - 8°C y, posteriormente, durante 8 horas a 30°C en luz difusa. Desde un punto de vista microbiológico, el producto debe ser utilizado de inmediato. Caso contrario, la preparación debe realizarse bajo condiciones controladas y mediante técnicas asépticas validadas. El tiempo y las condiciones de almacenamiento antes de usar son responsabilidad del usuario.
Sobredosificación.
La experiencia disponible acerca de las sobredosis de la formulación intravenosa de MabThera procedente de estudios clínicos en seres humanos es limitada. La dosis intravenosa máxima hasta la fecha es 5.000 mg (2.250 mg/m2), evaluada en un estudio de aumento de dosis en pacientes con leucemia linfocítica crónica. No se identificaron señales de seguridad adicionales. Los pacientes que experimenten sobredosis deberán interrumpir inmediatamente la infusión y ser monitoreados estrechamente. Tres pacientes en el estudio SABRINA (BO22334) de MabThera formulación subcutánea fueron inadvertidamente tratados con la formulación subcutánea por vía intravenosa con hasta un máximo de dosis de rituximab de 2780 mg sin manifestar ningún efecto adverso. Los pacientes que experimenten sobredosis o medicación errónea deberán ser monitorizados estrechamente. Se debe considerar la necesidad de un seguimiento periódico del recuento de células sanguíneas y del aumento del riesgo de infecciones mientras los pacientes estén con depleción de células B. Después de la comercialización, se notificaron cinco casos de sobredosis de MabThera. En tres de ellos no se registraron reacciones adversas. En los otros dos los efectos adversos fueron síntomas gripales, con una dosis de 1,8 g de rituximab e insuficiencia respiratoria mortal, con una dosis de 2 g de rituximab. Ante la eventualidad de una sobredosificación concurrir al Hospital más cercano o comunicarse con los Centros de Toxicología: Hospital de Pediatría Dr. Ricardo Gutiérrez: 4962-6666/2247; Policlínico Dr. G. A. Posadas: 4654-6648; 4658-7777; Hospital General de Niños Dr. Pedro de Elizalde: 4300-2115; 4363-2100 /2200 Interno 6217.
Presentación.
Vial de 15 ml con 1.400 mg/11,7 ml (120mg/ml): envase con 1.
Revisión.
Enero 2016. Aprobación: 02/05/2016. Disp. ANMAT N° 4.819 (RI+EMA+Shpe+ CDS:26.0C+27.0C).
MabThera® s.c.
ROCHE
1600 mg
Agente antineoplásico, anticuerpo monoclonal.
Composición.
Cada vial contiene: 1.600 mg de rituximab en una solución de 13,4 ml (120 mg/ml). Excipientes: hialuronidasa humana recombinante (rHuPH20) 2.000 U/ml, L-histidina y clorhidrato de L-histidina monohidrato 20 mM, a, a-trehalosa, dihidrato 210 mM, L-metionina 10 mM, polisorbato 80: 0,06% (m/v) y volumen total ajustado con agua para preparaciones inyectables c.s.
Farmacología.
Código ATC: L01XC02. Grupo farmacoterapéutico: Agentes antineoplásicos - Anticuerpos monoclonales. Propiedades farmacodinámicas: Mecanismo de acción: MabThera formulación subcutánea contiene hialuronidasa humana recombinante (rHuPH20), una enzima que se utiliza para incrementar la dispersión y la absorción de sustancias concomitantes, al administrarlas por vía subcutánea. Rituximab es un anticuerpo monoclonal quimérico murino/humano que se une específicamente al antígeno CD20, una fosfoproteína transmembranaria no-glucosilada, expresada en los linfocitos pre-B y B maduros. El antígeno se expresa en más del 95% de todos los linfomas no-Hodgkin (LNH) de células B. El antígeno CD20 se expresa tanto en células B normales como en tumorales, pero no en células madre hematopoyéticas, células pro-B, células plasmáticas normales ni en otros tejidos normales. Este antígeno no se internaliza tras la unión del anticuerpo ni se elimina de la superficie celular. El CD20 no circula en el plasma como antígeno libre y, por esta razón, no compite por la unión con los anticuerpos. El dominio Fab de rituximab se une al antígeno CD20 en la superficie de los linfocitos B, mientras que el dominio Fc puede incorporar efectores de la respuesta inmune para mediar la lisis de las células B. Los mecanismos posibles de la lisis celular mediada por efector incluyen la citotoxicidad dependiente del complemento (CDC), como resultado de la unión de Clq y la citotoxicidad celular dependiente de anticuerpos (ADCC) mediada por uno o más receptores Fcc de la superficie de los granulocitos, macrófagos y células NK (natural killer). También se ha demostrado que la unión de rituximab al antígeno CD20 de los linfocitos B induce la muerte celular por apoptosis. Después de completarse la administración de la primera dosis de MabThera, los recuentos de células B periféricas disminuyeron por debajo de lo normal. En los pacientes tratados con neoplasias hematológicas, la recuperación de células B comenzó a los 6 meses de tratamiento y en general, los niveles normales se lograron a los 12 meses de finalizado el mismo, aunque en algunos pacientes se requirió un lapso más prolongado (hasta un tiempo medio de recuperación de 23 meses después de la terapia de inducción). Experiencia clínica de MabThera formulación subcutánea en leucemia linfocítica crónica: Un estudio de Fase Ib (BO25341 - SAWYER) de dos partes, multicéntrico, aleatorizado, abierto, de grupos paralelos fue llevado a cabo en pacientes con LLC no tratados previamente, para investigar la no inferioridad del perfil farmacocinético, junto con la eficacia y seguridad de MabThera SC en combinación con quimioterapia. El objetivo de la Parte 1 fue seleccionar una dosis de MabThera SC que lograra niveles de Cvalle comparables con MabThera IV. Los pacientes con LLC no tratados previamente (n=64) fueron incorporados en cualquier momento durante su tratamiento con MabThera IV en combinación con quimioterapia. La dosis de 1.600 mg de MabThera SC fue elegida para la Parte 2 del estudio. El objetivo de la Parte 2 fue establecer la no inferioridad en los niveles de Cvalle observados entre la dosis confirmada de MabThera SC y la dosis de referencia de MabThera IV. Los pacientes con LLC no tratados previamente (n=176) fueron aleatorizados en los dos grupos de tratamiento: MabThera SC (n= 88); primer ciclo de MabThera IV 375 mg/m2 en combinación con quimioterapia más ciclos posteriores (2-6) de MabThera SC 1.600 mg asociado con quimioterapia. MabThera IV (n= 88): primer ciclo de MabThera IV 375 mg/m2 en combinación con quimioterapia seguido por hasta 5 ciclos de MabThera IV 500 mg/m2 en combinación con quimioterapia. Las tasas de respuesta fueron similares para MabThera IV y SC, con una tasa de respuesta global de 80.7% (95% CI: 70.9; 88.3) y 85.2% (95% CI: 76.1; 91.9) en los grupos de MabThera IV y SC respectivamente. Las estimaciones puntuales de la tasa de respuesta completa fueron 33,0% (95% IC: 23.3; 43.8) y 26.1% (95% IC: 17.3; 36.6) en los grupos de MabThera IV y SC, respectivamente. Los resultados globales confirman que MabThera SC 1.600 mg tiene un perfil riesgo/beneficio comparable al de MabThera IV 500 mg/m2. Experiencia clínica de MabThera concentrado para solución para infusión en leucemia linfocítica crónica: En dos estudios aleatorizados y abiertos (BO17072 - REACH; CLL-8/ML17102), un total de 817 pacientes con leucemia linfocítica crónica no tratados previamente y 552 con LLC en recidiva o refractaria se aleatorizaron para recibir cada uno quimioterapia FC (fludarabina 25 mg/m2, ciclofosfamida 250 mg/m2 , 1-3 días), cada 4 semanas, durante 6 ciclos o MabThera en combinación con FC (R-FC). MabThera fue administrado en una dosis de 375 mg/m2 un día antes de la quimioterapia durante el primer ciclo y en una dosis de 500 mg/m2 en el día 1 de cada ciclo de tratamiento posterior. Los pacientes fueron excluidos del estudio para LLC en recidiva o refractaria si previamente habían sido tratados con un anticuerpo monoclonal o si eran refractarios (definido como fracaso para alcanzar una remisión parcial durante por lo menos 6 meses) a fludarabina o a cualquier otro análogo de nucleósido. Se analizaron para la eficacia un total de 810 pacientes (403 R-FC, 407 FC) para el estudio de primera línea (Tabla 1a y Tabla 1b) y 552 (276 R-FC, 276 FC) para el estudio de recidiva o refractarios (Tabla 2). En el estudio de primera línea, después de una mediana de observación de 48,1 meses, la mediana de sobrevida libre de progresión fue de 55 meses en el grupo R-FC y de 33 meses en el grupo FC (p < 0,0001, log-rank test). El análisis de sobrevida global mostró un beneficio significativo del tratamiento con R-FC frente a FC, quimioterapia sola, (p = 0,0319, log-rank test) (Tabla 1a) El beneficio en términos de SLP se observó en forma sostenida en muchos de los subgrupos de pacientes analizados de acuerdo con el riesgo de la enfermedad de base (es decir, estadios A-C de Binet) y fue confirmado con un seguimiento más prolongado (Tabla 1b).


En los estudio de LLC en recidiva o refractaria, la mediana de sobrevida libre de progresión (variable principal) fue de 30,6 meses en el grupo R-FC y de 20,6 meses en el grupo FC (p=0,0002, log-rank test). El beneficio en términos de SLP fue observado en casi todos los subgrupos de pacientes analizados de acuerdo con el riesgo de enfermedad de base. Un ligero, pero no significativo aumento en la sobrevida global, fue notificado en la comparación del R-FC con el grupo FC.

Los resultados de otros estudios de soporte que utilizaron MabThera en combinación con otros regímenes de quimioterapia (incluyendo CHOP, FCM, PC, PCM, bendamustina y cladribina) para el tratamiento de pacientes con leucemia linfocítica crónica (LLC) en recidiva o refractaria o no tratados previamente demostraron también una alta tasa de respuesta global con beneficios en términos de SLP, aunque con una toxicidad ligeramente más elevada (especialmente mielotoxicidad). Estos estudios apoyan el uso de MabThera con quimioterapia. Datos en aproximadamente 180 pacientes previamente tratados con MabThera han demostrado beneficio clínico (incluyendo Respuesta Completa) y avalan el uso de MabThera en retratamiento. Inmunogenicidad: Los datos del programa de desarrollo SC indican que la formación de anticuerpos antirituximab (HACAs) después de la administración SC es comparable con el observado después de la administración IV. En el estudio SABRINA (BO22334), en pacientes con Linfoma Folicular con la formulación subcutánea de MabThera 1.400 mg, la incidencia de los anticuerpos antirituximab inducidos/incrementados por el tratamiento en el grupo SC fue bajo o similar al observado en el grupo IV (1% IV vs 2% SC). La incidencia de los anticuerpos anti rHuPH20 inducidos/incrementados por el tratamiento fue del 6% en el grupo IV comparado con el 9% en el grupo SC, y ninguno de los pacientes que fueron positivos para anticuerpos anti rHuPH20 fueron positivos para anticuerpos neutralizantes. La proporción global de pacientes en los que se observaron anticuerpos anti rHuPH20 resultó generalmente constante durante el periodo de seguimiento en ambas cohortes. En el estudio SAWYER (BO25341), en pacientes con Leucemia Linfocítica Crónica con la formulación subcutánea de MabThera 1.600 mg, la incidencia de los anticuerpos antirituximab inducidos/incrementados por el tratamiento fue similar en los dos grupos de tratamiento; 6,7% IV vs. 2,4% SC. La incidencia de los anticuerpos anti rHuPH20 inducidos/incrementados por el tratamiento sólo se midió en pacientes en el grupo SC y fue 10,6%. Ninguno de los pacientes que fueron positivos para anticuerpos anti rHuPH20 fueron positivos para anticuerpos neutralizantes. No se conoce la relevancia clínica del desarrollo de anticuerpos anti rHuPH20 o antirituximab después del tratamiento con MabThera SC. No hubo impacto de la presencia de anticuerpos anti rHuPH20 o antirituximab en la seguridad o eficacia en ambos estudios. Propiedades farmacocinéticas: Absorción: MabThera en una dosis fija de 1.600 mg fue administrada por 5 ciclos SC en intervalos de 4 semanas, a continuación del primer ciclo de MabThera IV, en pacientes con LLC no tratados previamente en combinación con quimioterapia (fludarabina y ciclofosfamida (FC)). La Cmáx sérica de MabThera en el Ciclo 6 fue más baja en el grupo de MabThera SC que en el de IV, con un valor de promedio geométrico (CV%) de 202 (36.1) mg/ml y 280 (24.6) mg/ml con la relación de la media geométrica resultante (Cmáx, SC/Cmáx, IV) de 0.719 (90% IC: 0.653, 0.792). El promedio geométrico Tmáx para MabThera SC fue aproximadamente de 3 días en comparación con el Tmáx resultante en el final o cerca del final de la infusión para MabThera IV. Distribución/Eliminación: Estudio SAWYER (BO25341): MabThera en una dosis fija de 1.600 mg fue administrado como una inyección SC, en el abdomen a intervalos de 4 semanas. Los pacientes con LLC CD20+ no tratados previamente fueron aleatorizados 1:1 para recibir MabThera SC (primer ciclo rituximab IV seguido por 5 ciclos de rituximab SC) o MabThera IV (6 ciclos) en combinación con hasta 6 ciclos de quimioterapia FC administrada cada cuatro semanas. Los valores del promedio geométrico de Cvalle en el ciclo 5 (pre-dosis ciclo 6) fueron más altos en el grupo MabThera SC que en el grupo MabThera IV (97,5 mg/ml versus 61,5 mg/ml respectivamente). De manera similar, los valores del promedio geométrico del ABC en el ciclo 6 fueron más altos en el grupo MabThera SC que en el de MabThera IV (4.088 mg·día/ml versus 3.630 mg·día/ml respectivamente). Poblaciones especiales: No hay información disponible en relación con la farmacocinética en pacientes con insuficiencia renal o hepática. Según el estudio BO22334, en pacientes con Linfoma Folicular con la formulación subcutánea de MabThera 1.400 mg, se observó un efecto entre la proporción del tamaño corporal y la exposición reportada en el ciclo 7, entre 1.400 mg de rituximab formulación subcutánea administrado cada 3 semanas y 375 mg/m2 de rituximab formulación intravenosa administrado cada 3 semanas con proporciones de Cvalle de 2,29, 1,31 y 1,41 en los pacientes con área de la superficie corporal (ASC) baja, media y alta, respectivamente (ASC baja ≤ 1,70 m2; 1,70 m2 < ASC media < 1,90 m2; ASC alta ≥ 1,90 m2). Las proporciones correspondientes de ABCt fueron 1,66, 1,17 y 1,32. No se registró evidencia de dependencia clínicamente relevante de la farmacocinética de rituximab sobre la edad y el sexo. En solo 13 pacientes se detectaron anticuerpos anti-rituximab que no generaron un incremento clínicamente significativo en el clearance en estado estacionario. Datos preclínicos sobre seguridad: Se ha demostrado que rituximab posee una alta especificidad para el antígeno CD20 de las células B. Durante los ensayos de toxicidad en monos cinomolgos no se registró ningún otro efecto además de la depleción de células B en la sangre periférica y en el tejido linfático, previsible por el mecanismo farmacológico. Se han realizado estudios de toxicidad en el desarrollo en monos cinomolgos que recibieron dosis de hasta 100 mg/kg (tratamiento desde el día 20 hasta el día 50 de la gestación); no se apreciaron evidencias de toxicidad fetal debidas a rituximab. No obstante, se observó, en forma dosis-dependiente y mediada por el mecanismo farmacológico, una depleción de células B en los órganos linfáticos de los fetos, que persistió después del nacimiento y se acompañó de una disminución de los niveles de IgG de los animales recién nacidos afectados. El recuento de células B de estos animales se normalizó en los 6 primeros meses de vida y no afectó negativamente a la reacción a la vacunación. No se han realizado estudios a largo plazo en animales para establecer el potencial carcinogénico de rituximab ni pruebas estándares para investigar la mutagenicidad, ya que éstas no son relevantes en el caso concreto de esta molécula. No se han efectuado estudios específicos para determinar la influencia de rituximab o rHuPH20 sobre la fertilidad. En general, no se observaron efectos nocivos en los órganos reproductores de machos o hembras en los estudios de toxicidad en monos cinomolgos. Adicionalmente, no se demostraron efectos de rHuPH20 sobre la calidad del semen. En estudios de desarrollo embriofetal en ratones, rHuPH20 produce reducción del peso fetal y pérdida de implantaciones a exposiciones sistémicas suficientemente superiores a la exposición terapéutica humana. No existe evidencia de dismorfogénesis (es decir, teratogénesis) derivada de la exposición sistémica a rHuPH20.
Indicaciones.
MabThera 1.600 mg solución para inyección subcutánea está indicado en pacientes adultos en combinación con quimioterapia para el tratamiento de pacientes con leucemia linfocítica crónica no tratada previamente o en recidiva o refractaria a un tratamiento previo. Sólo se dispone de datos limitados en relación con eficacia y seguridad para pacientes previamente tratados con anticuerpos monoclonales incluyendo MabThera o pacientes refractarios al tratamiento previo con MabThera y quimioterapia. (Para más información véase Farmacología - Propiedades farmacodinámicas).
Dosificación.
El reemplazo por cualquier otro agente biológico requiere el consentimiento del médico prescriptor. La formulación subcutánea de MabThera debe ser administrada bajo la estrecha supervisión de un médico experto y en un entorno que disponga en forma inmediata de un equipo completo de reanimación. Antes de cada administración de MabThera, siempre se debe suministrar premedicación consistente en un antipirético y un antihistamínico, por ejemplo paracetamol y difenhidramina. Se debe considerar la premedicación con glucocorticoides si MabThera no se va a administrar en combinación con quimioterapia que contenga esteroides. Posología: La dosis recomendada de MabThera formulación subcutánea utilizada en pacientes adultos con LLC es una inyección subcutánea con una dosis fija de 1.600 mg, independientemente del área de superficie corporal del paciente. Antes de comenzar con las inyecciones subcutáneas de MabThera, todos los pacientes deben recibir siempre previamente, una dosis completa de MabThera por infusión intravenosa, utilizando MabThera formulación intravenosa (véase Precauciones). Por lo tanto, el cambio a MabThera formulación subcutánea sólo puede ocurrir en el segundo ciclo o en los ciclos posteriores de tratamiento. Si los pacientes no pudieron recibir una dosis completa de la infusión intravenosa de MabThera antes del cambio, deben continuar los ciclos posteriores con MabThera formulación intravenosa hasta que se administre correctamente una dosis intravenosa completa. Es importante verificar el prospecto del medicamento a fin de garantizar que se está administrando al paciente la correcta concentración y/o formulación (intravenosa o subcutánea), según la indicación clínica. La formulación subcutánea de MabThera no debe administrarse por vía intravenosa, únicamente por inyección subcutánea. MabThera 1.600 mg solución para inyección subcutánea está indicada únicamente para el uso en leucemia linfocítica crónica (LLC). En pacientes con LLC se recomienda una profilaxis con adecuada hidratación y administración de uricostáticos 48 horas antes de comenzar la terapia para disminuir el riesgo del síndrome de lisis tumoral. Para los pacientes con LLC cuyo recuento de linfocitos sea > 25 x 109/l se recomienda administrar 100 mg de prednisona/prednisolona intravenosa poco después de la infusión con MabThera para reducir el riesgo y la gravedad de las reacciones agudas de la infusión y/o el síndrome de liberación de citoquinas. Primera administración intravenosa: La primera administración de MabThera IV debe realizarse mediante infusión intravenosa en una dosis de 375 mg/m2 de superficie corporal. La velocidad de infusión inicial recomendada es de 50 mg/h; posteriormente, la tasa puede ser escalada en incrementos de 50 mg/h cada 30 minutos hasta un máximo de 400 mg/h. Posteriores administraciones subcutáneas: Los pacientes que no fueron capaces de recibir la dosis completa de MabThera IV, deben continuar los ciclos posteriores con dosis de MabThera IV. Para los pacientes que son capaces de recibir la dosis completa por infusión de MabThera IV, se puede optar por administrar MabThera SC en los ciclos posteriores (ver Precauciones). La dosis recomendada de MabThera SC en combinación con quimioterapia es de 1.600 mg, administrados en el día 1 de cada ciclo de quimioterapia durante 5 ciclos. La quimioterapia se debe dar después de la administración de MabThera. Ajustes de la dosis durante el tratamiento: No se recomienda disminuir la dosis de MabThera. Cuando éste se administre en combinación con quimioterapia, se deben aplicar las reducciones de dosis estándares de la misma. Poblaciones especiales: Población pediátrica: No se ha establecido todavía la seguridad y eficacia de MabThera en niños menores de 18 años. No existen datos disponibles. Pacientes de edad avanzada: No se requiere ajustar la dosis en los pacientes de edad avanzada ( > 65 años de edad). Forma de administración: Inyecciones subcutáneas: MabThera formulación subcutánea debe ser administrado únicamente como inyección subcutánea, durante aproximadamente 5 minutos. La aguja para inyección subcutánea debe introducirse en la jeringa inmediatamente antes de la administración para evitar el riesgo de coagulación de la aguja. MabThera formulación subcutánea debe ser inyectado subcutáneamente en la pared abdominal y nunca se deben utilizar áreas en las que la piel presente irritación, hematomas, sensibilidad, durezas o en zonas con lunares o cicatrices. No se dispone de datos si la inyección se lleva a cabo en otras partes del cuerpo; por lo tanto, la aplicación debe limitarse a la pared abdominal. Durante el curso de tratamiento con MabThera formulación subcutánea, se recomienda utilizar sitios diferentes para administrar otros medicamentos por vía subcutánea. En caso de interrumpir una inyección, se puede volver a aplicarla en el mismo sitio u otro distinto, según corresponda. Administración de la infusión intravenosa: Consulte el Prospecto Información para Profesionales y el Prospecto Información para el Paciente del producto para esta formulación (MabThera 100 mg y 500 mg, concentrado de solución para infusión) para conocer en detalle las instrucciones y métodos para administrar esta forma de presentación.
Contraindicaciones.
Hipersensibilidad al principio activo, a cualquiera de sus excipientes, a las proteínas murinas, a la hialuronidasa o a cualquier otro excipiente listado en la sección Composición. Infecciones graves y activas (véase Precauciones). Pacientes en un estado inmunocomprometido grave.
Reacciones adversas.
La información proporcionada a continuación se refiere al uso de MabThera en oncología. Para datos relacionados con las indicaciones autoinmunes, consultar el Prospecto Información para Profesionales y el Prospecto Información para el Paciente de MabThera formulación intravenosa. Resumen del perfil de seguridad: Durante el programa de desarrollo, el perfil de seguridad de MabThera formulación subcutánea fue similar al de la formulación intravenosa, excepto por las reacciones localizadas en el lugar de la inyección. Dichas reacciones fueron muy frecuentes en pacientes que recibieron MabThera formulación subcutánea en los estudios SparkThera (BP22333) y SABRINA (BO22334), reportadas en hasta el 50% de los pacientes en algún momento durante el tratamiento. Los síntomas incluían dolor, inflamación, endurecimiento, hemorragias, eritema, prurito y erupción cutánea. Todas las manifestaciones observadas luego de la administración subcutánea fueron leves o moderadas, con excepción de un paciente que experimentó un episodio de erupción cutánea Grado 3 en el lugar de la inyección y otro que informó xerostomía (sequedad bucal) Grado 3. Reacciones adversas reportadas con el uso de MabThera formulación subcutánea: El riesgo de reacciones agudas asociado con la formulación subcutánea de MabThera fue evaluado en tres estudios clínicos abiertos. En el estudio BO22334 que incluyó a pacientes con linfoma folicular durante la inducción y el mantenimiento, se notificaron casos de reacciones graves relacionadas con la administración (Grado ≥ 3) en dos pacientes luego de la administración de MabThera formulación subcutánea (un paciente reportó erupción cutánea Grado 3 en el lugar de la inyección y otro xerostomía Grado 3), ambos luego del ciclo 2 de la inducción, es decir, la primera dosis de MabThera formulación subcutánea administrada a cada paciente. En el Estudio BP22333 que incluyó a pacientes con linfoma folicular durante el mantenimiento únicamente, no se informaron reacciones graves relacionadas con la administración. En el estudio SAWYER (BO25341), reacciones graves relacionadas con la administración (Grado ≥ 3) se comunicaron en cuatro pacientes (5%) después de la administración MabThera SC. Estos eventos fueron trombocitopenia de Grado 4 y ansiedad de Grado 3, eritema en el sitio de inyección y urticaria. Reacciones adversas reportadas con el uso de MabThera formulación intravenosa: Experiencia en Linfoma No-Hodgkin y Leucemia Linfocítica Crónica: El perfil de seguridad global de MabThera en Linfoma No-Hodgkin (LNH) y en Leucemia Linfocítica Crónica (LLC) se basa en los datos de pacientes de los ensayos clínicos y del seguimiento poscomercialización. Estos fueron tratados ya sea con MabThera como monoterapia (como tratamiento de inducción o de mantenimiento después de la inducción) o en combinación con quimioterapia. En pacientes que recibieron MabThera, las reacciones adversas al medicamento observadas con mayor frecuencia fueron las relacionadas con la infusión y en la mayoría ocurrieron durante la primera infusión. La incidencia de los síntomas relacionados con la infusión disminuyó sustancialmente con las posteriores infusiones y fue menor que el 1% después de ocho dosis de MabThera. Las reacciones adicionales informadas fueron dispepsia, erupción, hipertensión, taquicardia, características del síndrome de lisis tumoral. También se reportaron casos aislados de infarto de miocardio, fibrilación auricular, edema pulmonar y trombocitopenia aguda reversible. Durante los estudios clínicos de LNH, aproximadamente el 30 - 55% de los pacientes experimentaron reacciones infecciosas (en su mayoría bacterianas y virales) y en los estudios de LLC las cifras fueron del 30 - 50%. Las reacciones adversas graves al medicamento, notificadas u observadas con mayor frecuencia fueron: Reacciones relacionadas con la infusión (incluyendo síndrome de liberación de citoquinas, síndrome de lisis tumoral) (véase Precauciones). Infecciones (véase Precauciones). Acontecimientos cardiovasculares (véase Precauciones). Otras reacciones adversas graves al medicamento incluyen reactivación de la hepatitis B y LMP (véase Precauciones). En la Tabla 3 están incluidas las frecuencias de las reacciones adversas al medicamento informadas con MabThera tanto solo como en combinación con quimioterapia. Las reacciones adversas se enumeran en orden decreciente de gravedad dentro de cada intervalo de frecuencia. Las frecuencias se definen como muy frecuentes (≥ 1/10); frecuentes (≥ 1/100 a < 1/10); poco frecuentes (≥ 1/1.000 a < 1/100), raras (≥ 1/10.000 a < 1/1.000); muy raras ( < 1/10.000) y frecuencia no conocida (no puede ser estimada con los datos disponibles). Las reacciones adversas al medicamento identificadas sólo durante el seguimiento poscomercialización, y cuya frecuencia no puede ser estimada, se definen como "frecuencia no conocida". Lista tabulada de reacciones adversas:

Los siguientes términos han sido comunicados como eventos adversos durante los ensayos clínicos; sin embargo, fueron reportados con una incidencia menor o similar ( < 2% de diferencia entre los grupos) en el grupo de MabThera comparado con el grupo control: hematotoxicidad, infección neutropénica, infección en el tracto urinario, trastorno sensorial, fiebre, shock séptico, superinfección pulmonar, infección de implante, septicemia por estafilococo, infección pulmonar, rinorrea, edema pulmonar, insuficiencia cardíaca, trombosis venosa, edema de miembros inferiores, fracción de eyección anormal, deterioro general de la salud física, caída, insuficiencia multiorgánica, trombosis venosa profunda de las extremidades, hemocultivo positivo, control inadecuado de la diabetes mellitus. Los signos y síntomas indican que más del 50% de los pacientes en los ensayos clínicos sufrieron reacciones relacionadas con la infusión, que en su mayoría se observaron durante la primera infusión, generalmente en las primeras dos horas. Estos síntomas incluyeron principalmente fiebre, escalofríos y rigidez. Las reacciones cutáneas locales, incluyendo las que se producen en el sitio de inyección, fueron muy frecuentes en los pacientes que recibieron MabThera. En la Fase 3 del estudio SABRINA (BO22334), en pacientes con Linfoma Folicular con la formulación subcutánea de MabThera 1.400 mg, se notificaron reacciones cutáneas locales en hasta el 20% de los pacientes tratados con MabThera SC. Las reacciones cutáneas locales más frecuentes en el grupo MabThera SC fueron eritema en el sitio de inyección (13%), dolor en el sitio de inyección (7%), edema en el sitio de inyección (4%). Se observaron eventos similares en el estudio SAWYER (BO25341) en pacientes con Leucemia Linfocítica Crónica con la formulación subcutánea de MabThera 1.600 mg y se reportaron en hasta el 42% de los pacientes en el grupo MabThera SC. La mayoría de las reacciones cutáneas locales frecuentes fueron eritema en el sitio de inyección (26%), dolor en el sitio de inyección (16%), e hinchazón (5%). Los eventos observados tras la administración subcutánea fueron leves o moderados, excepto en un paciente en el estudio SABRINA que informó una reacción cutánea local de intensidad Grado 3 (erupción en el sitio de inyección) y dos pacientes en el estudio SAWYER que experimentaron reacciones cutáneas locales de Grado 3 (eritema en el sitio de inyección, dolor en el sitio de inyección, e inflamación en el sitio de inyección). Las reacciones cutáneas locales de cualquier grado en el grupo MabThera SC fueron más frecuentes durante el primer ciclo SC (Ciclo 2), seguido por el segundo, y la incidencia disminuyó con las inyecciones posteriores. El perfil de seguridad de MabThera SC era por lo demás comparable a la de la formulación IV. No se han observado casos de anafilaxia o reacciones graves de hipersensibilidad, síndrome de liberación de citoquinas o síndrome de lisis tumoral después de la administración SC durante el programa de desarrollo subcutáneo. Otros síntomas incluyeron rubor, angioedema, broncoespasmo, vómitos, náuseas, urticaria/rash, fatiga, cefalea, irritación de garganta, rinitis, prurito, dolor, taquicardia, hipertensión, hipotensión, disnea, dispepsia, astenia y características del síndrome de lisis tumoral. Las reacciones graves relacionadas con la infusión (tales como broncoespasmo, hipotensión) ocurrieron en hasta el 12% de los pacientes al momento del primer ciclo del tratamiento con rituximab en combinación con quimioterapia. Reacciones adicionales informadas en algunos casos fueron: infarto de miocardio, fibrilación auricular, edema pulmonar y trombocitopenia aguda reversible. Se comunicaron con menor frecuencia o frecuencia desconocida, exacerbación de las patologías cardíacas preexistentes, tales como angina de pecho o insuficiencia cardíaca congestiva o trastornos cardíacos graves (insuficiencia cardíaca, infarto de miocardio, fibrilación auricular), edema pulmonar, insuficiencia multiorgánica, síndrome de lisis tumoral, síndrome de liberación de citoquinas, insuficiencia renal e insuficiencia respiratoria. La incidencia de síntomas relacionados con la infusión disminuye considerablemente en las infusiones intravenosas siguientes y es menor al 1% de los pacientes en el octavo ciclo del tratamiento con MabThera. Descripción de reacciones adversas seleccionadas a MabThera: Infecciones e Infestaciones: MabThera indujo la depleción de células B en aproximadamente el 70 - 80% de los pacientes, pero se asoció con una disminución de las inmunoglobulinas séricas solamente en una minoría de ellos. Se informaron infecciones graves en aproximadamente el 4% de los pacientes tratados con MabThera como monoterapia. Comparando un tratamiento de mantenimiento con MabThera de hasta dos años de duración con el grupo de observación, se registraron frecuencias más elevadas de las infecciones globales, incluyendo algunas de Grados 3 o 4. No se observó toxicidad acumulada en las infecciones que se manifestaron durante los dos años del período de mantenimiento. Además, en los pacientes tratados con MabThera, se han comunicado otras infecciones virales graves, ya sean nuevas, reactivaciones o exacerbaciones, algunas de las cuales fueron mortales. La mayoría había recibido MabThera en combinación con quimioterapia o como parte de un trasplante de células madre hematopoyéticas. Ejemplos de estas infecciones virales graves son las causadas por los virus de la familia herpes (Citomegalovirus, Virus de la Varicela Zóster y Virus Herpes Simple), virus JC (Leucoencefalopatía Multifocal Progresiva [LMP]) y el virus de la hepatitis C. Se han informado en ensayos clínicos, casos de muerte por LMP después de progresión de la enfermedad y retratamiento. Se han notificado casos de reactivación de la hepatitis B, la mayoría de los cuales aparecieron en pacientes que recibieron MabThera en combinación con quimioterapia citotóxica. En pacientes con LLC en recidiva o refractaria, la incidencia de infección de hepatitis B (reactivación o infección primaria), Grados 3 - 4, fue 2% en R-FC comparado con 0% en FC. Se ha observado una progresión del sarcoma de Kaposi en pacientes expuestos a MabThera con esta enfermedad preexistente. Estos casos ocurrieron en indicaciones no aprobadas y la mayoría de los pacientes eran VIH positivos. Trastornos de la sangre y del sistema linfático: En los ensayos clínicos con MabThera como monoterapia administrado durante 4 semanas, las anomalías hematológicas que aparecieron en una minoría de pacientes fueron, en general, leves y reversibles. Se notificaron casos graves de neutropenia (Grados 3/4) en un 4,2%, anemia en un 1,1% y trombocitopenia en el 1,7 % de los pacientes. Durante el tratamiento de mantenimiento con MabThera de hasta dos años se informó una mayor incidencia de casos de leucopenia (Grados 3/4, 5% vs 2%) y neutropenia (Grados 3/4, 10% vs 4%) comparado con el grupo de observación. La incidencia de trombocitopenia fue baja (Grados 3/4, < 1%) y no hubo diferencias entre los grupos del tratamiento. En aproximadamente la mitad de los pacientes con información disponible para la recuperación de células B después de la finalización del tratamiento de inducción con MabThera, transcurrieron 12 meses o más para que los niveles de células B volvieran a los valores normales. Durante los ciclos de tratamiento en los ensayos con MabThera en combinación con quimioterapia, la leucopenia (Grados 3/4, R-CHOP 88% vs CHOP 79%, R-FC 23% vs. FC 12%) y la neutropenia (R-CVP 24% vs CVP 14%; R-CHOP 97% vs CHOP 88%, R-FC 30% vs. FC 19% en pacientes con LLC no tratados previamente, pancitopenia (R-FC 3% vs. FC 1% en pacientes con LLC no tratados previamente), se notificaron normalmente con mayor frecuencia comparada con la quimioterapia sola. Sin embargo, este aumento de los valores de neutropenia en pacientes tratados con MabThera y quimioterapia no se asoció con un mayor porcentaje de infecciones e infestaciones en comparación con aquellos tratados sólo con quim
ioterapia. Los estudios en pacientes con LLC previamente no tratados que están en recaída o refractario, han demostrado que hasta en el 25% de los pacientes tratados con R-FC la neutropenia se prolongó (definida como que el recuento de neutrófilo permanece por debajo de 1 x 109/l entre los días 24 y 42 después de la última dosis) o fue de aparición tardía (definida como recuento de neutrófilos por debajo de 1 x 109 /l tras los 42 días después de la última dosis en pacientes que no tuvieron neutropenia prolongada o que se recuperaron antes del día 42) tras el tratamiento en el grupo de MabThera y FC. No se observó una diferencia relevante entre los grupos de tratamiento con respecto a anemia de Grado 3 y 4 o trombocitopenia. En el estudio de primera línea para LLC, la anemia de Grados 3/4 fue reportada por el 4% de los pacientes tratados con E-FC comparado con el 7% de los que recibieron FC, y la trombocitopenia de Grados 3/4 por el 7% de los pacientes del grupo R-FC en comparación con el 10% en el grupo FC. En el estudio de LLC en recidiva o refractaria, eventos adversos de anemia de Grados 3/4 fueron informados por el 12% de los pacientes tratados con R-FC en comparación con el 13% de los que recibieron FC y la trombocitopenia de Grados 3/4 reportada por el 11% de los pacientes en el grupo R-FC en comparación con el 9% en el grupo FC. Se informaron algunos casos de neutropenia tardía ocurridos después de más de 4 semanas posteriores a la última infusión con MabThera. En los ensayos de LLC en primera línea en el estadio C de la clasificación de Binet los pacientes en el grupo de R-FC experimentaron mayor número de reacciones adversas frente al grupo de FC (R-FC 83% comparado con FC 71%). En el estudio de LLC en recidiva o refractaria, fue notificada trombocitopenia Grados 3/4 en el 11% de pacientes en el grupo R-FC en comparación con el 9% en el grupo FC. En los estudios de MabThera en pacientes con macroglobulinemia de Waldenström se han observado aumentos transitorios en los niveles séricos de IgM después del inicio del tratamiento que pueden estar asociados con hiperviscosidad y síntomas relacionados. El incremento transitorio de IgM generalmente descendió hasta por lo menos el nivel basal en un período de 4 meses. En los estudios poscomercialización se han comunicado casos de trombocitopenia aguda reversible relacionada con la infusión. Trastornos cardiovasculares: Durante los ensayos clínicos con MabThera como monoterapia, se informaron reacciones cardiovasculares en el 18,8% de los pacientes, siendo hipotensión e hipertensión las más frecuentes. Se notificaron casos de arritmia de Grados 3 o 4 (incluyendo taquicardia ventricular y supraventricular) y de angina de pecho durante la infusión. Durante el tratamiento de mantenimiento, la incidencia de los trastornos cardíacos de Grados 3/4 fue comparable entre los pacientes tratados con MabThera y el grupo de observación. Los eventos cardíacos fueron reportados como reacciones adversas graves (incluyendo fibrilación auricular, infarto de miocardio, insuficiencia del ventrículo izquierdo, isquemia miocárdica) en el 3% de los pacientes tratados con MabThera en comparación con < 1% de los del grupo de observación. En los ensayos que evalúan MabThera en combinación con quimioterapia, la incidencia de arritmias cardíacas de Grados 3/4, predominantemente arritmias supraventriculares, tales como taquicardia y flutter/fibrilación auricular, fue mayor en el grupo de R-CHOP (14 pacientes, 6,9%) comparado con el grupo de CHOP (3 pacientes, 1,5%). Todas estas arritmias ocurrieron en el contexto de la infusión de MabThera o se asociaron con condiciones propensas como fiebre, infección, infarto agudo de miocardio o enfermedad preexistente respiratoria y cardiovascular (ver Precauciones). No se observaron diferencias entre los grupos de R-CHOP y CHOP en la incidencia de otras reacciones cardíacas de Grados 3 y 4, incluidas insuficiencia cardíaca, trastornos miocárdicos y de las arterias coronarias. En LLC, la incidencia global de trastornos cardíacos de Grados 3/4 fue menor tanto en los ensayos de primera línea de tratamiento (4% R-FC comparado con 3% FC) como en los estudios de recidiva o refractarios (4% R-FC comparado con 4% FC). En los estudios poscomercialización se observaron eventos cardíacos severos, incluyendo insuficiencia cardíaca e infarto de miocardio, principalmente en pacientes con una condición cardíaca previa y/o con quimioterapia cardiotóxica y mayormente asociado con reacciones relacionadas con la infusión. Se reportaron muy raros casos de vasculitis, predominantemente cutánea, como vasculitis leucocitoclástica. Trastornos respiratorios, torácicos y mediastínicos: Insuficiencia respiratoria / insuficiencia e infiltración pulmonar en el contexto de reacciones relacionadas con la infusión (ver Precauciones). En adición a los eventos pulmonares asociados con las infusiones, se han comunicado casos de enfermedad pulmonar intersticial con resultado de muerte. Trastornos neurológicos: Durante el período de tratamiento (fase del tratamiento de inducción que consta de R-CHOP como mínimo durante más de ocho ciclos), cuatro pacientes (2%) tratados con R-CHOP, todos con factores de riesgo cardiovascular, sufrieron accidentes cerebrovasculares tromboembólicos durante el primer ciclo. No hubo diferencias en la incidencia de otros eventos tromboembólicos entre los grupos de tratamiento. En contraste, tres pacientes (1,5%) tuvieron episodios cerebrovasculares en el grupo de CHOP, todos ellos ocurridos durante el período de seguimiento. En LLC, la incidencia global de trastornos del sistema nervioso Grados 3 o 4 fue menor, tanto en ensayos de primera línea de tratamiento (4% R-FC comparado con 4% FC) como en estudios de recidiva o refractarios (3% R-FC comparado con 3% FC). Se han informado casos de Síndrome de Encefalopatía Posterior Reversible (SEPR)/Síndrome Leucoencefalopatía Posterior Reversible (SLPR). Los signos y síntomas incluyen alteraciones en la visión, dolor de cabeza, convulsiones y alteración del estado mental, con o sin hipertensión asociada. El diagnóstico de SEPR/SLPR debe confirmarse mediante técnicas de imagen cerebral. En estos casos se han reconocido factores de riesgo para SEPR/SLPR, incluyendo enfermedad subyacente, hipertensión, terapia inmunosupresora y/o quimioterapia. Raramente se notificaron casos de neuropatía craneal, como pérdida severa de la visión, pérdida de la audición, pérdida de otros sentidos como parálisis del nervio facial, que acaecieron en diferentes tiempos durante muchos meses después de la finalización de la terapia con MabThera. Trastornos gastrointestinales: En pacientes con Linfoma No-Hodgkin tratados con MabThera, se han observado casos de perforación gastrointestinal, que en algunos casos causaron la muerte. En la mayoría se administró MabThera en combinación con quimioterapia. Exploraciones complementarias: Niveles de IgG: En los ensayos clínicos que evaluaban el tratamiento de mantenimiento con MabThera en pacientes con linfoma folicular en recaída o refractario, después del tratamiento de inducción, la mediana de los niveles de IgG estaba por debajo del límite inferior de la normalidad (LIN) ( < 7g/L) en ambos grupos, tanto en el de observación como en el de MabThera. En el grupo de observación, la mediana del nivel de IgG aumentó posteriormente por encima de LIN, pero se mantuvo constante en el grupo de MabThera. La proporción de pacientes con niveles IgG por debajo de LIN fue aproximadamente del 60% en el grupo de MabThera durante los 2 años de tratamiento, mientras que en el grupo de observación descendió (36% después de 2 años). En pacientes pediátricos tratados con MabThera se ha observado un número pequeño de casos, espontáneos y en la bibliografía, de hipogammaglobulinemia, en algunas circunstancias grave y que requirió terapia prolongada de reemplazo de inmunoglobulina. No se conocen las consecuencias de la depleción prolongada de células B en esta población. Trastornos de la piel y del tejido subcutáneo: Se han notificado muy raramente casos de Necrólisis Epidérmica Tóxica (Síndrome de Lyell) y Síndrome de Stevens-Johnson, alguno con desenlace mortal. Subpoblaciones y Monoterapia - 4 semanas de tratamiento: Pacientes de edad avanzada (≥ 65 años): La incidencia de cualquier reacción y de las reacciones adversas de Grados 3/4 fueron similares en pacientes de edad avanzada y en jóvenes (88,3% versus 92,0% para cualquier reacción adversa y 16,0% versus 18,1% para las reacciones adversas de Grados 3 y 4). Terapia de combinación: Pacientes de edad avanzada (≥ 65 años): La incidencia de reacciones adversas sanguíneas y linfáticas de Grados 3/4 fue más elevada en pacientes de edad avanzada (≥ 65 años de edad) comparado con los más jóvenes, con LLC en recidiva o refractaria no tratados previamente. Enfermedad voluminosa o bulky: Los pacientes con enfermedad voluminosa o bulky tienen una incidencia mayor de reacciones adversas de Grados 3 y 4 que aquellos sin esta característica (25,6% versus 15,4%). La incidencia de cualquier reacción adversa fue similar en estos dos grupos (92,3% en pacientes con enfermedad voluminosa o bulky versus 89,2% en los que no la tienen). Retratamiento con monoterapia: El porcentaje de pacientes que reportaron cualquier reacción adversa de Grados 3 y 4 y reacciones adversas después del retratamiento con más ciclos de MabThera fue similar al porcentaje de pacientes que reportaron cualquier reacción adversa y reacciones adversas de Grados 3 y 4 después de la exposición inicial (95,0% versus 89,7% para cualquier evento adverso y 13,3% versus 14,8% para reacciones adversas de Grados 3 y 4). Comunicación de reportes de reacciones adversas: Es importante comunicar las presuntas reacciones adversas después de la autorización del medicamento. Esto permite la monitorización continua de la relación riesgo/beneficio. Se solicita a los profesionales de la salud informar sobre cualquier sospecha de eventos adversos asociados con el uso de MabThera al Área de Farmacovigilancia de Roche al siguiente teléfono 0800-77-ROCHE (76243). En forma alternativa, esta información puede ser reportada ante ANMAT. Ante cualquier inconveniente con el producto, el paciente puede llenar la ficha que está en la Página Web de la ANMAT: http://www.anmat.gov.ar/farmacovigilancia/Notificar.asp o llamar a ANMAT responde al 0800-333-1234.
Precauciones.
Para mejorar la trazabilidad de los medicamentos biológicos, el nombre del producto administrado debe estar claramente registrado (o mencionado) en la historia clínica del paciente. La información proporcionada en Precauciones corresponde para el uso de MabThera formulación subcutánea en las indicaciones aprobadas "Tratamiento de Linfoma No-Hodgkin" (concentración 1.400 mg) y "Tratamiento de Leucemia Linfocítica Crónica" (concentración 1.600 mg). Para datos relacionados con otras indicaciones, referirse al Prospecto Información para Profesionales y al Prospecto Información para el Paciente de MabThera formulación intravenosa. Leucoencefalopatía Multifocal Progresiva: El uso de MabThera puede asociarse con un mayor riesgo de Leucoencefalopatía Multifocal Progresiva (LMP). Los pacientes deben ser monitorizados a intervalos regulares para detectar cualquier nuevo signo o síntoma neurológico, así como cualquier empeoramiento que pueda indicar LMP. Casos de Leucoencefalopatía Multifocal Progresiva (LMP) han sido reportados durante el uso de MabThera en NHL y LLC (ver Reacciones adversas). La mayoría de los pacientes lo habían recibido en combinación con quimioterapia o como parte de un trasplante de células madre hematopoyéticas. Si se sospechase que el paciente sufre LMP, debe suspenderse la administración de MabThera hasta que se haya descartado dicha posibilidad. El médico debe evaluar a los pacientes para determinar si los síntomas constituyen señales de alteración neurológica, y si es así, si son indicativos de LMP. Se debe estimar si está clínicamente indicada la consulta con un neurólogo. Si existe alguna duda, además de la evaluación, deberá considerarse un estudio de imagen de resonancia magnética preferiblemente con contraste, un análisis del LCR para detectar ADN del virus JC y la repetición de las evaluaciones neurológicas. El médico debe estar especialmente alerta a los síntomas indicativos de LMP, que el paciente pueda no advertir (por ejemplo, manifestaciones cognitivas, neurológicas o psiquiátricas). Se le debe aconsejar que informe a su pareja o a la persona que lo cuide, acerca de su tratamiento, ya que ellos pueden detectar síntomas de los cuales el paciente no es consciente. Si el paciente desarrolla LMP, se debe suspender el tratamiento con MabThera permanentemente. En pacientes inmunocomprometidos con LMP, se ha observado la estabilización o mejora del desenlace clínico después de la reconstitución del sistema inmune. Se desconoce si la detección precoz de LMP y la suspensión del tratamiento con MabThera pueden llevar a una estabilización similar o a una mejoría del desenlace clínico. Reacciones relacionadas con la administración/infusión: MabThera está asociado con reacciones relacionadas con la infusión/administración, que pueden vincularse con la liberación de citoquinas y/u otros mediadores químicos. El síndrome de liberación de citoquinas puede no diferenciarse clínicamente de las reacciones agudas de hipersensibilidad. Este conjunto de reacciones que incluyen los síndromes de liberación de citoquinas, y de lisis tumoral y reacciones anafilácticas e hipersensibilidad se describen a continuación. Estas no están específicamente vinculadas con la vía de administración de MabThera y pueden ser observadas con ambas formulaciones. Se han comunicado reacciones severas relacionadas con la infusión con desenlace fatal durante la etapa de poscomercialización de MabThera formulación intravenosa, con un inicio que oscila dentro de 30 minutos a 2 horas después de comenzar la primera infusión de MabThera formulación intravenosa. Estas se caracterizan por eventos pulmonares y en algunos casos incluyen lisis tumoral rápida y las características del síndrome de lisis tumoral, además de fiebre, escalofríos, rigidez, hipotensión, urticaria, angioedema y otros síntomas (véase Reacciones adversas). El síndrome de liberación de citoquinas grave se caracteriza por disnea grave, frecuentemente acompañada de broncoespasmo e hipoxia, además de fiebre, escalofríos, rigidez, urticaria y angioedema. Este síndrome puede estar relacionado con algunas características del síndrome de lisis tumoral, tales como hiperuricemia, hiperpotasemia, hipocalcemia, hiperfosfatemia, insuficiencia renal aguda, elevación de la lactato dehidrogenasa (LDH) y también con insuficiencia respiratoria aguda y muerte. La insuficiencia respiratoria aguda puede estar acompañada por eventos tales como, infiltración intersticial o edema pulmonar, visibles a la exploración radiológica torácica. El síndrome se manifiesta frecuentemente dentro de la primera o segunda hora después de iniciar la primera infusión. Los pacientes con antecedentes de insuficiencia pulmonar o con infiltración tumoral pulmonar, pueden tener un riesgo mayor de mal pronóstico y deben aumentarse las precauciones durante su tratamiento. En aquéllos que desarrollen síndrome de liberación de citoquinas grave (véase Dosificación) se debe interrumpir la infusión inmediatamente y deben recibir medicación sintomática de choque. Dado que a la mejoría inicial de los síntomas clínicos puede seguir una recidiva, se debe monitorizar estrechamente a estos pacientes hasta que el síndrome de lisis tumoral y la infiltración pulmonar se hayan resuelto o hayan sido descartados. Una vez solucionados completamente los signos y síntomas, raramente se repite el síndrome de liberación de citoquinas en tratamientos posteriores. Los pacientes con gran masa tumoral (≥ 25 x 109/l) o con un elevado número de células tumorales circulantes, como aquellos con LLC que pueden tener un riesgo mayor de desarrollar un síndrome de liberación de citoquinas muy grave, deben tratarse, extremando las precauciones durante el tratamiento. Estos pacientes deben monitorizarse muy estrechamente durante la primera infusión y en ellos se debe considerar reducir la velocidad de la primera infusión o un fraccionamiento de la dosis durante más de dos días en el primer ciclo y algún ciclo posterior si el recuento de linfocitos es aún > 25 x 109/l. Se han notificado casos de reacciones de hipersensibilidad, incluyendo anafilácticas, después de la administración intravenosa de proteínas. A diferencia del síndrome de liberación de citoquinas, los episodios verdaderos de hipersensibilidad se presentan generalmente durante los primeros minutos de la infusión. Conviene disponer para uso inmediato de medicamentos utilizados para combatirlos, es decir, adrenalina, antihistamínicos y glucocorticoides, por si ocurriera una reacción alérgica durante la administración de MabThera. Las manifestaciones clínicas de anafilaxia pueden parecerse a las del síndrome de liberación de citoquinas anteriormente descripto. Las reacciones atribuibles a la hipersensibilidad se han informado menos frecuentemente que las vinculadas con la liberación de citoquinas. Además de las reacciones mencionadas, se informaron algunos casos de infarto de miocardio, fibrilación auricular, edema pulmonar y trombocitopenia reversible aguda. Dado que se puede producir hipotensión durante la administración de MabThera, se debe considerar interrumpir los tratamientos antihipertensivos 12 horas antes de la misma. En el 77% de los pacientes tratados con MabThera formulación intravenosa se han observado reacciones adversas relacionadas con la infusión (incluyendo el síndrome de liberación de citoquinas acompañado de hipotensión y broncoespasmo en el 10% de los pacientes) (véase Reacciones adversas). Generalmente, estos síntomas son reversibles después de la interrupción de la infusión de MabThera y la administración de un antipirético, un antihistamínico y ocasionalmente oxígeno, solución salina intravenosa o broncodilatadores, y, en caso de necesidad, glucocorticoides. En los estudios clínicos se han informado reacciones relacionadas con la administración en hasta el 50% de los pacientes tratados con MabThera formulación subcutánea. Las reacciones ocurrieron dentro de las 24 horas de la inyección subcutánea y consistieron primordialmente en eritema, prurito, erupciones cutáneas y reacciones en el lugar de la inyección, tales como, dolor, inflamación y enrojecimiento, y fueron generalmente de grado leve o moderado (Grados 1 o 2) y de carácter transitorio. En pacientes que recibieron MabThera subcutáneo en los estudios clínicos, las reacciones cutáneas locales fueron muy frecuentes; se reportaron en hasta el 50% de los pacientes en algún momento durante el tratamiento. Los síntomas incluyeron dolor, inflamación, induración, hemorragia, eritema, prurito y erupciones cutáneas (véase Reacciones adversas). Algunas reacciones cutáneas locales se produjeron más de 24 horas después de la administración subcutánea de MabThera. La mayoría de las observadas después de la aplicación subcutánea fueron leves o moderadas y se resolvieron sin necesidad de tratamiento específico. Antes de comenzar con las inyecciones subcutáneas de MabThera, todos los pacientes deben recibir siempre previamente, una dosis completa de MabThera por infusión intravenosa, utilizando MabThera formulación intravenosa. El mayor riesgo de experimentar una reacción relacionada con la administración es generalmente observado en el ciclo 1. El inicio del tratamiento con MabThera formulación intravenosa permite demorar o detener la infusión intravenosa y lograr de esta manera un mejor manejo de las reacciones relacionadas con la administración. Si los pacientes no pudieron recibir una dosis completa de MabThera infusión intravenosa previa al cambio, deben continuar los ciclos posteriores con MabThera formulación intravenosa hasta que una dosis intravenosa completa sea administrada exitosamente. Por lo tanto, la sustitución por MabThera formulación subcutánea sólo puede ocurrir en el ciclo 2 o en los siguientes. En pacientes que pueden recibir la dosis completa por infusión de MabThera IV, los ciclos posteriores de MabThera pueden ser administrados subcutáneamente utilizando la formulación de MabThera SC (ver Dosificación). Como con la formulación intravenosa, MabThera formulación subcutánea debe ser administrada en un contexto en el que los equipos completos de reanimación estén inmediatamente disponibles y bajo la supervisión estricta de un profesional de la salud con experiencia. La premedicación, que incluye un analgésico/antipirético y un antihistamínico, siempre debe ser administrada antes de cada dosis de MabThera formulación subcutánea. También debe ser considerada la premedicación con glucocorticoides. Los pacientes deben ser observados durante por lo menos 15 minutos después de la administración subcutánea de MabThera. Un período más prolongado puede ser apropiado en aquéllos con un riesgo mayor de reacciones de hipersensibilidad. Se debe advertir a los pacientes que se comuniquen inmediatamente con su médico si se presentan síntomas que sugieren reacciones de hipersensibilidad severas o síndrome de liberación de citoquinas en cualquier momento después de la administración del medicamento. Eventos pulmonares: Los eventos pulmonares incluyen hipoxia, infiltración pulmonar e insuficiencia respiratoria aguda. Algunos de estos eventos han sido precedidos por broncoespasmo severo y disnea. En algunos casos, los síntomas empeoran con el tiempo, mientras que en otros la mejoría inicial fue seguida por un deterioro clínico. Por lo tanto, los pacientes que experimentaron eventos pulmonares u otros síntomas graves relacionados con la infusión deben ser estrechamente vigilados hasta que se produzca la resolución completa de sus síntomas. Los pacientes con antecedentes de insuficiencia pulmonar o con infiltración tumoral pulmonar pueden estar en mayor riesgo de mala evolución y deben ser tratados con mayor precaución. La insuficiencia respiratoria aguda puede estar acompañada de eventos tales como la infiltración intersticial pulmonar o edema, visible en una radiografía de tórax. El síndrome se manifiesta generalmente dentro de una o dos horas de iniciar la primera infusión. Los pacientes que experimentan eventos pulmonares graves deben interrumpir la administración de MabThera inmediatamente (ver Dosificación) y recibir tratamiento sintomático agresivo. Lisis tumoral rápida: MabThera media la rápida lisis de las células benignas y malignas CD20 positivas. Se ha informado que los signos y síntomas (por ejemplo, la hiperuricemia, hiperpotasemia, hipocalcemia, hiperfosfatemia, insuficiencia renal aguda, elevación de la LDH), concordantes con el síndrome de lisis tumoral (SLT) se produjeron después de la primera infusión intravenosa de MabThera en pacientes con un alto número de linfocitos malignos circulantes. Se debe considerar la profilaxis para SLT para quienes estén en riesgo de desarrollar lisis tumoral rápida (por ejemplo, los que tienen una alta carga tumoral o un número alto ( > 25 x 109 / l) de células malignas circulantes, como los pacientes con LLC y linfoma de células del manto). Estos pacientes deben ser seguidos de cerca y realizarse monitoreos de laboratorio adecuados. Debe proporcionarse una terapia médica apropiada a aquellos que desarrollan signos y síntomas compatibles con lisis tumoral rápida. Después del tratamiento y para la resolución completa de los signos y síntomas, la posterior terapia con MabThera IV se ha administrado en combinación con la profilaxis para SLT en un número limitado de casos. Trastornos cardíacos: Dado que se puede producir hipotensión durante la administración de MabThera se debe considerar la interrupción de los medicamentos antihipertensivos 12 horas antes y durante la administración de MabThera IV/SC. Se han informado casos de angina de pecho, arritmias cardíacas, tales como flutter/aleteo y fibrilación auricular, insuficiencia cardíaca y/o infarto de miocardio en pacientes tratados con MabThera. Por lo tanto, se deben monitorizar cuidadosamente a quienes tengan antecedentes de enfermedad cardíaca y/o cardiotoxicidad asociada con la quimioterapia. Toxicidad hematológica: Aunque MabThera en monoterapia no tiene efecto mielosupresor, se recomienda prudencia antes de tratar a pacientes con un recuento de neutrófilos < 1,5 x 109/l y/o plaquetas < 75 x 109/l, puesto que la experiencia clínica en esta población es limitada. La formulación intravenosa de MabThera se ha utilizado en 21 pacientes sometidos a trasplante autólogo de médula ósea y en otros grupos de riesgo con función de la médula ósea presumiblemente reducida, sin que haya inducido mielotoxicidad. Se deben realizar recuentos de sangre total en forma regular, incluyendo recuento de neutrófilos y plaquetas, durante la monoterapia con MabThera. Cuando MabThera se administra en combinación con quimioterapia, deben realizarse hemogramas completos regulares de acuerdo con la práctica médica habitual. Infecciones: Durante el tratamiento con MabThera pueden producirse infecciones graves e incluso mortales (véase Reacciones adversas). MabThera no debe ser administrado a pacientes con infecciones graves activas (por ejemplo, tuberculosis, sepsis e infecciones oportunistas, véase Contraindicaciones). El médico debe tener especial precaución cuando considere el uso de MabThera en pacientes con antecedentes de infecciones crónicas o recurrentes o en condiciones subyacentes que puedan provocar una mayor predisposición a infecciones (véase Reacciones adversas). Se han informado casos de reactivación de hepatitis B, en pacientes tratados con la formulación intravenosa de MabThera, que incluyeron casos de hepatitis fulminante con fallecimiento. La mayoría de estos pacientes habían estado expuestos también a quimioterapia citotóxica. Los informes son confusos tanto por el estado de la enfermedad subyacente como por la quimioterapia citotóxica. En todos los pacientes se debe llevar a cabo la detección del virus de la hepatitis B (VHB) antes de iniciar el tratamiento con MabThera. Al menos debe incluir HBsAg y HBcAc. Esto puede ser complementado con otros marcadores apropiados de acuerdo con las guías locales. Los pacientes con hepatitis B activa no deben ser tratados con MabThera. En aquéllos con serología positiva de hepatitis B (bien HBsAg o HBcAc), se debe consultar con un especialista en enfermedades hepáticas antes de iniciar el tratamiento y deben ser monitorizados y tratados siguiendo las normativas médicas locales para prevenir la reactivación de la hepatitis B. Se han notificado casos muy raros de Leucoencefalopatía Multifocal Progresiva (LMP), durante el uso poscomercialización de MabThera formulación intravenosa en LNH y LLC (véase Reacciones adversas). La mayoría de los pacientes había recibido MabThera en combinación con quimioterapia o como parte de un trasplante de células madre hematopoyéticas. Los médicos que tratan a pacientes con LNH o LLC deben considerar la LMP en el diagnóstico diferencial de pacientes que informaron síntomas neurológicos y la consulta con un neurólogo debe considerarse como clínicamente indicada. Inmunizaciones: En pacientes con LNH no se ha estudiado la seguridad de la inmunización con vacunas de virus vivos después de recibir tratamiento con MabThera; por tanto, no se recomiendan estas vacunas. Los pacientes tratados con MabThera pueden recibir vacunas inactivadas; sin embargo, con éstas los porcentajes de respuesta pueden ser menores. En un estudio no aleatorizado de pacientes con LNH de bajo Grado con recidivas, que recibieron la formulación intravenosa de MabThera en monoterapia cuando se comparó con el grupo control no tratado sano, el porcentaje de respuesta a la vacunación fue menor con el antígeno de recuerdo del tétanos (16% comparado con 81%), y con neoantígeno Keyhole Limpet Haemocyanin (KLH) (4% comparado con 76% cuando se determinó un incremento > de 2 en el título de anticuerpo). Esto implicó que los títulos de anticuerpos medidos antes del tratamiento frente antígenos como Streptococcus pneumoniae, gripe A, paperas, rubéola, y varicela, se mantuvieron hasta al menos 6 meses después del tratamiento con MabThera. Reacciones cutáneas: Se han notificado casos de reacciones cutáneas graves, tales como necrólisis epidérmica tóxica (Síndrome de Lyell) y Síndrome de Stevens-Johnson, algunas con desenlace mortal (véase Reacciones adversas). Si aparecen tales reacciones, el tratamiento debe suspenderse permanentemente. Efectos sobre la capacidad para conducir y utilizar máquinas: No se han realizado estudios de los efectos de MabThera sobre la capacidad para conducir y utilizar máquinas, aunque la actividad farmacológica y las reacciones adversas notificadas hasta la fecha sugieren que MabThera podría tener un efecto nulo o insignificante sobre la capacidad para conducir y utilizar máquinas. Fertilidad, embarazo y lactancia: Anticoncepción en mujeres: Durante y hasta 12 meses después del tratamiento con MabThera las mujeres en edad fértil deben usar métodos contraceptivos eficaces debido al largo tiempo de permanencia de rituximab en el organismo en pacientes con depleción de células B. Embarazo: Se sabe que las inmunoglobulinas IgG atraviesan la barrera placentaria. No se han determinado los niveles de linfocitos B en recién nacidos de madres expuestas a MabThera en ensayos clínicos. No existen datos suficientes ni controlados de los estudios en mujeres embarazadas; sin embargo, se han notificado depleción transitoria de células B y linfocitopenia en algunos niños nacidos de madres expuestas a MabThera durante el embarazo. Por estos motivos, MabThera no debe administrarse a mujeres embarazadas, a menos que el beneficio esperado supere el riesgo potencial. Similares efectos han sido observados en estudios en animales (véase Datos preclínicos sobre seguridad). En los ensayos de toxicidad llevados a cabo en monos cinomolgos, no se han hallado indicios de embriotoxicidad intrauterina. Las crías de animales nacidas de madres expuestas a MabThera presentaron una depleción de las poblaciones de linfocitos B durante el período posnatal. Las mujeres en edad fértil deben utilizar métodos anticonceptivos eficaces durante y por 12 meses después del tratamiento con MabThera. La formulación SC contiene hialuronidasa humana recombinante (rHuPH20) (ver Composición). Los estudios farmacocinéticos y toxicológicos en animales demuestran reducción en el peso fetal y aumento en el número de reabsorciones después de la inyección de rHuPH20, a niveles de exposición sistémica materna comparables a los que podrían manifestarse después de la administración en bolo accidental IV de un solo vial de la formulación MabThera SC en los seres humanos, con base en los supuestos más conservadores posibles. Además, durante el programa de desarrollo rituximab SC, se encontró un paciente con niveles mensurables de rHuPH20 en muestras de sangre tomadas después de la administración SC; sin que se observaran efectos adversos. Con el fin de reducir el riesgo potencial adicional de toxicidad embriofetal resultante de la exposición a rHuPH20, las pacientes que conciban mientras estén siendo tratadas con MabThera SC deben discontinuar el tratamiento con la formulación SC. Lactancia: Se desconoce si rituximab se excreta en la leche materna. Sin embargo, teniendo en cuenta que la IgG se elimina en la leche materna y que se ha detectado rituximab en la leche de monas en período de lactancia, las mujeres no deben amamantar a sus hijos durante el tratamiento con MabThera ni durante los 12 meses siguientes. Fertilidad: Los estudios en animales no han revelado efectos deletéreos de rituximab o hialuronidasa humana recombinante (rHuPH20) en los órganos reproductores.
Interacciones.
Actualmente existen datos limitados sobre las posibles interacciones medicamentosas con MabThera. En pacientes con LLC, la administración conjunta con MabThera no parece afectar la farmacocinética de fludarabina o ciclofosfamida. Además, no se registró ningún efecto aparente de fludarabina y ciclofosfamida sobre la farmacocinética de MabThera. La coadministración con metotrexato no modifica la farmacocinética de MabThera en los pacientes con artritis reumatoidea. Los pacientes con títulos de anticuerpos humanos antimurinos o antiquiméricos (HAMA/HACA) pueden sufrir reacciones alérgicas o de hipersensibilidad al ser tratados con otros anticuerpos monoclonales terapéuticos o de diagnóstico.
Conservación.
Los viales deben conservarse en heladera entre 2°C y 8°C. No congelar. Conservar los viales en el embalaje exterior para proteger su contenido de la luz. Para las condiciones de conservación después de abrir por primera vez, véase "Período de validez". Precauciones especiales de eliminación y otras manipulaciones: MabThera se suministra en viales monodosis, apirógenos, estériles, sin conservantes. Se deben cumplir estrictamente las siguientes instrucciones referentes al uso y a la eliminación de jeringas y otros objetos medicinales punzantes: Nunca reutilizar agujas y jeringas. Colocar todas las agujas y jeringas en un recipiente descartable para objetos punzantes. La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él se realizará de acuerdo con la normativa local. Este medicamento no debe ser utilizado después de la fecha de vencimiento indicada en el envase. Este medicamento debe ser usado exclusivamente bajo prescripción y vigilancia médica y no puede repetirse sin nueva receta médica. Mantenga los medicamentos fuera del alcance de los niños. Incompatibilidades: No se han observado incompatibilidades entre la formulación subcutánea de MabThera y el material de polipropileno o policarbonato de la jeringa, o las agujas para transferencia e inyección de acero inoxidable, y los tapones cónicos Luer de polietileno. Período de validez: Una vez transferida del vial a la jeringa, la solución de MabThera formulación subcutánea se mantiene física y químicamente estable durante 48 horas a 2°C - 8°C y, posteriormente, durante 8 horas a 30°C en luz difusa. Desde un punto de vista microbiológico, el producto debe ser utilizado de inmediato. Caso contrario, la preparación debe realizarse bajo condiciones controladas y mediante técnicas asépticas validadas. El tiempo y las condiciones de almacenamiento antes de usar son responsabilidad del usuario.
Sobredosificación.
La experiencia disponible acerca de las sobredosis de la formulación intravenosa de MabThera procedente de estudios clínicos en seres humanos es limitada. La dosis intravenosa máxima hasta la fecha es 5.000 mg (2.250 mg/m2), evaluada en seres humanos en un estudio de aumento de dosis en pacientes con leucemia linfocítica crónica. No se identificaron señales de seguridad adicionales. Los pacientes que experimenten sobredosis deberán interrumpir inmediatamente la infusión y ser monitorizados estrechamente. Se debe considerar la necesidad de un seguimiento periódico del recuento de células sanguíneas y del aumento del riesgo de infecciones mientras los pacientes estén con depleción de células B. Tres pacientes con diagnóstico de Linfoma Folicular incluidos en el estudio SABRINA (BO22334) fueron tratados inadvertidamente con la formulación SC de MabThera 1.400 mg por vía IV a una dosis máxima de rituximab de 2.780 mg, sin reacciones adversas. Los pacientes que experimentaron sobredosis o errores en la medicación con MabThera SC deben ser monitorizados cuidadosamente. Después de la comercialización, se notificaron cinco casos de sobredosis de MabThera. En tres de ellos no se registraron reacciones adversas. En los otros dos los efectos adversos fueron síntomas gripales, con una dosis de 1,8 g de rituximab e insuficiencia respiratoria mortal, con una dosis de 2 g de rituximab. Ante la eventualidad de una sobredosificación concurrir al Hospital más cercano o comunicarse con los Centros de Toxicología: Hospital de Pediatría Dr. Ricardo Gutiérrez: 4962-6666/2247; Policlínico Dr. G. A. Posadas: 4654-6648; 4658-7777; Hospital General de Niños Dr. Pedro de Elizalde: 4300-2115; 4363-2100 /2200 Interno 6217.
Presentación.
Vial con 1.600 mg/13.4 ml (120mg/ml), envase con 1.
Revisión.
Septiembre 2015. Aprobación: 17/03/2017. Disp. ANMAT N° 2.671 (EL+EMA+ ANMAT C004/13+Shpe+CDS:26.0C+CDS:27.0C.
Laboratorio que comercializa Mabthera Sc
ROCHE →

