Herceptin®
ROCHE
Trastuzumab.
Agente antineoplásico, anticuerpo monoclonal.
Composición.
Cada vial monodosis contiene 150 mg de trastuzumab, en un excipiente compuesto por clorhidrato de L-histidina 3,36 mg, L-histidina 2,16 mg, dihidrato de a, a-trehalosa 136,2 mg y polisorbato 20: 0,60 mg. Disolvente: No se suministra el agua para las preparaciones inyectables. Cada vial multidosis contiene 440 mg de trastuzumab, en un excipiente compuesto por clorhidrato de L-histidina 9,9 mg, L-histidina 6,4 mg, dihidrato de a, a-trehalosa 400,0 mg y polisorbato 20: 1,8 mg. Disolvente: Cada vial contiene agua bacteriostática para inyectables c.s.p. 20,9 ml (como disolvente) y alcohol bencílico 229,9 mg (1,1%, como conservante antimicrobiano). Herceptin 150 mg y 440 mg es un polvo liofilizado para preparar una solución concentrada administrable en infusión de color blanco a amarillo pálido. El concentrado reconstituido de Herceptin contiene 21 mg/ml de trastuzumab. El disolvente es un líquido límpido e incoloro.
Farmacología.
Código ATC: L01XC03. Grupo farmacoterapéutico: Agente antineoplásico, anticuerpo monoclonal. Propiedades farmacodinámicas: Trastuzumab es un anticuerpo monoclonal humanizado IgG1 contra el receptor 2 del factor de crecimiento epidérmico humano (HER2). La sobreexpresión de HER2 se observa en el 20% - 30% de los cánceres de mama primarios. Estudios de las tasas de positividad de HER2 en cáncer gástrico (CG), cuando se utiliza tinción inmunohistoquímica (IHQ) e hibridación in situ por fluorescencia (FISH) o hibridación in situ por colorimetría (CISH), han mostrado que existe una gran variación en la tasa de positividad de HER2, que oscila entre un 6,8% y un 34,0% para IHQ y entre un 7,1% y un 42,6% para FISH. Como se observó durante la incorporación de pacientes en el ensayo BO18255, la tasa general de HER2 positivo en cáncer gástrico avanzado fue del 15% para IHQ3+ e IHQ2+, o del 22,1% cuando se aplicó la definición más amplia de IHQ3+ o FISH+. Los ensayos indican que los pacientes con cáncer de mama, cuyos tumores sobreexpresan HER2 tienen una sobrevida libre de enfermedad más corta si se compara con aquéllos cuyos tumores no sobreexpresan HER2. El dominio extracelular del receptor (ECD, p105) puede liberarse en el torrente sanguíneo y ser medido en muestras de suero. Mecanismo de acción: Trastuzumab se une con una alta afinidad y especificidad al subdominio IV, una región yuxtamembrana del dominio extracelular de HER2. La unión del trastuzumab a HER2 inhibe la vía de señalización de HER2 independiente del ligando y previene la división proteolítica de su dominio extracelular, un mecanismo de activación de HER2. Como resultado, trastuzumab ha demostrado, tanto en ensayos in vitro como en animales, que inhibe la proliferación de células tumorales humanas que sobreexpresan HER2. Además, trastuzumab es un potente mediador de la citotoxicidad dependiente de anticuerpos mediada por células (ADCC). Se ha demostrado in vitro, que la ADCC mediada por trastuzumab se ejerce preferentemente sobre células que sobreexpresan HER2 si se compara con células cancerosas que no sobreexpresan HER2. Diagnóstico de la sobreexpresión de HER2 o de la amplificación del gen HER2: Diagnóstico de la sobreexpresión de HER2 o de la amplificación del gen HER2 en cáncer de mama: Herceptin debe ser empleado únicamente en pacientes cuyos tumores sobreexpresen la proteína HER2 o presenten amplificación del gen HER2 determinados mediante un método exacto y validado. La sobreexpresión de HER2 puede ser detectada empleando una evaluación basada en técnicas inmunohistoquímicas (IHQ) de bloques tumorales fijados (ver Precauciones) y la amplificación del gen HER2 mediante hibridación in situ por fluorescencia (FISH) o hibridación in situ por colorimetría (CISH) de bloques tumorales fijados. Los pacientes se elegirán para ser tratados con Herceptin si muestran fuerte sobreexpresión de HER2, descripta como una calificación 3+ por IHQ o como resultado positivo por FISH o CISH. Para asegurar resultados exactos y reproducibles, el test debe ser realizado en un laboratorio especializado que pueda garantizar la validación de los procedimientos de valoración. En la Tabla 1 se indica el sistema de valoración recomendado para evaluar los patrones de tinción por IHQ.
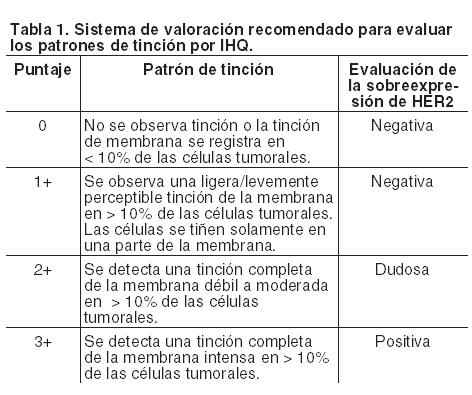
En general, el resultado se considera positivo por FISH si la relación entre el número de copias del gen HER2 por célula tumoral es mayor o igual a 2 veces el número de copias del cromosoma 17 o bien que la cantidad de copias del gen HER2 por célula tumoral sea mayor de 4 en el caso de que no se emplee el cromosoma 17 como control. Como norma general, se considera un resultado positivo por CISH si existen más de 5 copias del gen HER2 por núcleo en más del 50% de las células tumorales. Para instrucciones más completas sobre la realización de los análisis y la interpretación de los resultados consulte la información incluida en los envases de ensayos FISH y CISH que hayan sido validados. Las recomendaciones oficiales sobre la prueba de HER2 pueden ser también aplicadas. En cualquier otro método que se emplee para la evaluación de la proteína HER2 o la expresión del gen, los análisis deben ser realizados únicamente en laboratorios que puedan asegurar el uso de métodos validados y adecuados al conocimiento científico actual. Estos deberán ser suficientemente precisos y exactos para demostrar la sobreexpresión del HER2 y deben ser capaces de distinguir entre la sobreexpresión de HER2 moderada (es decir, 2+) y fuerte (3+). Diagnóstico de la sobreexpresión de HER2 o de la amplificación del gen HER2 en cáncer gástrico: Sólo se deberá usar un método exacto y validado para determinar la sobreexpresión de HER2 o la amplificación del gen HER2. Se recomienda el test IHQ como primera opción y en el caso de que también se requiera conocer el status de la amplificación del gen HER2, se debe emplear hibridación in situ con plata (SISH) o FISH. Sin embargo, para poder evaluar en paralelo la histología y la morfología del tumor se recomienda utilizar la técnica SISH. Para asegurar los procedimientos de validación del test y la obtención de resultados exactos y reproducibles, el test debe realizarse en un laboratorio con personal entrenado para ello. Para instrucciones más completas sobre la realización de los ensayos y la interpretación de los resultados, consulte la información incluida en las pruebas para determinar HER2. En el ensayo BO18255 (ToGA), los pacientes con tumores IHQ3+ o FISH positivos fueron definidos como HER2 positivos, y por lo tanto, fueron incluidos en el mismo. Según los resultados de ensayos clínicos, los efectos beneficiosos se limitaron a los pacientes con el nivel más alto de la sobreexpresión de la proteína HER2, considerada como una calificación 3+ por IHQ, ó 2+ por IHQ y con un resultado de FISH positivo. En un estudio comparativo (D008548) se observó un alto grado de concordancia ( > 95%) entre las técnicas SISH y FISH para la detección de la amplificación del gen HER2 en pacientes con cáncer gástrico. La sobreexpresión de HER2 debe ser detectada empleando una evaluación basada en técnicas inmunohistoquímicas (IHQ) de bloques tumorales fijados y la amplificación del gen HER2 mediante hibridación in situ usando SISH o FISH de bloques tumorales fijados. En la Tabla 2 se indica el sistema de valoración recomendado para evaluar los patrones de tinción por IHQ.
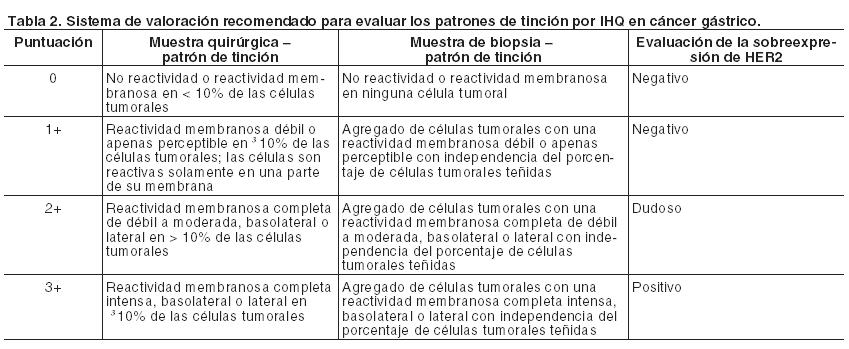
En general, el resultado se considera positivo por SISH o FISH si la relación del número de copias del gen HER2 por célula tumoral es mayor o igual a 2 veces la cantidad de copias del cromosoma 17. Eficacia clínica y seguridad: Cáncer de Mama Metastásico (CMM): Formulación intravenosa: Se ha empleado Herceptin i.v. como monoterapia en ensayos clínicos con pacientes con cáncer de mama metastásico cuyos tumores sobreexpresaban HER2 después del fracaso de uno o más regímenes quimioterápicos para su enfermedad metastásica (Herceptin i.v. solo). También se utilizó Herceptin i.v. en ensayos clínicos en combinación con paclitaxel o docetaxel en pacientes que no habían recibido quimioterapia para su enfermedad metastásica. Aquéllos con terapia adyuvante previa con antraciclinas fueron tratados con paclitaxel (175 mg/m2 infundido en 3 horas) con o sin Herceptin i.v. En el estudio pivotal de docetaxel (100 mg/m2 infundido en 1 hora) con o sin Herceptin i.v., el 60% de los pacientes había recibido terapia adyuvante previa con antraciclinas. Herceptin i.v. se administró hasta la progresión de la enfermedad. No se estudió la eficacia de Herceptin i.v. en combinación con paclitaxel en pacientes que no habían recibido tratamiento adyuvante previo con antraciclinas. Sin embargo, la asociación de Herceptin i.v. más docetaxel fue eficaz en los pacientes, independientemente de que hubieran recibido o no terapia adyuvante previa con antraciclinas. La técnica para evaluar la sobreexpresión del HER2 empleada para determinar la elegibilidad de los pacientes en los ensayos clínicos pivotales de monoterapia con Herceptin y de Herceptin más paclitaxel fue por tinción inmunohistoquímica de HER2 de material fijado de tumores de mama empleando los anticuerpos monoclonales murinos CB11 y 4D5. Los tejidos se fijaron en formalina o fijador de Bouin. Este ensayo clínico de investigación llevado a cabo en un laboratorio central empleaba una escala de 0 a 3+. Se incluyeron los pacientes clasificados con tinción 2+ o 3+ mientras que se excluyeron aquellos con 0 ó 1+. Más del 70% de los incorporados tenían sobreexpresión 3+. Los datos sugieren que los efectos beneficiosos fueron superiores entre los pacientes con mayores niveles de sobreexpresión de HER2 (3+). La principal técnica utilizada para determinar la positividad de HER2 en los estudios pivotales con docetaxel, con o sin Herceptin i.v., fue la inmunohistoquímica. Una minoría de los pacientes fue evaluada mediante hibridación in situ por fluorescencia (FISH). En este estudio, el 87% de los pacientes incluidos era IHQ3+ y el 95% IHQ3+ y/o FISH positivo. Dosificación semanal para Cáncer de Mama Metastásico: Los resultados de eficacia provenientes de los estudios con monoterapia y en combinación se resumen en la Tabla 3:
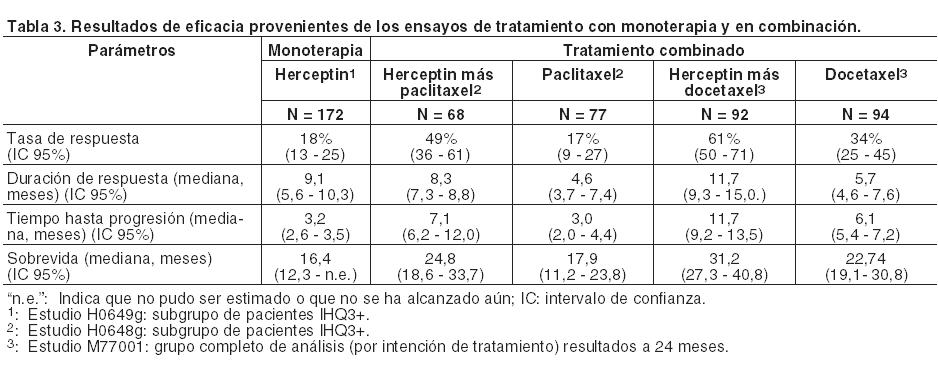
Tratamiento combinado de Herceptin i.v. y anastrozol: Herceptin ha sido estudiado en combinación con anastrozol como tratamiento de primera línea en pacientes con cáncer de mama metastásico, que sobreexpresan HER2 y con receptor hormonal positivo (es decir, para el receptor de estrógenos [RE] y/o el receptor de progesterona [RP] en pacientes posmenopáusicas). La sobrevida libre de progresión se duplicó en el grupo de Herceptin i.v. y anastrozol comparado con el grupo de anastrozol (4,8 meses comparados con 2,4 meses). En el resto de los parámetros las mejorías observadas para la asociación se manifestaron en la respuesta global (16,5% comparado con 6,7%); en beneficio clínico (42,7 comparado con 27,9%) y en tiempo hasta progresión (4,8 meses comparado con 2,4 meses). No se ha registrado ninguna diferencia en el tiempo hasta respuesta y en la duración de ésta, entre ambos grupos. La mediana de sobrevida global aumentó en 4,6 meses para los pacientes tratados con la combinación. Esta diferencia no fue estadísticamente significativa; sin embargo, más de la mitad de los pacientes que pertenecían al grupo que sólo recibía anastrozol pasaron al tratamiento que contenía Herceptin i.v. ante la progresión de la enfermedad. Dosificación cada 3 semanas para Cáncer de Mama Metastásico: Los resultados de eficacia procedentes de los estudios no comparativos con monoterapia y en combinación se resumen en la Tabla 4:
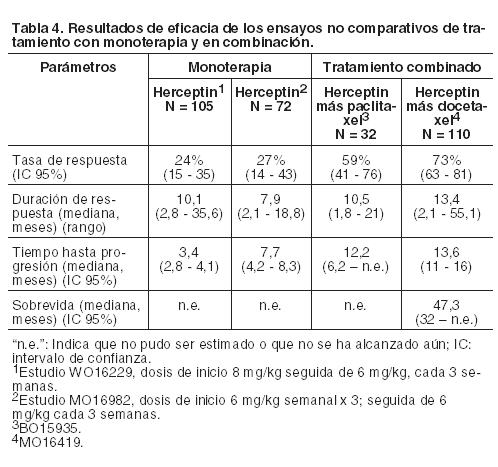
Localizaciones de progresión: La frecuencia de la progresión en el hígado se redujo significativamente en pacientes tratados con Herceptin i.v. en combinación con paclitaxel en comparación con paclitaxel solo (21,8% frente a 45,7%; p = 0,004). Mayor cantidad de pacientes tratados con Herceptin i.v. y paclitaxel progresaron en el sistema nervioso central que aquéllos que recibieron paclitaxel solo (12,6% comparado con 6,5%; p = 0,377). Cáncer de Mama Precoz - Tratamiento adyuvante: Formulación intravenosa: El cáncer de mama precoz se define como carcinoma invasivo, primario, no metastásico de mama. Para adyuvancia, Herceptin i.v. se ha investigado en 4 grandes ensayos multicéntricos, aleatorizados: El ensayo BO16348 fue diseñado para comparar uno y dos años de tratamiento de Herceptin i.v. cada tres semanas en comparación con observación, en pacientes con cáncer de mama precoz HER2 positivo después de cirugía, quimioterapia establecida y radioterapia (si correspondía). Además, se realizó una comparación entre el tratamiento con Herceptin i.v. de un año frente a dos años. A los pacientes asignados a Herceptin i.v. se les administró una dosis de inicio de 8 mg/kg, seguida de 6 mg/kg cada tres semanas durante uno o dos años. Los ensayos NSAPB B-31 y NCCTG N9831, que comprenden un análisis conjunto, fueron diseñados para investigar la utilidad clínica de la combinación del tratamiento de Herceptin i.v. con paclitaxel después de la quimioterapia AC. Además, en el ensayo NCCTG N9831 también se evaluó la adición secuencial de Herceptin i.v. a quimioterapia AC→P en pacientes con cáncer de mama precoz HER2 positivo después de cirugía. El ensayo BCIRG 006 fue diseñado para investigar la combinación del tratamiento de Herceptin con docetaxel tanto después de la quimioterapia AC como asociado con docetaxel y carboplatino en pacientes con cáncer de mama precoz HER2 positivo después de cirugía. El ensayo BO16348 (HERA) sobre cáncer de mama precoz se limitó a adenocarcinoma de mama invasivo, primario, operable, con ganglios axilares positivos o ganglios axilares negativos, si los tumores eran por lo menos de 1 cm de diámetro. En el análisis conjunto de los ensayos NSAPB B-31 y NCCTG N9831, el cáncer de mama precoz se restringió a mujeres con cáncer de mama operable de alto riesgo, definido como HER2 positivo y ganglio linfático axilar positivo o HER2 positivo y ganglio linfático negativo con características de alto riesgo (tamaño del tumor > 1 cm y RE negativo o tamaño del tumor > 2 cm, independientemente del estado de receptor hormonal). En el estudio BCIRG 006 HER2 positivo, el cáncer de mama precoz se limitó a pacientes con ganglio linfático positivo o a aquéllos con ganglio negativo de alto riesgo (sin compromiso de ganglio linfático [pN0], y al menos 1 de los siguientes factores: tamaño de tumor mayor de 2 cm, receptor negativo de estrógeno y progesterona, grado histológico y/o nuclear 2 - 3, o edad < 35 años). Los resultados de eficacia del ensayo BO16348 después de una mediana de seguimiento de 12 meses* y 8 años** están resumidos en la Tabla 5:
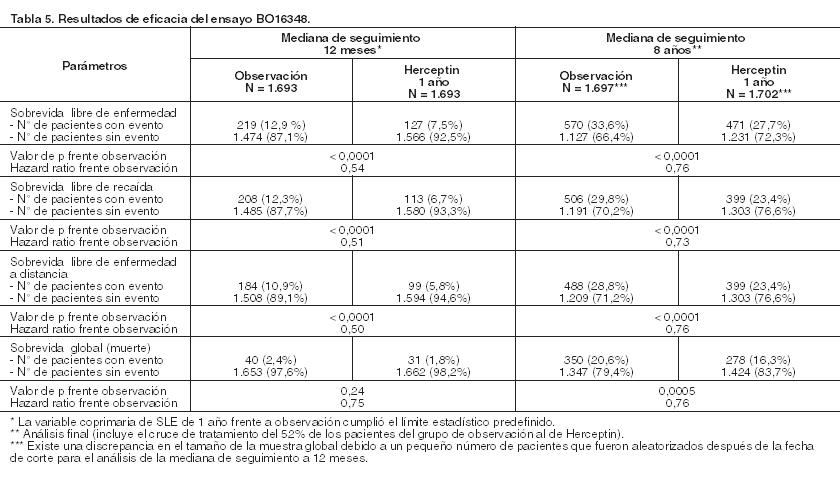
Los resultados del análisis intermedio de eficacia cruzaron el límite estadístico preespecificado para la comparación de 1 año de Herceptin i.v. frente a observación. Después de una mediana de seguimiento de 12 meses, el hazard ratio (HR) para la sobrevida libre de enfermedad (SLE) fue de 0,54% (IC del 95%: 0,44 - 0,67), lo cual expresado en beneficio absoluto, en términos de SLE a 2 años, es de 7,6 puntos porcentuales (85,8% frente a 78,2%) a favor del grupo de Herceptin. El análisis final se realizó después de una mediana de seguimiento de 8 años, y mostró que 1 año de tratamiento con Herceptin i.v. está asociado con una reducción del riesgo del 24% comparada con observación solo (HR = 0,76, IC del 95%: 0,67 - 0,86). Esto se traduce en un beneficio absoluto en términos de una tasa de sobrevida libre de enfermedad a 8 años de 6,4 puntos porcentuales a favor de 1 año de tratamiento con Herceptin i.v. En este análisis final, la prolongación del tratamiento con Herceptin i.v. a una duración de dos años no mostró beneficio adicional sobre la terapia de 1 año [HR de SLE en la población por intención de tratar (ITT) de 2 años frente a 1 año = 0,99 (IC del 95%: 0,87 - 1,13), valor de p = 0,90 y HR de SG = 0,98 (0,83 - 1,15); valor de p = 0,78]. La tasa de disfunción cardíaca asintomática se incrementó en el grupo de 2 años (8,1% frente a 4,6% en el grupo de 1 año). Más pacientes experimentaron al menos un evento adverso de Grado 3 ó 4 en el grupo de 2 años de tratamiento (20,4%) comparado con el grupo de 1 año (16,3%). En los ensayos NSAPB B-31 y NCCTG N9831 Herceptin i.v. fue administrado en combinación con paclitaxel, después de quimioterapia AC. Doxorrubicina y ciclofosfamida fueron administrados concomitantemente de la siguiente forma: Doxorrubicina por bolo intravenoso, 60 mg/m2 administrado cada 3 semanas durante 4 ciclos. Ciclofosfamida intravenoso, 600 mg/m2 administrado en 30 minutos, cada 3 semanas durante 4 ciclos. Paclitaxel en combinación con Herceptin i.v., se administró de la siguiente manera: Paclitaxel intravenoso - 80 mg/m2 como infusión intravenosa continua, administrada cada semana durante 12 semanas. O Paclitaxel intravenoso - 175 mg/m2 como infusión intravenosa continua, administrada cada 3 semanas durante 4 ciclos (día 1 de cada ciclo). Los resultados de eficacia del análisis conjunto de los estudios NSAPB B-31 y NCCTG N9831 en el momento del análisis definitivo de SLE* están resumidos en la Tabla 6. La mediana de duración del seguimiento fue de 1,8 años para los pacientes del grupo AC→P y de 2,0 años para aquéllos del grupo AC→PH.
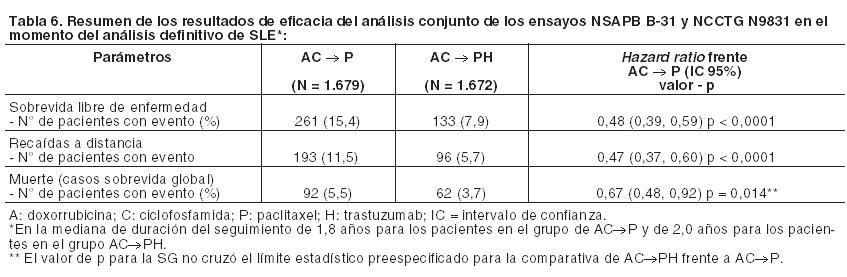
Para la variable primaria, sobrevida libre de enfermedad, la adición de Herceptin i.v. a paclitaxel dio lugar a un descenso del 52% del riesgo de recaídas de la enfermedad. El hazard ratio se traduce en un beneficio absoluto, en términos de tasa de SLE a 3 años, de 11,8 puntos porcentuales (87,2% frente a 75,4%) en el grupo AC→PH (Herceptin i.v.). En el momento de la actualización de los datos de seguridad después de una mediana de 3,5 a 3,8 años de seguimiento, una investigación de la sobrevida libre de enfermedad reconfirma la magnitud del beneficio mostrado en el análisis definitivo de este parámetro. A pesar del cruce a Herceptin i.v. en el grupo control, la adición de Herceptin i.v. a la quimioterapia con paclitaxel causó una disminución del 52% en el riesgo de recurrencia de la enfermedad. El agregado de Herceptin i.v. a la quimioterapia con paclitaxel también generó una reducción del 37% en el riesgo de muerte. El resultado final planificado anticipadamente de SG del análisis conjunto de los estudios NSAPB B-31 y NCCTG N9831 se realizó cuando habían ocurrido 707 muertes (mediana de seguimiento de 8,3 años en el grupo AC→PH). El tratamiento con AC→PH originó una mejora estadísticamente significativa en SG comparada con AC→P (HR estratificado = 0,64; IC del 95%: [0,55, 0,74]; valor de p log-rank < 0,0001). A los 8 años, se estimó una tasa de sobrevida de 86,9% en el grupo AC→PH y de 79,4% en el grupo AC→P, con un beneficio absoluto de 7,4% (IC del 95%: 4,9%, 10,0%). Los resultados finales de SG del análisis conjunto de los estudios NSAPB B-31 y NCCTG N9831 se resumen en la Tabla 7.
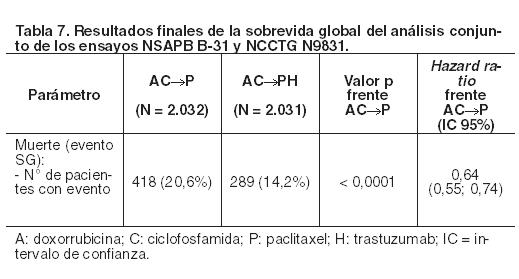
Se investigó también la sobrevida libre de enfermedad (SLE) en el resultado final de SG del análisis conjunto de los ensayos NSAPB B-31 y NCCTG N9831. Los resultados de la SLE actualizados (HR estratificado = 0,61; IC del 95% [0,54, 0,69]) mostraron un beneficio de SLE similar al del análisis de sobrevida libre de enfermedad primario definitivo, a pesar de que el 24,8% de los pacientes en el grupo AC→P pasaron a recibir Herceptin i.v. A los 8 años, se estimó una tasa de SLE del 77,2% (IC del 95%: 75,4, 79,1) en el grupo de AC→PH, con un beneficio absoluto del 11,8% comparado con el grupo AC→P. En el ensayo BCIRG 006, Herceptin fue administrado tanto en combinación con docetaxel, después de la quimioterapia (AC→DH) como asociado con docetaxel y carboplatino (DCarbH). Docetaxel fue administrado de la siguiente forma: Docetaxel intravenoso - 100 mg/m2 como infusión intravenosa durante 1 hora, administrado cada 3 semanas durante 4 ciclos (día 2 del primer ciclo de docetaxel, a continuación día 1 de cada ciclo posterior).o Docetaxel intravenoso - 75 mg/m2 como infusión intravenosa durante 1 hora, administrado cada 3 semanas durante 6 ciclos (día 2 del ciclo 1, a continuación día 1 de cada ciclo posterior), que fue seguido de: Carboplatino - ABC = 6 mg/ml/min administrado como infusión intravenosa durante 30 - 60 minutos repetido cada 3 semanas durante un total de 6 ciclos. Herceptin fue administrado semanalmente con quimioterapia y después cada 3 semanas durante un total de 52 semanas. Los resultados de eficacia procedentes de BCIRG 006 están resumidos en las Tablas 8 y 9. La mediana de duración del seguimiento fue de 2,9 años en el grupo de AC→D y de 3,0 años en cada uno de los grupos AC→DH y DCarbH.
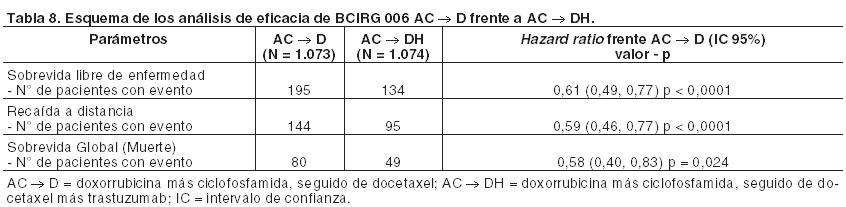
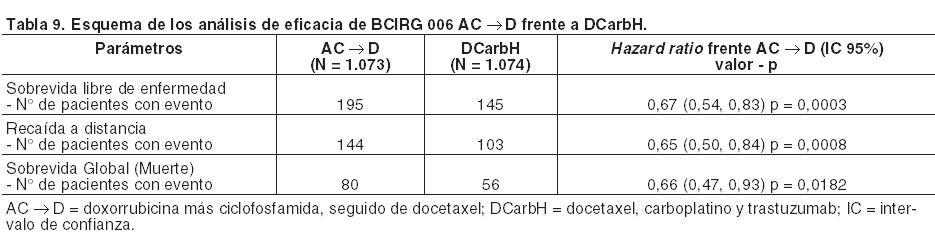
En el ensayo BCIRG 006 para el objetivo primario, sobrevida libre de enfermedad, el hazard ratio se traduce en un beneficio absoluto, en términos de tasa de SLE a 3 años, de 5,8 puntos porcentuales (86,7% frente a 80,9%) en el grupo AC→DH (Herceptin i.v.) y de 4,6 puntos porcentuales (85,5% frente a 80,9%) en el grupo de DCarbH (Herceptin i.v.) comparado con AC→D. En el ensayo BCIRG 006, 213/1.075 pacientes en el grupo DCarbH (TCH), 221/1.074 pacientes en el grupo AC→DH (AC→TH) y 217/1.073 en el grupo AC→D (AC→T) tuvieron un status en la escala de Karnofsky de ≤ 90 (bien 80 ó 90). No se observó beneficio en la sobrevida libre de enfermedad en este subgrupo de pacientes (hazard ratio = 1,16, IC del 95% [0,73 - 1,83]) para DCarbH (TCH) frente a AC→D (AC→T); (hazard ratio = 0,97, IC del 95% [0,60 - 1,55] para AC→DH (AC→TH) frente a AC→D). Además, se llevó a cabo un examen exploratorio post-hoc de los datos del análisis conjunto (AC) de los ensayos clínicos NSABP B31/NCCTG N9831* y BCIRG 006 combinando los eventos de sobrevida libre de enfermedad y los eventos cardíacos sintomáticos y se resume en la Tabla 10.

Cáncer de Mama Precoz - Tratamiento neoadyuvante-adyuvante: Formulación intravenosa: Hasta el momento, no existen datos disponibles que comparen la eficacia de Herceptin i.v. administrado con quimioterapia en el tratamiento adyuvante con la obtenida en el tratamiento neoadyuvante/adyuvante. Para el tratamiento neoadyuvante-adyuvante, se realizó el ensayo MO16432, multicéntrico, aleatorizado, que fue diseñado para investigar la eficacia clínica de la administración simultánea de Herceptin i.v. con quimioterapia neoadyuvante, que incluye antraciclinas y taxanos, seguido de Herceptin i.v. en adyuvancia, hasta una duración total de 1 año de tratamiento. En el ensayo se incorporó a pacientes con un diagnóstico reciente de cáncer de mama localmente avanzado (estadio III) o cáncer de mama precoz inflamatorio. Los pacientes con tumores HER2+ se aleatorizaron para recibir quimioterapia neoadyuvante simultáneamente con Herceptin i.v. neoadyuvante-adyuvante o quimioterapia neoadyuvante sola. En el ensayo MO16432, se administró Herceptin i.v. (8 mg/kg de dosis de inicio, seguido de 6 mg/kg de mantenimiento cada 3 semanas) simultáneamente con 10 ciclos de quimioterapia neoadyuvante de la siguiente manera: Doxorrubicina 60 mg/m2 y paclitaxel 150 mg/m2, administrado cada 3 semanas durante 3 ciclos, seguido de: Paclitaxel 175 mg/m2 administrado cada 3 semanas durante 4 ciclos, seguido de: CMF el 1° y 8° día cada 4 semanas durante 3 ciclos, el cual fue seguido después de cirugía de: Ciclos adicionales de Herceptin i.v. en adyuvancia (hasta completar 1 año de tratamiento). Los resultados de eficacia del ensayo MO16432 se resumen en la Tabla 11. La duración mediana del seguimiento en el grupo de Herceptin i.v. fue de 3,8 años.
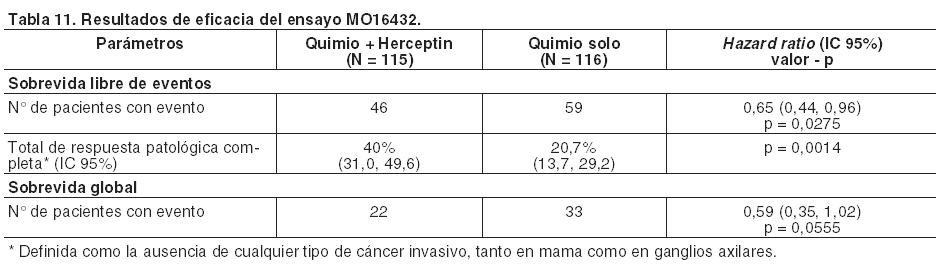
Se estimó un beneficio absoluto de 13 puntos porcentuales a favor del grupo de Herceptin i.v. en términos de sobrevida libre de eventos a los tres años (65% frente a 52%). Cáncer gástrico metastásico (CGM): Herceptin se ha estudiado en el ensayo BO18255 (ToGA) de Fase III, aleatorizado, abierto, en combinación con quimioterapia frente a quimioterapia sola. La quimioterapia se administró de la siguiente manera: Capecitabina - 1.000 mg/m2 diarios, por vía oral, 2 veces por día durante 14 días, cada 3 semanas durante 6 ciclos (desde la noche del día 1 a la mañana del día 15 de cada ciclo). O 5-fluorouracilo intravenoso - 800 mg/m2 por día, en infusión intravenosa continua durante 5 días, cada 3 semanas durante 6 ciclos (del día 1 al día 5 de cada ciclo). Cualquiera de los tratamientos anteriores se administró junto con: Cisplatino - 80 mg/m2 cada 3 semanas durante 6 ciclos el primer día de cada ciclo. Los resultados de eficacia del ensayo BO18255, se resumen en la Tabla 12:
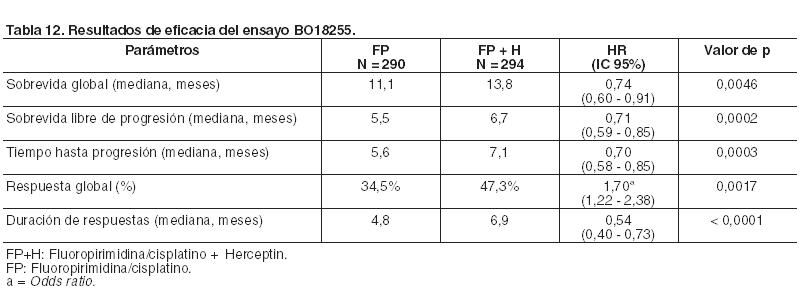
Los pacientes que fueron incorporados en el ensayo, que no habían sido tratados previamente para el adenocarcinoma de estómago o unión gastroesofágica HER2 positivo, localmente avanzado o recurrente y/o metastásico e inoperable, no eran susceptibles de tratamiento curativo. La variable principal de eficacia fue la sobrevida global, definida como el tiempo desde la fecha de distribución al azar hasta la fecha de fallecimiento, por cualquier causa. En el momento del análisis, un total de 349 pacientes aleatorizados habían fallecido: 182 (62,8%) en el grupo control y 167 (56,8%) en el grupo de tratamiento. La mayoría de los decesos fueron debidos a eventos relacionados con el cáncer subyacente. Análisis posteriores por subgrupos indican que el efecto positivo del tratamiento está limitado a aquellos tumores con mayores niveles de proteína HER2 (IHQ 2+/FISH+ e IHQ 3+). La mediana de sobrevida global para el grupo con alta expresión de HER2 fue de 11,8 meses comparado con 16 meses (hazard ratio = 0,65, IC 95% [0,51 - 0,83]) y la mediana de sobrevida libre de progresión fue de 5,5 meses comparado con 7,6 meses (hazard ratio = 0,64, IC 95% [0,51 - 0,79]) para FP comparado con FP+H, respectivamente. Para la sobrevida global, el hazard ratio fue de 0,75, IC 95% [0,51 - 1,11]) en el grupo de IHQ2+/FISH+ y de 0,58, IC 95% [0,41 - 0,81] en el grupo de IHQ3+/FISH+. En un examen exploratorio por subgrupos llevado a cabo en el ensayo BO18255 (ToGA) no se observó un beneficio aparente en la sobrevida global con la adición de Herceptin i.v. en pacientes con ECOG PS 2 en el estado basal (hazard ratio = 0,96, IC 95% [0,51 - 1,79]), con enfermedad no medible [hazard ratio = 1,78, IC 95% [0,87 - 3,66]) y con enfermedad localmente avanzada [hazard ratio = 1,20, IC 95% [0,29 - 4,97]). Inmunogenicidad: Se evaluó la producción de anticuerpos en 903 pacientes tratados con Herceptin i.v., solo o en combinación con quimioterapia. En un paciente, se detectaron anticuerpos humanos anti-trastuzumab, sin que tuviera manifestaciones alérgicas. No existen datos disponibles de inmunogenicidad para Herceptin i.v. en cáncer gástrico. Pacientes pediátricos: La Agencia Europea de Medicamentos ha eximido al titular de la obligación de presentar resultados de ensayos realizados con Herceptin i.v. en los diferentes grupos de población pediátrica en cáncer de mama y cáncer gástrico (ver Dosificación, Pacientes pediátricos). Propiedades farmacocinéticas: Formulación intravenosa: La farmacocinética de trastuzumab se evaluó en un modelo de análisis farmacocinético poblacional utilizando datos agrupados de 1.582 sujetos que recibieron Herceptin i.v. en 18 ensayos clínicos de Fases I, II y III. Un modelo de dos compartimientos de eliminación paralela lineal y no lineal desde el compartimiento central describió el perfil concentración-tiempo de trastuzumab. Debido a la eliminación no lineal, el clearance total se incrementó con concentraciones decrecientes. El clearance lineal fue de 0,127 litro/día para el cáncer de mama (cáncer de mama metastásico y cáncer de mama precoz) y de 0,176 litro/día para el cáncer gástrico metastásico. Los valores de los parámetros de eliminación no lineales fueron de 8,81 mg/día para la tasa de eliminación máxima (Vmáx) y de 8,92 mg/litro para la constante de Michaelis-Menten (Km). El volumen del compartimiento central fue de 2,62 litros para los pacientes con cáncer de mama y de 3,63 litros para aquéllos con cáncer gástrico metastásico. Los valores de las exposiciones farmacocinéticas (con 5 - 95 percentiles) y los parámetros farmacocinéticos de población pronosticados a concentraciones clínicamente relevantes (Cmáx y Cmín) para los pacientes con cáncer de mama y cáncer gástrico metastásico tratados con los regímenes posológicos aprobados de cada 3 semanas y cada semana, se muestran en la Tabla 13 (ciclo 1) y en la Tabla 14 (en estado estacionario).
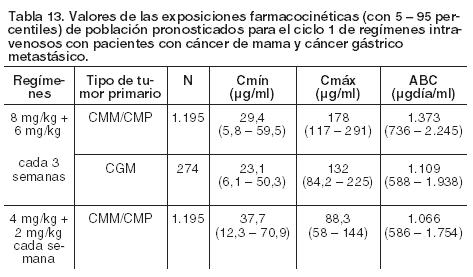
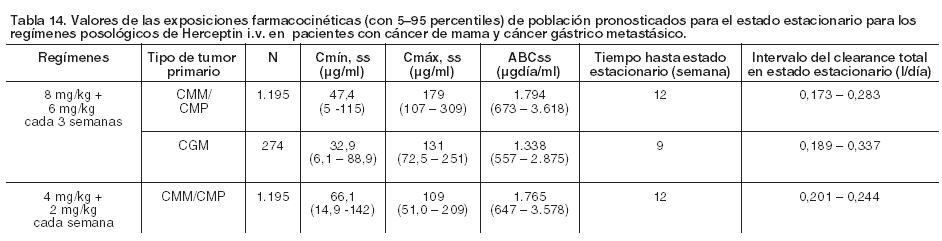
Lavado de trastuzumab: El período de tiempo de lavado de trastuzumab se evaluó después de la administración intravenosa y subcutánea utilizando los respectivos modelos farmacocinéticos de población. Los resultados de estas simulaciones indican que por lo menos el 95% de los pacientes alcanzarán concentraciones que son < 1 mg/ml (aproximadamente 3% de la Cmín, ss, predicha para la población, o alrededor del 97% de lavado) a los siete meses después de la última dosis. Farmacocinética en poblaciones especiales: Pacientes con insuficiencia renal: No se han llevado a cabo estudios farmacocinéticos detallados en pacientes con insuficiencia renal. En un análisis farmacocinético de la población, la insuficiencia renal demostró no afectar la disposición de trastuzumab. Datos preclínicos sobre seguridad: Formulación intravenosa: No existió evidencia de toxicidad aguda o relacionada con dosis múltiples en estudios de hasta 6 meses, o en toxicidad reproductiva en teratología, fertilidad en hembras o en ensayos de toxicidad gestacional tardía/transferencia placentaria. Herceptin i.v. no es genotóxico. Un estudio de trehalosa, un excipiente principal de la formulación, no reveló ninguna toxicidad. No se han llevado a cabo estudios a largo plazo en animales para establecer el potencial carcinogénico de Herceptin i.v. o para determinar sus efectos sobre la fertilidad en machos.
Indicaciones.
Cáncer de Mama: Cáncer de Mama Metastásico (CMM): Herceptin está indicado para el tratamiento de pacientes adultos con cáncer de mama metastásico (CMM) HER2 positivo: Como monoterapia para el tratamiento de aquellos pacientes que hayan recibido por lo menos dos regímenes quimioterápicos para su enfermedad metastásica. La quimioterapia previa debe haber incluido por lo menos una antraciclina y un taxano, excepto que estos tratamientos no estén indicados en los pacientes. Los pacientes con receptores hormonales positivos también deben haber fracasado al tratamiento hormonal, excepto que éste no esté indicado. En combinación con paclitaxel para el tratamiento de aquellos pacientes que no hayan recibido quimioterapia para su enfermedad metastásica y en los cuales no esté indicado un tratamiento con antraciclinas. En combinación con docetaxel para el tratamiento de aquellos pacientes que no hayan recibido quimioterapia para su enfermedad metastásica. En combinación con un inhibidor de la aromatasa para el tratamiento de pacientes posmenopáusicas con cáncer de mama metastásico y receptor hormonal positivo, que no hayan sido previamente tratadas con trastuzumab. Cáncer de Mama Precoz (CMP): Herceptin está indicado para el tratamiento de pacientes adultos con cáncer de mama precoz (CMP) HER2 positivo: Después de cirugía, quimioterapia (adyuvante o neoadyuvante) y radioterapia (si corresponde) (ver Farmacología, Propiedades farmacodinámicas). Después de quimioterapia adyuvante con doxorrubicina y ciclofosfamida, en combinación con paclitaxel o docetaxel. En combinación con quimioterapia adyuvante consistente en docetaxel y carboplatino. En combinación con quimioterapia neoadyuvante seguido de tratamiento en adyuvancia con Herceptin para enfermedad localmente avanzada (incluyendo enfermedad inflamatoria) o tumores > 2 cm de diámetro (véanse Precauciones y Farmacología, Propiedades farmacodinámicas). Herceptin debe emplearse únicamente en pacientes con cáncer de mama metastásico o cáncer de mama precoz, cuyos tumores sobreexpresen HER2 o tengan amplificación del gen HER2 determinados mediante un método exacto y validado (véanse Precauciones y Farmacología, Propiedades farmacodinámicas). Cáncer gástrico metastásico (CGM): Herceptin en combinación con capecitabina o 5-fluorouracilo y cisplatino, está indicado para el tratamiento de pacientes adultos con adenocarcinoma gástrico o unión gastroesofágica metastásico, HER2 positivo, que no hayan recibido un tratamiento previo para las metástasis. Herceptin debe emplearse únicamente en pacientes con cáncer gástrico metastásico, cuyos tumores sobreexpresen HER2, definido por IHQ2+ y confirmado por un resultado SISH o FISH o por un resultado IHQ3+. Se debe emplear un método exacto y validado (ver Precauciones y Farmacología, Propiedades farmacodinámicas).
Dosificación.
Es obligatorio realizar el test para estudiar el HER2 antes de iniciar la terapia (ver Precauciones y Farmacología, Propiedades farmacodinámicas). El tratamiento con Herceptin i.v. únicamente debe iniciarse por un especialista con experiencia en la administración de quimioterapia citotóxica (ver Precauciones), y debe ser administrado solamente por un profesional de la salud. El reemplazo por cualquier otro agente biológico requiere el consentimiento del médico prescriptor. Se debe tener precaución cuando no se cuente con datos disponibles del cambio que avalen la intercambiabilidad entre Herceptin i.v. y un biosimilar administrado. Es importante revisar el Prospecto Información para Profesionales del producto para asegurar que se está administrando la formulación correcta (Herceptin i.v. o Herceptin s.c.) al paciente, según se prescribió. La formulación de Herceptin intravenoso no está prevista para la administración subcutánea y se debe emplear solamente por vía intravenosa. El cambio de tratamiento entre las formulaciones de Herceptin intravenoso y Herceptin subcutáneo y viceversa, utilizando un régimen posológico cada tres semanas, se investigó en el ensayo clínico MO22982 (ver Reacciones adversas). Para evitar errores de medicación, es importante leer atentamente las etiquetas de los viales para asegurarse de que el medicamento que se está preparando y administrando es Herceptin (trastuzumab) y no Kadcyla (trastuzumab emtansina). Posología: Cáncer de Mama Metastásico (CMM): Pauta cada tres semanas: La dosis de inicio recomendada de Herceptin i.v. es de 8 mg/kg de peso. La dosis de mantenimiento recomendada es de 6 mg/kg de peso cada tres semanas, comenzando tres semanas después de la dosis de inicio. Pauta semanal: La dosis de inicio recomendada de Herceptin i.v. es de 4 mg/kg de peso. La dosis semanal de mantenimiento recomendada de Herceptin i.v. es de 2 mg/kg de peso, comenzando una semana después de la dosis de inicio. Administración en combinación con paclitaxel o docetaxel: En los estudios pivotales (H0648g, M77001), el paclitaxel o el docetaxel fueron administrados el día siguiente después de la dosis de inicio de Herceptin i.v. (para información acerca de las dosis, véase el Prospecto Información para Profesionales de paclitaxel o docetaxel), e inmediatamente después de las dosis siguientes de Herceptin i.v., si la dosis precedente de Herceptin i.v. fue bien tolerada. Administración en combinación con un inhibidor de la aromatasa: En el ensayo pivotal (BO16216) se administró Herceptin i.v. junto con anastrozol desde el día 1. No hubo restricciones acerca de cómo administrar en el tiempo Herceptin i.v. y anastrozol (para información acerca de la dosis, véase el Prospecto Información para Profesionales de anastrozol o de otros inhibidores de la aromatasa). Cáncer de Mama Precoz (CMP): Pauta semanal y cada 3 semanas: En la pauta cada 3 semanas la dosis de inicio recomendada de Herceptin i.v. es de 8 mg/kg de peso. La dosis de mantenimiento recomendada de Herceptin es de 6 mg/kg de peso cada 3 semanas, comenzando 3 semanas después de la dosis de inicio. En la pauta semanal se debe administrar una dosis inicial de 4 mg/kg seguida de 2 mg/kg cada semana, en forma concomitante con paclitaxel después de quimioterapia con doxorrubicina y ciclofosfamida. Para tratamiento en combinación con quimioterapia, véase Farmacología, Propiedades farmacodinámicas. Cáncer Gástrico Metastásico (CGM): Pauta cada 3 semanas: La dosis de inicio recomendada es de 8 mg/kg de peso. La dosis de mantenimiento recomendada es de 6 mg/kg de peso cada 3 semanas, comenzando 3 semanas después de la dosis de inicio. Duración del tratamiento: Cáncer de Mama Metastásico (CMM), Cáncer de Mama Precoz (CMP) y Cáncer Gástrico Metastásico (CGM): Los pacientes con cáncer de mama metastásico (CMM) o cáncer gástrico metastásico (CGM) deben recibir tratamiento con Herceptin i.v. hasta progresión de la enfermedad. Aquéllos con cáncer de mama precoz (CMP) deben ser tratados con Herceptin i.v. durante 1 año (18 ciclos cada 3 semanas) o hasta recaída de la enfermedad, lo que ocurra primero; no se recomienda prolongar el tratamiento en cáncer de mama precoz más de un año (ver Farmacología, Propiedades farmacodinámicas). Reducción de dosis: Cáncer de Mama Metastásico (CMM), Cáncer de Mama Precoz (CMP) y Cáncer Gástrico Metastásico (CGM): No se realizaron reducciones en la dosis de Herceptin i.v. durante los ensayos clínicos. Los pacientes pueden continuar la terapia durante los períodos de mielosupresión reversible inducida por quimioterápicos, pero deben ser cuidadosamente monitorizados para detectar posibles complicaciones debidas a la neutropenia durante estos lapsos. Consulte el Prospecto Información para Profesionales de paclitaxel, docetaxel o inhibidor de la aromatasa para información sobre cómo reducir o retrasar las administraciones de estos medicamentos. Si la fracción de eyección del ventrículo izquierdo (FEVI) desciende ≥ 10 puntos porcentuales de fracción de eyección (FE) respecto del valor inicial y hasta por debajo del 50%, el tratamiento debe ser suspendido y se debe repetir la evaluación de la FEVI después de aproximadamente 3 semanas. Si ésta no ha mejorado o ha disminuido más, o se desarrolló insuficiencia cardíaca congestiva (ICC) sintomática se debe considerar seriamente interrumpir el tratamiento con Herceptin i.v., a menos que los beneficios para un caso individual sean considerados mayores que los riesgos. Todos estos pacientes deben ser derivados a un cardiólogo para su evaluación y seguimiento. Omisión de dosis: Cáncer de Mama Metastásico (CMM), Cáncer de Mama Precoz (CMP) y Cáncer Gástrico Met
astásico (CGM): Si el paciente ha omitido una dosis de Herceptin i.v. y ha transcurrido una semana o menos, debe administrársele tan pronto como sea posible la dosis habitual de mantenimiento (régimen semanal: 2 mg/kg; régimen cada 3 semanas: 6 mg/kg). No hay que esperar al siguiente ciclo. Por lo tanto, las siguientes dosis de mantenimiento de Herceptin i.v. deben administrarse 7 días o 21 días después, de acuerdo con el esquema semanal o cada 3 semanas, respectivamente. Si el paciente ha omitido una dosis de Herceptin i.v. y ha transcurrido más de una semana, debe volver a administrársele tan pronto como sea posible la dosis inicial durante aproximadamente 90 minutos (régimen semanal: 4 mg/kg; régimen cada 3 semanas: 8 mg/kg). Las siguientes dosis de mantenimiento de Herceptin i.v. (régimen semanal: 2 mg/kg; régimen cada 3 semanas: 6 mg/kg, respectivamente) se deben administrar 7 días o 21 días después, de acuerdo con el esquema semanal o cada 3 semanas, respectivamente. Poblaciones especiales de pacientes: No se han realizado estudios farmacocinéticos específicos en pacientes de edad avanzada ni en aquéllos con insuficiencia renal o hepática. En un análisis farmacocinético de la población, la edad y la insuficiencia renal no afectaban la biodisponibilidad de trastuzumab. Pacientes pediátricos: No existe un uso relevante de Herceptin en esta población. Forma de administración: La dosis de inicio de Herceptin se debe administrar como infusión intravenosa durante 90 minutos. No administrar como pulso o bolo intravenoso. La infusión intravenosa de Herceptin debe ser administrada por un profesional sanitario entrenado en el manejo de anafilaxia y con un dispositivo de emergencia disponible. Se debe observar a los pacientes durante al menos seis horas desde el comienzo de la primera infusión y durante dos horas desde el inicio de las siguientes infusiones, para detectar síntomas tales como fiebre y escalofríos u otras manifestaciones relacionadas con la infusión (ver Precauciones y Reacciones adversas). La interrupción o la disminución del ritmo de la infusión pueden ayudar a controlar estas reacciones. Puede continuarse la infusión cuando los síntomas disminuyan. Si la dosis de inicio es bien tolerada, las dosis siguientes pueden administrarse en infusión de 30 minutos. Para mayor información sobre las instrucciones de uso y manipulación de Herceptin formulación intravenosa, ver Precauciones especiales de eliminación y otras manipulaciones.
Contraindicaciones.
Hipersensibilidad al trastuzumab, a las proteínas murinas o a cualquiera de los excipientes. Disnea grave en reposo debida a complicaciones de la enfermedad maligna avanzada o que requieran terapia suplementaria con oxígeno.
Reacciones adversas.
Resumen del perfil de seguridad: Entre las reacciones adversas más serias y/o frecuentes comunicadas hasta la fecha con el uso de Herceptin i.v. y Herceptin s.c. se encuentran disfunción cardíaca, reacciones relacionadas con la infusión, hematotoxicidad (en particular neutropenia), infecciones y reacciones adversas pulmonares. Tabla de reacciones adversas con la formulación intravenosa: Las reacciones adversas se definen en las siguientes categorías de frecuencia: muy frecuentes (≥ 1/10), frecuentes (≥ 1/100 a < 1/10), poco frecuentes (≥ 1/1.000 a < 1/100), raras (≥ 1/10.000 a < 1/1.000), muy raras ( < 1/10.000) y no conocidas (cuando la frecuencia no se puede estimar con los datos disponibles). Dentro de cada grupo de frecuencia, las reacciones adversas se presentan en orden decreciente de gravedad. En la Tabla 15 se presentan las reacciones adversas notificadas en relación con el uso de Herceptin i.v., solo o en combinación con quimioterapia, en ensayos clínicos pivotales y en la etapa de poscomercialización. Todos los términos incluidos se basan en los porcentajes más altos observados en los ensayos clínicos pivotales.
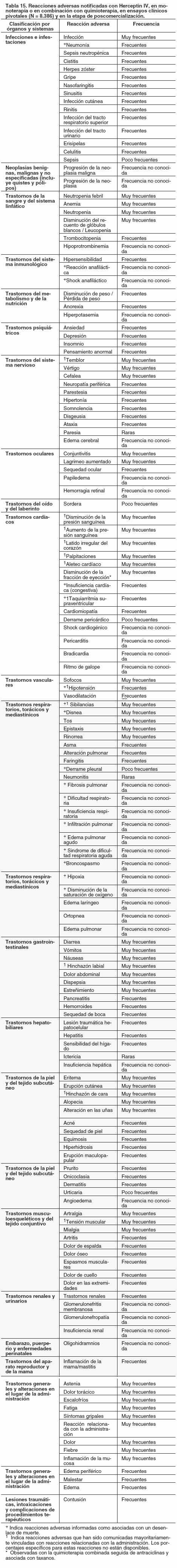
Descripción de las reacciones adversas seleccionadas: Inmunogenicidad: En el tratamiento neoadyuvante-adyuvante del cáncer de mama precoz, el 8,1% (24/296) de los pacientes tratados con Herceptin i.v. desarrollaron anticuerpos contra trastuzumab (independientemente de la presencia de anticuerpos al inicio del tratamiento). Anticuerpos neutralizantes anti-trastuzumab fueron detectados en 2 de 24 muestras posinicio de pacientes tratados con Herceptin i.v. La relevancia clínica de estos anticuerpos se desconoce; sin embargo, estos anticuerpos no parecieron haber afectado la farmacocinética, la eficacia (determinada por la respuesta patológica completa) y la seguridad (señalada por la aparición de reacciones relacionadas con la infusión) de Herceptin i.v. Disfunción cardíaca: La insuficiencia cardíaca congestiva (NYHA II - IV) es una reacción adversa frecuente con Herceptin i.v. y ha sido asociada con un desenlace fatal (ver Precauciones). En pacientes tratados con Herceptin i.v. se observaron signos y síntomas de disfunción cardíaca, tales como disnea, ortopnea, aumento de la tos, edema pulmonar, galope S3, o reducción de la fracción de eyección del ventrículo (ver Precauciones). En tres ensayos clínicos pivotales de Herceptin i.v., administrado como tratamiento adyuvante en combinación con quimioterapia, la incidencia de disfunción cardíaca Grados 3/4 (concretamente insuficiencia cardíaca congestiva sintomática) fue similar en pacientes que recibieron quimioterapia sola (es decir, sin Herceptin i.v.) y en aquéllos a los que se les administró Herceptin i.v. secuencialmente a un taxano (0,3% - 0,4%). La tasa fue mayor en los pacientes tratados con Herceptin i.v. simultáneamente con un taxano (2,0%). En el tratamiento neoadyuvante, la experiencia de la coadministración de Herceptin i.v. con regímenes de antraciclinas a dosis bajas es limitada (ver Precauciones). Cuando se administró Herceptin i.v. después de terminar la quimioterapia adyuvante, se observó insuficiencia cardíaca NYHA Clases III - IV en un 0,6% de las pacientes en el grupo de un año después de una mediana de seguimiento de 12 meses. Luego de una mediana de seguimiento de 3,6 años, la incidencia de ICC severa y disfunción ventricular izquierda permaneció baja, a 0,8% y 9,8%, respectivamente, después de 1 año de tratamiento con Herceptin i.v. En el ensayo BO16348, después de una mediana de seguimiento de 8 años, la incidencia de ICC severa (NYHA Clases III y IV) en el grupo de tratamiento con Herceptin i.v. durante 1 año fue de 0,8%, y la tasa de insuficiencia ventricular izquierda asintomática y sintomática leve de 4,6%. La reversibilidad de la insuficiencia cardíaca congestiva severa (definida como una secuencia de por lo menos dos valores consecutivos de FEVI ≥ 50% después de un evento) fue evidente para el 71,4% de los pacientes tratados con Herceptin i.v. La reversibilidad de la disfunción ventricular izquierda asintomática y sintomática leve se demostró para el 79,5% de las pacientes. Aproximadamente el 17% de los eventos relacionados con disfunción cardíaca ocurrieron después de terminar con Herceptin i.v. En el análisis conjunto de los ensayos NSABP B-31 y NCCTG N9831, con una mediana de seguimiento de 8,1 años para el grupo AC→PH (doxorrubicina y ciclofosfamida, seguido de paclitaxel con trastuzumab), la incidencia por paciente de una nueva aparición de disfunción cardíaca, según lo determinado por FEVI, se mantuvo sin cambios en comparación con el análisis realizado con una mediana de seguimiento de 2,0 años en el grupo AC→PH: el 18,5% de los pacientes del grupo AC→PH con FEVI disminuida de ≥ 10% a menos del 50%. La reversibilidad de la disfunción ventricular izquierda se informó en el 64,5% de los pacientes del grupo AC→PH que experimentaron ICC sintomática, siendo asintomática durante el último seguimiento, y el 90,3% tuvo recuperación total o parcial de FEVI. En los ensayos pivotales en metástasis de Herceptin i.v., la incidencia de alteración cardíaca varió entre 9% y 12% cuando se dio en combinación con paclitaxel comparado con 1% - 4% para paclitaxel solo. En monoterapia, la incidencia fue 6% - 9%. La tasa mayor de disfunción cardíaca se observó en los pacientes que estaban recibiendo Herceptin i.v. simultáneamente con antraciclinas/ciclofosfamida (27%), significativamente mayor que con antraciclinas/ciclofosfamida sola (7% - 10%). En un ensayo posterior con monitorización prospectiva de la función cardíaca, la incidencia de ICC sintomática fue de 2,2% en los pacientes que estaban recibiendo Herceptin i.v. y docetaxel, comparado con 0% en los tratados con docetaxel solo. La mayoría de los pacientes (79%) que tuvieron disfunción cardíaca en estos ensayos experimentaron una mejoría después de recibir el tratamiento estándar para la ICC. Reacciones a la infusión, reacciones de tipo alérgico e hipersensibilidad: Cuando hay metástasis se estima que aproximadamente el 40% de los pacientes tratados con Herceptin i.v. presentará alguna reacción relacionada con la infusión. Sin embargo, la mayoría de estas reacciones son de intensidad leve a moderada (sistema de graduación NCI-CTC) y tienden a manifestarse al inicio del tratamiento, es decir en la primera, segunda o tercera infusión, reduciéndose su frecuencia en las infusiones posteriores. Estas reacciones incluyen escalofríos, fiebre, disnea, hipotensión, sibilancias, broncospasmo, taquicardia, saturación de oxígeno reducida, dificultad respiratoria, erupción cutánea, náuseas, vómitos y cefalea (ver Precauciones). La tasa de reacciones relacionadas con la infusión de todos los Grados varió entre los ensayos dependiendo de la indicación, ya sea que trastuzumab se administrara concomitantemente con quimioterapia o como monoterapia, y de la metodología de recopilación de datos. Las reacciones anafilácticas severas que requieren intervención inmediata adicional, pueden ocurrir durante la primera o segunda infusión de Herceptin i.v. (ver Precauciones) y han sido asociadas con un desenlace de muerte. Se han observado reacciones anafilácticas en casos aislados. Hematotoxicidad: Ocurren muy frecuentemente casos de neutropenia febril. Las reacciones adversas que se manifiestan con frecuencia incluyen anemia, leucopenia, trombocitopenia y neutropenia. La frecuencia de presencia de hipoprotrombinemia no es conocida. El riesgo de neutropenia puede incrementarse levemente cuando trastuzumab es administrado con docetaxel seguido de una terapia con antraciclina. Reacciones pulmonares: Rara vez ocurren reacciones adversas pulmonares severas con el uso de Herceptin y se han asociado con desenlace fatal. Entre éstas se incluyen, pero no se limitan: infiltrados pulmonares, síndrome de dificultad respiratoria aguda, neumonía, neumonitis, derrame pleural, dificultad respiratoria, edema pulmonar agudo e insuficiencia respiratoria (ver Precauciones). Cambio de tratamiento de Herceptin i.v. a Herceptin s.c. y viceversa: En el ensayo MO22982 se investigó el cambio entre Herceptin i.v. y Herceptin s.c., y viceversa, en pacientes con cáncer de mama precoz HER2 positivo, con el objetivo primario de evaluar la preferencia de los pacientes entre ambos, Herceptin i.v. en infusión o Herceptin s.c. en inyección. En este ensayo, se investigaron 2 cohortes (una usando Herceptin s.c. en vial y la otra Herceptin s.c. con sistema de administración) utilizando un diseño cruzado de 2 grupos con 488 pacientes que fueron aleatorizados a una de las dos secuencias diferentes de tratamiento con Herceptin cada tres semanas (Herceptin i.v. [ciclos 1-4] → Herceptin s.c. [ciclos 5-8], o Herceptin s.c. [ciclos 1-4] → Herceptin i.v. [ciclos 5-8]). Había pacientes tanto sin terapia previa con Herceptin i.v. (20,3%) como pre-expuestos a Herceptin i.v. (79,7%) como parte del tratamiento adyuvante en curso para cáncer de mama precoz HER2 positivo. En general, los cambios de Herceptin i.v. a Herceptin s.c. y viceversa fueron bien tolerados. Las tasas pre-cambio (ciclos 1-4) de eventos adversos serios, eventos adversos Grado 3 e interrupciones del tratamiento debido a efectos adversos fueron bajas ( < 5%) y similares a las tasas pos-cambio (ciclos 5-8). No se notificaron reacciones adversas de Grados 4 ó 5. Comunicación de reportes de reacciones adversas: Es importante comunicar las presuntas reacciones adversas después de la autorización del medicamento. Esto permite la monitorización continua de la relación riesgo/beneficio. Se solicita a los profesionales de la salud informar de cualquier sospecha de eventos adversos asociados con el uso de Herceptin® al Área de Farmacovigilancia de Roche al siguiente teléfono 0800-77-ROCHE (76243). En forma alternativa, esta información puede ser reportada ante ANMAT. Ante cualquier inconveniente con el producto, el paciente puede llenar la ficha que está en la Página Web de la ANMAT: http://www.anmat.gov.ar/farmacovigilancia/Notificar.asp o llamar a ANMAT responde al 0800-333-1234.
Precauciones.
A fin de mejorar la trazabilidad de los medicamentos biológicos, el nombre comercial y el número de lote del producto deben estar claramente registrados (o mencionados) en la historia clínica del paciente. La determinación de HER2 debe llevarse a cabo en un laboratorio especializado que pueda asegurar una adecuada validación de los procedimientos de valoración (véase Farmacología, Propiedades farmacodinámicas). Actualmente no hay datos disponibles de ensayos clínicos sobre el retratamiento en pacientes que hayan sido previamente tratados con Herceptin como adyuvante. Disfunción cardíaca: Consideraciones generales: Los pacientes tratados con Herceptin i.v. tienen un riesgo mayor de desarrollar insuficiencia cardíaca congestiva (ICC) (New York Heart Association [NYHA] Clases II - IV) o disfunción cardíaca asintomática. Estos eventos se han observado en pacientes tratados con Herceptin i.v. en monoterapia o en combinación con taxanos (paclitaxel o docetaxel), particularmente después de quimioterapia con una antraciclina (doxorrubicina o epirrubicina). Dicha insuficiencia puede ser de moderada a grave y se ha asociado con mortalidad (ver Reacciones adversas). Además, se debe tener precaución cuando se traten pacientes con un mayor riesgo cardíaco (por ejemplo, hipertensión, antecedentes de enfermedad arterial coronaria, insuficiencia cardíaca congestiva, fracción de eyección del ventrículo izquierdo [FEVI] menor de 55%, edad avanzada). Todos los candidatos para el tratamiento con Herceptin i.v., pero especialmente aquellos tratados previamente con antraciclinas y ciclofosfamida (AC), deben ser sometidos a examen cardíaco basal, incluyendo historial y examen físico, electrocardiograma (ECG), ecocardiograma y/o ventriculografía isotópica (MUGA) o resonancia magnética nuclear. La monitorización puede ayudar a identificar a los pacientes que desarrollen disfunción cardíaca. Las evaluaciones cardíacas realizadas antes de iniciar el tratamiento se deben repetir cada 3 meses durante el tratamiento, y cada 6 meses después de la interrupción del mismo, hasta los 24 meses desde la última administración de Herceptin i.v. Se debe efectuar una cuidadosa evaluación del beneficio-riesgo antes de decidir el tratamiento con Herceptin i.v. Simulaciones con modelos farmacocinéticos de población indican que trastuzumab puede persistir en el torrente circulatorio hasta 7 meses después de la finalización del tratamiento con Herceptin i.v. o s.c. (ver Farmacología, Propiedades farmacocinéticas). Los pacientes que reciban antraciclinas después de la supresión de Herceptin i.v., pueden posiblemente tener un mayor riesgo de padecer disfunción cardíaca. Si fuera posible, el especialista debe evitar el tratamiento basado en antraciclinas hasta 7 meses después de finalizar la administración de Herceptin i.v. En caso de que se empleen antraciclinas se debe monitorizar cuidadosamente la función cardíaca del paciente. Los pacientes que después del cribado basal presenten eventos cardiovasculares, deberían ser sometidos a una evaluación cardiológica más exhaustiva. La función cardíaca debe ser monitorizada en todos los pacientes durante el tratamiento (por ejemplo, cada 12 semanas). La monitorización puede ayudar a identificar a aquéllos que desarrollen disfunción cardíaca. Si ésta es asintomática, los pacientes se pueden beneficiar al realizarles un control más frecuente (por ejemplo, cada 6 - 8 semanas). Si los pacientes tienen una disminución continuada de la función ventricular izquierda, pero permanece asintomática, el especialista debe valorar la interrupción del tratamiento si no se observa beneficio clínico con Herceptin i.v. No se ha estudiado en forma prospectiva la seguridad después de continuar o reanudar el tratamiento con Herceptin i.v. en pacientes que presenten disfunción cardíaca. Si la fracción de eyección del ventrículo izquierdo (FEVI) desciende más de o igual a 10 puntos porcentuales en la fracción de eyección (FE) respecto del valor inicial y hasta por debajo del 50%, el tratamiento debe ser interrumpido y se repetirá la evaluación de la FEVI después de aproximadamente 3 semanas. Si la FEVI no ha mejorado o ha disminuido más, o se ha desarrollado una ICC sintomática, se debe considerar seriamente interrumpir el tratamiento con Herceptin i.v., a menos que los beneficios para un caso individual sean considerados mayores que los riesgos. Todos estos pacientes deben ser derivados a un cardiólogo para su evaluación y seguimiento. Si se presenta insuficiencia cardíaca sintomática durante la terapia con Herceptin i.v., debe tratarse con los medicamentos habituales para estos casos. La mayoría de los pacientes que desarrollaron ICC o disfunción cardíaca asintomática en ensayos pivotales mejoraron con el tratamiento médico estándar para la ICC, que incluía un inhibidor de la enzima convertidora de angiotensina (IECA) o un bloqueante del receptor de angiotensina y un betabloqueante. La mayoría de los pacientes que manifestaron síntomas cardíacos y una evidencia de beneficio clínico con el tratamiento con Herceptin i.v., continuaron con el mismo sin presentar acontecimientos clínicos cardíacos adicionales. Cáncer de Mama Metastásico (CMM): No deben administrarse simultáneamente en combinación Herceptin i.v. y antraciclinas en el tratamiento de pacientes con cáncer de mama metastásico. Los pacientes con cáncer de mama metastásico a los que previamente se les haya administrado antraciclinas, tienen también riesgo de presentar disfunción cardíaca al ser tratados con Herceptin i.v., aunque este peligro es menor que si se administra Herceptin i.v. y antraciclinas simultáneamente. Cáncer de Mama Precoz (CMP): En los pacientes con cáncer de mama precoz se debe repetir una evaluación cardiológica como la realizada al inicio, cada 3 meses durante el tratamiento, y cada 6 meses después de la interrupción del mismo, hasta 24 meses desde la última administración de Herceptin i.v. En aquéllos que reciben quimioterapia con antraciclinas se recomienda un seguimiento más prolongado, y debe hacerse cada año hasta 5 años desde la última administración de Herceptin i.v., o más tiempo si se observa un descenso continuo de la fracción de eyección del ventrículo izquierdo (FEVI). Los pacientes con antecedentes de infarto de miocardio (IM), angina de pecho que requiera tratamiento con medicamentos, antecedentes de ICC o existencia de ICC (NYHA, Clases II-IV), FEVI menor de 55%, otras cardiomiopatías, arritmia cardíaca que exija farmacoterapia, valvulopatía clínicamente significativa, hipertensión poco controlada (solamente con medicación estándar) y derrame pericárdico con repercusión o efectos hemodinámicos fueron excluidos de los ensayos pivotales de Herceptin i.v. en neoadyuvancia del cáncer de mama precoz y, por lo tanto, el tratamiento no se puede recomendar en estos pacientes. Tratamiento adyuvante: No se debe administrar Herceptin i.v. y antraciclinas simultáneamente en combinación para el tratamiento adyuvante. En los pacientes con cáncer de mama precoz (CMP) se observó un aumento en la incidencia de eventos cardíacos sintomáticos y asintomáticos cuando se administró Herceptin i.v. después de la quimioterapia con antraciclina en comparación con un régimen sin antraciclinas de docetaxel y carboplatino. Este incremento en la incidencia de eventos cardíacos fue más marcado con la administración simultánea de Herceptin i.v. más taxanos si se lo compara con la forma secuencial. Independientemente del régimen utilizado, la mayoría de los eventos cardíacos sintomáticos se produjeron en los primeros 18 meses. En uno de los tres ensayos pivotales realizados, con una mediana de seguimiento disponible de 5,5 años (BCIRG 006), se observó una elevación continua de la tasa acumulada de eventos cardíacos sintomáticos o de FEVI en los pacientes a los que se les administró Herceptin i.v. simultáneamente con un taxano después del tratamiento con antraciclinas; el aumento fue de hasta 2,37% en comparación con, aproximadamente, el 1% en los dos grupos de comparación (antraciclina y ciclofosfamida seguido de taxanos y taxanos, carboplatino y Herceptin i.v.). Los factores de riesgo para los eventos cardíacos identificados en cuatro grandes ensayos adyuvantes fueron pacientes de edad avanzada (mayores de 50 años), baja FEVI basal ( < 55%) antes o después de la iniciación del tratamiento con paclitaxel, descenso en la FEVI de 10 - 15 puntos, y terapia previa o concomitante con medicamentos antihipertensivos. En los pacientes que recibieron Herceptin i.v. después de la finalización de la quimioterapia adyuvante, el riesgo de disfunciones cardíacas se asoció con una mayor dosis acumulada de antraciclinas administrada antes del comienzo con Herceptin i.v. y un índice de masa corporal (IMC) > 25 kg/m2. Tratamiento neoadyuvante-adyuvante: En pacientes con cáncer de mama precoz elegibles para tratamiento neoadyuvante-adyuvante, Herceptin i.v. sólo debe ser administrado simultáneamente con antraciclinas en pacientes no tratados previamente y sólo con regímenes de antraciclinas a dosis bajas, es decir con dosis máximas acumulativas de doxorrubicina 180 mg/m2 o epirrubicina 360 mg/m2. Si los pacientes han sido tratados simultáneamente con un ciclo completo de dosis bajas de antraciclinas y Herceptin i.v. en el tratamiento de neoadyuvancia, después de la cirugía no se les debe administrar quimioterapia citotóxica. En otras situaciones, la decisión de si es necesaria quimioterapia adicional citotóxica se determinará de acuerdo con los factores individuales. La experiencia de la coadministración de trastuzumab con regímenes de antraciclinas a dosis bajas se limita a dos ensayos. Herceptin i.v. fue administrado simultáneamente con quimioterapia neoadyuvante que contenía de 3 a 4 ciclos de una antraciclina (dosis acumulativa de doxorrubicina 180 mg/m2 o dosis de epirrubicina 300 mg/m2). La incidencia de disfunción cardíaca sintomática fue baja en el grupo de Herceptin i.v. (hasta 1,7%). La experiencia clínica es escasa en pacientes mayores de 65 años de edad. Reacciones asociadas con la infusión e hipersensibilidad: Se han notificado reacciones serias asociadas con la infusión con Herceptin i.v. las cuales incluyeron disnea, hipotensión, sibilancias, hipertensión, broncospasmo, taquiarritmia supraventricular, disminución de la saturación de oxígeno, anafilaxia, dificultad respiratoria, urticaria y angioedema (véase Reacciones adversas). Se puede utilizar medicación previa para reducir el riesgo de aparición de estos acontecimientos. La mayoría de estas reacciones ocurren durante o dentro de las 2,5 horas siguientes al comienzo de la primera infusión. Si aparece una reacción a la infusión, se debe interrumpir o administrarse en forma más lenta y el paciente debe ser monitorizado hasta la resolución de cualquiera de los síntomas observados (ver Dosificación). Estos pueden ser tratados con un analgésico/antipirético como meperidina o paracetamol, o un antihistamínico como difenhidramina. La mayoría de los pacientes presentaron resolución de los síntomas y posteriormente recibieron infusiones adicionales de Herceptin i.v. Las reacciones serias se trataron satisfactoriamente con terapia de apoyo tal como oxígeno, beta-agonistas y corticoides. En raras ocasiones, estas reacciones se asocian con una evolución clínica con desenlace fatal. Los pacientes que presenten disnea en reposo debida a complicaciones de su enfermedad maligna avanzada y comorbilidades pueden presentar mayor riesgo de una reacción fatal a la infusión. Por lo tanto, estos pacientes no deben ser tratados con Herceptin i.v. (ver Contraindicaciones). También se ha notificado una mejora inicial seguida de un empeoramiento clínico y reacciones tardías con un rápido deterioro clínico. Se han producido fallecimientos en horas y hasta una semana después de la infusión. En muy raras ocasiones, los pacientes han experimentado la aparición de síntomas relacionados con la infusión y reacciones pulmonares más de seis horas después del inicio de la infusión con Herceptin i.v. Los pacientes deben ser advertidos de la posibilidad de un inicio tardío y deben ser instruidos para contactarse con su médico si aparecen estos síntomas. Reacciones pulmonares: Durante el período de poscomercialización, se han comunicado reacciones pulmonares severas con el uso de Herceptin i.v. (ver Reacciones adversas), que en algunas ocasiones han sido mortales. Adicionalmente, se han observado casos de enfermedad pulmonar intersticial incluyendo infiltrados pulmonares, síndrome de dificultad respiratoria aguda, neumonía, neumonitis, derrame pleural, dificultad respiratoria, edema pulmonar agudo e insuficiencia respiratoria. Los factores de riesgo asociados con la enfermedad pulmonar intersticial incluyen la terapia previa o concomitante con otros antineoplásicos que se conoce que están asociados con enfermedad pulmonar intersticial, tales como taxanos, gemcitabina, vinorelbina y radioterapia. Estas reacciones pueden darse como parte de una reacción relacionada con la infusión o aparecer tardíamente. Los pacientes que presenten disnea en reposo debida a complicaciones de su enfermedad maligna avanzada y comorbilidades pueden presentar mayor riesgo de reacciones pulmonares. Por lo tanto, estos pacientes no deben ser tratados con Herceptin i.v. (véase Contraindicaciones). Debe prestarse especial atención a las neumonitis, especialmente en pacientes tratados concomitantemente con taxanos. Herceptin inyectable multidosis: El alcohol bencílico, conservante utilizado en el agua bacteriostática para preparaciones inyectables suministrada, provocó efectos tóxicos en recién nacidos y niños menores de 3 años. En caso de que Herceptin i.v. deba administrarse a pacientes con hipersensibilidad conocida al alcohol bencílico, el polvo deberá diluirse únicamente con agua para preparaciones inyectables y sólo se empleará una dosis por frasco. Se descartará cualquier residuo no utilizado. El agua estéril para preparaciones inyectables que se usa para la reconstitución de un concentrado para infusión de 150 mg de trastuzumab para inyección única no contiene alcohol bencílico. Efectos sobre la capacidad para conducir y utilizar máquinas: La influencia de Herceptin i.v. sobre la capacidad para conducir y utilizar máquinas es nula o insignificante. Sin embargo, los pacientes que presentan síntomas relacionados con la infusión (ver Precauciones) deben ser advertidos de no conducir vehículos o utilizar maquinaria hasta que los síntomas remitan. Fertilidad, embarazo y lactancia: Mujeres en edad fértil/Anticoncepción: Se debe advertir a las mujeres en edad fértil que utilicen métodos anticonceptivos eficaces durante el tratamiento con Herceptin i.v. y durante siete meses después de concluido el mismo (ver Farmacología, Propiedades farmacocinéticas). Embarazo: Se han llevado a cabo estudios de reproducción en monos cynomolgus, con dosis hasta 25 veces la dosis semanal de mantenimiento en seres humanos de 2 mg/kg de Herceptin i.v. sin que se haya revelado evidencia alguna de alteración de la fertilidad o daño al feto. Se ha observado transferencia placentaria de trastuzumab durante la fase temprana de gestación (días 20 - 50 de gestación) y tardía (días 120 - 150 de gestación). No se conoce si Herceptin i.v. puede afectar la capacidad reproductiva. Dado que los estudios de reproducción animal no son siempre predictivos de la respuesta en seres humanos, se debe evitar Herceptin i.v. durante el embarazo, a menos que el beneficio potencial para la madre supere el riesgo potencial para el feto. En el período de poscomercialización se han notificado casos de retraso del crecimiento renal y/o insuficiencia renal en el feto asociado con oligohidramnios, algunos vinculados con hipoplasia pulmonar fatal del feto, en mujeres embarazadas en tratamiento con Herceptin i.v. Si se produjera un embarazo, se debe advertir a la paciente, acerca de la posibilidad de daño fetal. Si se trata a una mujer embarazada con Herceptin i.v., o si una paciente se embaraza mientras recibe Herceptin i.v. o dentro de los siete meses siguientes a la última dosis de Herceptin i.v., es deseable realizar un seguimiento estrecho por un equipo multidisciplinario. Lactancia: Un estudio llevado a cabo en monos cynomolgus con dosis 25 veces la dosis de mantenimiento semanal en seres humanos de 2 mg/kg de Herceptin i.v. demostró que trastuzumab se excreta en la leche. La presencia de trastuzumab en el suero de monos pequeños no se ha asociado con ninguna reacción adversa en su crecimiento o desarrollo desde el nacimiento al mes de edad. Se ignora si trastuzumab pasa a la leche humana. Dado que la IgG humana se secreta en la leche humana, y el potencial de daño para el niño es desconocido, se debe evitar la lactancia durante el tratamiento con Herceptin i.v. y durante los 7 meses después de su finalización. Fertilidad: No se dispone de datos sobre la fertilidad.
Interacciones.
No se han realizado estudios formales de interacciones de medicamentos con Herceptin i.v. en seres humanos. No se han observado interacciones clínicamente significativas entre Herceptin i.v. y la medicación concomitante usada en los ensayos clínicos. En los estudios donde se administró Herceptin i.v. en combinación con docetaxel, carboplatino o anastrozol, la farmacocinética de estos medicamentos no se alteró, ni tampoco la de trastuzumab. Las concentraciones de paclitaxel y doxorrubicina (y sus principales metabolitos 6-a-hidroxil-paclitaxel, OH-P, y doxorrubicinol, DOL) no se modificaron por la presencia de trastuzumab. Sin embargo, trastuzumab podría aumentar la exposición total de un metabolito de la doxorrubicina, (7-deoxi-13 dihidro-doxorrubicinoma, D7D). La bioactividad de D7D y el impacto clínico del aumento de este metabolito no se ha esclarecido aún. No se observaron cambios en las concentraciones de trastuzumab en la presencia de paclitaxel y doxorrubicina. Los resultados de un subestudio de interacción medicamentosa que evaluó la farmacocinética de capecitabina y cisplatino cuando son usados con o sin trastuzumab, sugirieron que la exposición a los metabolitos bioactivos de capecitabina, por ejemplo 5-FU, no se alteraba por la administración concomitante de cisplatino, ni por el empleo simultáneo de cisplatino más trastuzumab. Sin embargo, la capecitabina por sí misma mostró concentraciones más altas y una vida media mayor cuando se combinaba con trastuzumab. Los datos también sugirieron que la farmacocinética de cisplatino no se modificaba por el uso concomitante de capecitabina ni por la asociación de capecitabina más trastuzumab.
Incompatibilidades.
No se han observado incompatibilidades entre Herceptin i.v. y las bolsas de cloruro de polivinilo, polietileno o polipropileno. Este medicamento no debe mezclarse o diluirse con otros productos, excepto los mencionados en "Precauciones especiales de eliminación y otras manipulaciones". No diluir con soluciones de glucosa, ya que causa agregación de la proteína.
Conservación.
Vial con 150 mg y vial con 440 mg: Los viales deben conservarse en heladera entre 2°C a 8°C. Para las condiciones de conservación del medicamento una vez abierto, ver Período de validez y Precauciones especiales de eliminación y otras manipulaciones. Precauciones especiales de eliminación y otras manipulaciones: Se deben emplear métodos asépticos adecuados. Reconstitución: Herceptin i.v. se debe manejar cuidadosamente durante la reconstitución. Si durante la misma se produce espuma excesiva o se agita la solución reconstituida de Herceptin i.v. se pueden originar problemas con la cantidad de solución de Herceptin i.v. que se pueda extraer del vial. Instrucciones para la reconstitución - vial con 440 mg: La reconstitución se debe realizar con agua bacteriostática para inyección (suministrada en el envase), que contiene alcohol bencílico al 1,1%. De esta manera, se obtiene una solución para dosis múltiples, que contiene 21 mg/ml de trastuzumab, a un pH de aproximadamente 6,0. Se debe evitar el empleo de otros solventes para reconstitución, excepto por agua para preparaciones inyectables en caso de pacientes con hipersensibilidad conocida al alcohol bencílico. Con una jeringa estéril, inyecte lentamente 20 ml de agua bacteriostática para preparaciones inyectables en el vial que contiene Herceptin i.v. liofilizado, dirigiendo el flujo hacia el liofilizado. Mueva el vial en círculos con suavidad para ayudar la reconstitución. ¡No lo agite! Instrucciones para la reconstitución - vial con 150 mg: Con una jeringa estéril, inyecte lentamente 7,2 ml de agua estéril para preparaciones inyectables en el vial que contiene Herceptin i.v. liofilizado, dirigiendo el flujo hacia el liofilizado. Mueva el vial en círculos con suavidad para ayudar la reconstitución. ¡No lo agite! La formación de una ligera espuma después de la reconstitución es usual. Deje el vial en reposo durante aproximadamente 5 minutos. Herceptin i.v. reconstituido es una solución transparente de incolora a amarillo pálido y debe estar esencialmente libre de partículas visibles. Dilución de la solución reconstituida: Se determinará el volumen de solución requerida: sobre la base de la dosis inicial de 4 mg de trastuzumab/kg de peso corporal o dosis semanales posteriores de 2 mg de trastuzumab/kg de peso corporal: Volumen (ml) = Peso corporal (kg) x dosis (4 mg/kg dosis inicial ó 2 mg/kg para dosis sucesivas): 21 (mg/ml, concentración de la solución reconstituida) sobre la base de la dosis inicial de 8 mg de trastuzumab/kg de peso corporal o dosis posteriores cada 3 semanas de 6 mg de trastuzumab/kg de peso corporal: Volumen (ml) = Peso corporal (kg) x dosis (8 mg/kg dosis inicial ó 6 mg/kg para dosis sucesivas) 21 (mg/ml, concentración de la solución reconstituida). La cantidad apropiada de solución se deberá extraer del vial y añadirse a una bolsa de infusión que contenga 250 ml de cloruro sódico al 0,9%. No se debe emplear soluciones de glucosa (ver Incompatibilidades). La bolsa debe invertirse suavemente varias veces para mezclar la solución y evitar la formación de espuma. Los medicamentos de uso parenteral deben comprobarse visualmente antes de su administración para detectar la posible existencia de partículas o decoloración. Se debe administrar la infusión inmediatamente después de haber sido preparada (véase Período de validez). La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él, se realizará de acuerdo con la normativa local. Este medicamento no debe ser utilizado después de la fecha de vencimiento indicada en el envase. Este medicamento debe ser usado exclusivamente bajo prescripción y vigilancia médica y no puede repetirse sin nueva receta médica. Mantenga los medicamentos fuera del alcance de los niños. Período de validez: Vial con 150 mg: Período de validez de la solución reconstituida: Después de la reconstitución con agua para preparaciones inyectables, la solución reconstituida es física y químicamente estable durante 48 horas a 2°C - 8°C. Desde el punto de vista microbiológico, la solución reconstituida debe diluirse inmediatamente en solución para infusión. En caso contrario, la persona que lo administre será responsable de los tiempos y las condiciones de almacenamiento previo al uso del medicamento que, en general, no deberían exceder las 24 horas a una temperatura de 2°C a 8°C, a menos que la reconstitución se realice mediante técnicas asépticas controladas y validadas. No congelar la solución reconstituida. Período de validez de la solución para infusión que contiene el producto reconstituido: La solución para infusión (solución para infusión de cloruro de sodio al 0,9%) que contiene el producto reconstituido es física y químicamente estable durante 24 horas a una temperatura de 2°C a 8°C. Desde el punto de vista microbiológico, la solución para infusión intravenosa de Herceptin i.v. debe usarse inmediatamente. En caso contrario, la persona que lo administre será responsable de los tiempos y las condiciones de almacenamiento previo al uso del medicamento que, en general, no deberían exceder las 24 horas a una temperatura de 2°C a 8°C, a menos que la reconstitución y la dilución se realicen mediante técnicas asépticas controladas y validadas. Vial con 440 mg: Período de validez de la solución reconstituida: El contenido de un vial de Herceptin i.v. reconstituido con agua bacteriostática para preparaciones inyectables suministrada con el envase puede conservarse durante 28 días a una temperatura comprendida entre 2°C y 8°C. La solución reconstituida contiene un conservante y puede entonces utilizarse en administraciones repetidas. Cualquier resto de solución reconstituida deberá desecharse en un plazo de 28 días. Herceptin i.v. debe ser reconstituido con agua para preparaciones inyectables cuando es administrado a pacientes con hipersensibilidad conocida al alcohol bencílico (ver Precauciones). En caso de que Herceptin i.v. sea reconstituido con agua para preparaciones inyectables, sólo debe ser utilizada una dosis de Herceptin i.v. por vial. La solución reconstituida debe ser empleada inmediatamente y cualquier porción no administrada debe ser descartada. No congelar la solución reconstituida. Período de validez de la solución para infusión que contiene el producto reconstituido: La solución para infusión (solución para infusión de cloruro de sodio al 0,9%) que contiene el producto reconstituido es física y químicamente estable durante 24 horas a una temperatura de 2°C a 8°C. Desde el punto de vista microbiológico, la solución para infusión intravenosa de Herceptin i.v. debe usarse inmediatamente. En caso contrario, la persona que lo administre será responsable de los tiempos y las condiciones de almacenamiento previo al uso del medicamento que, en general, no deberían exceder las 24 horas a una temperatura de 2°C a 8°C, a menos que la reconstitución y la dilución hayan tenido lugar en condiciones asépticas controladas y validadas.
Sobredosificación.
No hay experiencia de sobredosis en ensayos clínicos con seres humanos. En los ensayos clínicos no se han administrado dosis superiores a 10 mg/kg de Herceptin i.v. solo. Hasta este límite, las dosis fueron bien toleradas. Ante la eventualidad de una sobredosificación concurrir al Hospital más cercano o comunicarse con los Centros de Toxicología: Hospital de Pediatría Dr. Ricardo Gutiérrez: 4962-6666/2247; Policlínico Dr. G. A.

