ENBREL Jeringa Prellenada
PFIZER
Inhibidor del factor de necrosis tumoral (FNT) alfa (FNT-a).
Composición.
Cada jeringa prellenada de 25 mg contiene: Etanercept 25 mg, sacarosa, cloruro de sodio, clorhidrato de L- arginina, Fosfato de sodio dibásico dihidratado, Fosfato de sodio monobásico dihidratado y agua para inyección. Cada jeringa prellenada de 50 mg contiene: Etanercept 50 mg, sacarosa, cloruro de sodio, clorhidrato de L- arginina, Fosfato de sodio dibásico dihidratado, Fosfato de sodio monobásico dihidratado y agua para inyección. El etanercept es una proteína humana compuesta por el receptor p75 del factor de necrosis tumoral y la porción Fc de la IgG1 humana, obtenida por tecnología del ADN recombinante a partir de un cultivo de células de ovario de hámster chino (CHO). Etanercept es una proteína dimérica construida genéticamente por fusión del dominio extracelular soluble del receptor-2 del factor de necrosis tumoral humano (FNTR2/p75), unido al dominio Fc de la IgG1 humana. Este componente Fc contiene la región bisagra, las regiones CH2 y CH3, pero no la región CH1 de la IgG1. Etanercept contiene 934 aminoácidos y tiene un peso molecular aparente de aproximadamente 150 kilodaltons. La actividad específica de etanercept es 1.7 x 106 unidades/mg.
Farmacología.
Propiedades Farmacodinámicas: El factor de necrosis tumoral (FNT) es una citoquina dominante en el proceso inflamatorio de la artritis reumatoidea. También se han encontrado niveles elevados de FNT en la membrana sinovial y placas psoriásicas de pacientes con artritis psoriásica y en el suero y el tejido sinovial de pacientes con espondilitis anquilosante. En psoriasis en placas, la infiltración por células inflamatorias incluyendo las células T conduce al incremento de los niveles de FNT en lesiones psoriásicas comparadas con los niveles en la piel no involucrada. Etanercept es un inhibidor competitivo de la unión del FNT a sus receptores de superficie celular, y, por ello, inhibe la actividad biológica del FNT. El FNT y la linfotoxina son citoquinas proinflamatorias que se unen a dos receptores de superficie diferentes: los receptores del factor de necrosis tumoral (rFNT) 55-kilodalton (p55) y 75-kilodalton (p75). Ambos receptores de FNT existen de forma natural unidos a la membrana y en forma soluble. Se cree que los receptores del FNT solubles regulan la actividad biológica del FNT. El FNT y la linfotoxina existen predominantemente como homotrímeros, dependiendo su actividad biológica del entrecruzamiento de los receptores del FNT de la superficie celular. Los receptores solubles diméricos, tales como etanercept poseen mayor afinidad por el FNT que los receptores monoméricos y son inhibidores competitivos considerablemente más potentes de la unión del FNT a sus receptores celulares. Además, la utilización de una región Fc de inmunoglobulina como elemento de fusión en la construcción de un receptor dimérico la dota de una vida media sérica más larga. Mecanismo de acción: Gran parte de la patología articular en la artritis reumatoidea y espondilitis anquilosante y de la patología cutánea en psoriasis en placas, está mediada por moléculas proinflamatorias ligadas a una red controlada por el FNT. Se piensa que el mecanismo de acción del etanercept es la inhibición competitiva de la unión del FNT a los receptores del FNT de la superficie celular impidiendo la respuesta celular mediada por el FNT provocando que el FNT sea biológicamente inactivo. El etanercept también puede modular la respuesta biológica controlada por moléculas adicionales que regulan a la baja (por ejemplo, citoquinas, moléculas de adhesión o proteinasas) que se inducen o regulan por el FNT. Eficacia clínica y seguridad: Esta sección presenta los datos de cuatro estudios controlados y aleatorizados en pacientes adultos con artritis reumatoidea, tres estudios en artritis idiopática juvenil poliarticular (AIJ), un estudio en pacientes adultos con artritis psoriásica, un estudio en pacientes adultos con espondilitis anquilosante, un estudio en pacientes adultos con espondiloartritis axial no radiográfica y cuatro estudios en pacientes adultos con psoriasis en placa. Pacientes adultos con artritis reumatoidea: Se evaluó la eficacia de Enbrel en un estudio doble ciego, aleatorizado y controlado con placebo. El estudio evaluó a 234 pacientes adultos con artritis reumatoidea activa que no habían respondido al tratamiento con por lo menos uno pero no más de cuatro antirreumáticos modificadores de la enfermedad (ARME). Se administraron dosis subcutáneas de 10 mg ó 25 mg de Enbrel o placebo dos veces por semana durante 6 meses consecutivos. Los resultados de este estudio controlado se expresaron en porcentajes de mejoría de la artritis reumatoidea empleando los criterios de respuesta del Colegio Americano de Reumatología (ACR).Las respuestas ACR 20 y 50 fueron superiores en los pacientes tratados con Enbrel a los 3 y 6 meses que en los pacientes tratados con placebo (ACR 20: Enbrel 62 % y 59 %, placebo 23 % y 11 % a los 3 y 6 meses respectivamente; ACR 50: Enbrel 41 % y 40 %, placebo 8 % y 5 % a los 3 y 6 meses respectivamente; p < 0,01 Enbrel vs. placebo en todas las visitas de evaluación de las respuestas ACR 20 y ACR 50). Aproximadamente el 15 % de los pacientes tratados con Enbrel alcanzaron una respuesta ACR 70 a los 3 y 6 meses en comparación con menos del 5 % de los pacientes en el grupo de placebo. Los pacientes tratados con Enbrel en general presentaron respuestas clínicas entre 1 y 2 semanas de iniciado el tratamiento y casi todas se produjeron alrededor de los 3 meses. Se observó una relación dosis-respuesta; los resultados con dosis de 10 mg se ubicaron entre los del placebo y la dosis de 25 mg. Enbrel demostró ser significativamente mejor que el placebo en todos los componentes de los criterios del ACR y en las otras evaluaciones de la actividad de la artritis reumatoidea no incluidas en los criterios de respuesta ACR, tales como rigidez matinal. Se realizó un Cuestionario para la Evaluación de la Salud (HAQ - Health Assessment Questionnaire) cada 3 meses durante el estudio, que incluía las subescalas de discapacidad, vitalidad, salud mental, estado general de salud y estado de salud asociado con la artritis. Se observaron mejorías en todas las subescalas del HAQ en los pacientes tratados con Enbrel a los 3 y 6 meses, en comparación con los controles. En general, los síntomas de la artritis reaparecieron al mes de suspender la administración de Enbrel. De acuerdo con los resultados de los estudios abiertos, la reanudación del tratamiento con Enbrel después de una interrupción de hasta 24 meses produjo el mismo grado de respuesta que en los pacientes tratados con Enbrel sin interrupción del tratamiento. Se observaron respuestas continuas duraderas de hasta 10 años en estudios abiertos de extensión del tratamiento al administrarse Enbrel sin interrupción. Se comparó la eficacia de Enbrel con metotrexato en un tercer estudio aleatorio, controlado con droga activa, con evaluaciones radiológicas ciegas como una variable principal en 632 pacientes adultos con artritis reumatoidea activa ( < 3 años de duración) vírgenes de tratamiento con metotrexato. Se administraron dosis subcutáneas de 10 mg ó 25 mg de Enbrel dos veces por semana durante 24 meses. Las dosis de metotrexato se ajustaron desde 7,5 mg/semana hasta un máximo de 20 mg/semana durante las primeras 8 semanas del estudio, continuándose hasta 24 meses. La mejoría clínica, que incluía comienzo de la acción dentro de las 2 semanas con Enbrel 25 mg, fue similar a la observada en los estudios anteriores, manteniéndose durante los 24 meses. En la evaluación basal los pacientes presentaban un grado moderado de discapacidad, con puntajes promedios en el HAQ de 1,4 a 1,5. El tratamiento con Enbrel 25 mg produjo mejorías sustanciales a los 12 meses, alrededor del 44 % de los pacientes alcanzó un puntaje normal en el HAQ (menos de 0,5). Este beneficio se mantuvo en el segundo año del estudio. En este estudio se evaluó mediante radiografías el daño estructural en las articulaciones y se expresó como variación en el índice total de Sharp (TSS - Total Sharp Score) y sus componentes, índice de erosión e índice de estrechamiento del espacio articular (JSN - Joint Space Narrowing). Se obtuvieron radiografías de manos/muñecas y pies en la visita basal, a los 6, 12 y 24 meses. La dosis de 10 mg de Enbrel demostró tener menor efecto sobre el daño estructural que la dosis de 25 mg. Enbrel 25 mg fue significativamente superior al metotrexato en los resultados de la erosión a los 12 y 24 meses. Las diferencias en los índices de TSS y JSN no fueron estadísticamente significativas entre metotrexato y Enbrel 25 mg. La figura a continuación presenta los resultados.
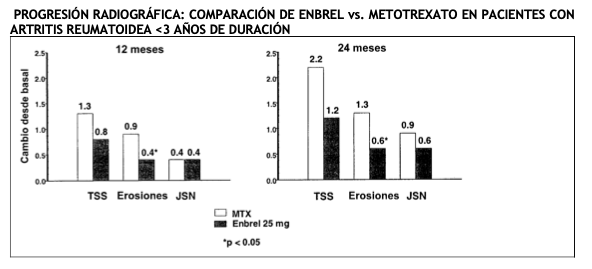
En otro estudio controlado con comparador activo doble-ciego, aleatorizado, en pacientes con AR tratados con Enbrel en monoterapia (25 mg dos veces por semana), metotrexato en monoterapia (7,5 a 20 mg por semana, siendo 20 mg la dosis media), y la combinación de Enbrel y metotrexato iniciada concomitantemente, se compararon la eficacia clínica, la seguridad y la progresión radiográfica en 682 pacientes adultos con artritis reumatoidea activa de 6 meses a 20 años de duración (mediana 5 años) que tuvieron una respuesta no satisfactoria a al menos 1 fármaco modificador de la enfermedad (FARMEs) distinto de metotrexato. Los pacientes en el grupo de Enbrel en combinación con metotrexato tuvieron respuestas ACR20, ACR50 y ACR70 y mejoras de las escalas DAS y HAQ significativamente mayores, a las 24 y a las 52 semanas, que los pacientes de cualquiera de los grupos de tratamiento en monoterapia (los resultados se muestran en la tabla a continuación). Después de 24 meses de tratamiento, también se observaron ventajas significativas con la administración de Enbrel en combinación con metotrexato, al compararla con la administración de ambos, Enbrel y metotrexato, como monoterapia.
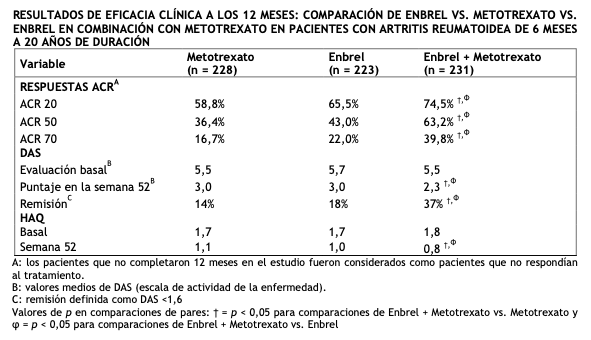
La progresión radiológica a los 12 meses fue significativamente inferior en el grupo de Enbrel que en el grupo de metotrexato, mientras que la combinación fue significativamente mejor que cualquiera de las dos monoterapias para retardar la progresión radiográfica (Ver figura a continuación).
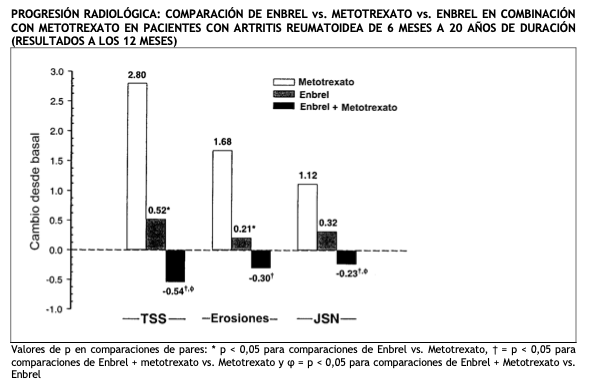
Después de 24 meses de tratamiento, también se observaron ventajas significativas con el tratamiento combinado de Enbrel y metotrexato en comparación con la administración de Enbrel o metotrexato en monoterapia. Asimismo se observaron ventajas significativas con la monoterapia de Enbrel en comparación con la monoterapia de metotrexato después de 24 meses. En un análisis en el que se consideró que todos los pacientes que habían abandonado el estudio por cualquier motivo habían progresado, el porcentaje de pacientes sin progresión (variación en TSS ≤ 0,5) a los 24 meses fue superior en el grupo de Enbrel combinado con metotrexato que en los grupos de Enbrel solo y metotrexato solo (62 %, 50 % y 36 % respectivamente; p < 0,05). La diferencia entre Enbrel solo y metotrexato solo también fue significativa (p < 0,05). El índice de ausencia de progresión, entre los pacientes que completaron 24 meses de tratamiento en el estudio, fue del 78 %, 70 % y 61 %, respectivamente. Se evaluó la seguridad y eficacia de Enbrel 50 mg (dos inyecciones SC de 25 mg) administrado una vez por semana en un estudio doble ciego, controlado con placebo en 420 pacientes con artritis reumatoidea activa. En este estudio, 53 pacientes recibieron placebo, 214 pacientes recibieron 50 mg de Enbrel una vez por semana y 153 pacientes recibieron 25 mg de Enbrel dos veces por semana. El perfil de seguridad y eficacia de los dos regímenes de tratamiento con Enbrel fue similar a las 8 semanas en cuanto al efecto sobre los signos y síntomas de la artritis reumatoidea; los resultados de la semana 16 no mostraron comparabilidad (sin inferioridad) entre los dos regímenes. Una inyección única de 50 mg/ml de etanercept resultó ser bioequivalente a dos inyecciones simultáneas de 25 mg/ml. Pacientes adultos con artritis psoriásica: Se evaluó la eficacia de Enbrel en un estudio doble ciego, aleatorio y controlado con placebo en 205 pacientes con artritis psoriásica. Los pacientes tenían entre 18 y 70 años de edad y presentaban artritis psoriásica activa (≥ 3 articulaciones inflamadas y ≥ 3 articulaciones hiperestésicas) en por lo menos una de las siguientes formas: (1) compromiso interfalángico distal (IFD); (2) artritis poliarticular (ausencia de nódulos reumatoideos y presencia de psoriasis); (3) artritis mutilante; (4) artritis psoriásica asimétrica; o (5) anquilosis espondilítica. Los pacientes también presentaban psoriasis en placa con una lesión calificada como objetivo ≥ 2 cm de diámetro. Los pacientes habían sido tratados anteriormente con AINES (86 %), ARMES (80 %) y corticosteroides (24 %). Los pacientes en tratamiento estable con metotrexato durante ≥ 2 meses podían continuar con una dosis estable ≤ 25 mg/semana de metotrexato. Se administraron dosis de 25 mg de Enbrel (en base a los resultados de los estudios posológicos en pacientes con artritis reumatoidea) o placebo por vía SC dos veces por semana durante 6 meses. Al finalizar el estudio doble ciego, los pacientes podían ingresar a un estudio abierto de extensión a largo plazo por una duración total de hasta 2 años. Las respuestas clínicas se expresaron como porcentaje de pacientes que lograron respuestas ACR 20, 50 y 70 y porcentaje con mejoría en los Criterios de Respuesta en Artritis Psoriásica (PsARC). La siguiente tabla resume los resultados.
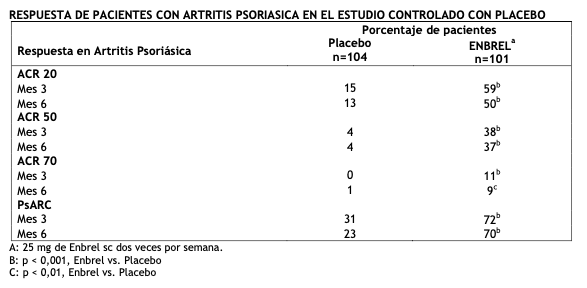
Entre los pacientes con artritis psoriásica tratados con Enbrel, se observaron respuestas clínicas en la primera visita (4 semanas) que se mantuvieron durante los 6 meses de tratamiento. Enbrel fue significativamente mejor que el placebo en todas las determinaciones de la actividad de la enfermedad (p < 0,001), observándose respuestas similares con y sin el tratamiento concomitante con metotrexato. Se evaluó la calidad de vida de los pacientes con artritis psoriásica en cada visita mediante el índice de discapacidad del HAQ. Los resultados del índice de discapacidad demostraron mejorías significativas en los pacientes con artritis psoriásica tratados con Enbrel, en relación con los tratados con placebo (p < 0,001), en todas las visitas de evaluación. En el estudio en artritis psoriásica se evaluaron los cambios radiológicos. Se obtuvieron radiografías de manos y muñecas en la visita basal, a los 6, 12 y 24 meses. El índice total de Sharp (TSS) modificado a los 12 meses se presenta en la Tabla a continuación. En un análisis en el que se consideró que todos los pacientes que habían abandonado el estudio por cualquier motivo habían progresado, el porcentaje de pacientes sin progresión (variación en TSS ≤ 0,5) a los 12 meses fue superior en el grupo de Enbrel que en el grupo de placebo (73 % vs. 47 % respectivamente; p ≤ 0,001). El efecto de Enbrel sobre la progresión radiológica se mantuvo en los pacientes que continuaron en tratamiento durante el segundo año. Se observó retardo del daño articular periférico en los pacientes con compromiso poliarticular simétrico de las articulaciones.

El tratamiento con Enbrel produjo una mejoría en la función física durante el período doble ciego y este beneficio se mantuvo durante la exposición más prolongada de hasta 2 años. No hay suficiente evidencia de la eficacia de Enbrel en pacientes con artropatías psoriásicas en forma de espondilitis anquilosante y artritis mutilante debido al pequeño número de pacientes estudiados. No se han realizado estudios en pacientes con artritis psoriásica con la dosis de 50 mg una vez por semana. La evidencia de la eficacia del régimen posológico una vez por semana en esta población de pacientes se basa en los resultados del estudio en pacientes con espondilitis anquilosante. Pacientes adultos con espondilitis anquilosante: Se evaluó la eficacia de Enbrel en la espondilitis anquilosante en tres estudios doble ciego y aleatorizados en los que se comparó la administración de 25 mg de Enbrel dos veces por semana con placebo. Se incorporó un total de 401 pacientes, de los cuales 203 recibieron Enbrel. El más amplio de estos estudios (n = 277) incluyó a pacientes con edades comprendidas entre 18 y 70 años y con espondilitis anquilosante activa definida como valores de la Escala Visual Analógica (VAS) ≥ 30 en el promedio de la intensidad y duración de la rigidez matinal más valores de VAS ≥ 30 en por lo menos dos de los siguientes tres parámetros: evaluación global por el paciente, promedio de valores de VAS para dorsalgia nocturna y dolor de espalda total; promedio de 10 preguntas en el Índice Funcional de Espondilitis Anquilosante de Bath (BASFI- Bath Ankylosing Spondylitis Functional Index). Los pacientes que tomaban ARMES, AINES o corticosteroides podían continuar con dosis estables de estos agentes. No se incluyeron pacientes con anquilosis completa de la columna lumbar en el estudio. Se administraron dosis subcutáneas de 25 mg de Enbrel (en base a los resultados de los estudios posológicos en pacientes con artritis reumatoidea) o placebo dos veces por semana durante 6 meses en 138 pacientes. La variable principal de eficacia (ASAS 20) fue una mejoría ≥ 20 % en por lo menos 3 de los 4 parámetros (evaluación global por el paciente, dolor de espalda, BASFI e inflamación) de Evaluación de la Espondilitis Anquilosante (ASAS - Assessment in Ankylosing Spondylitis) y ausencia de deterioro en los restantes parámetros. Se utilizaron los mismos criterios de 50 % ó 70 % de mejoría para las respuestas ASAS 50 y ASAS 70, respectivamente. En comparación con el placebo, el tratamiento con Enbrel produjo mejorías significativas en las respuestas ASAS 20, ASAS 50 y ASAS 70 a las 2 semanas de iniciado el tratamiento.
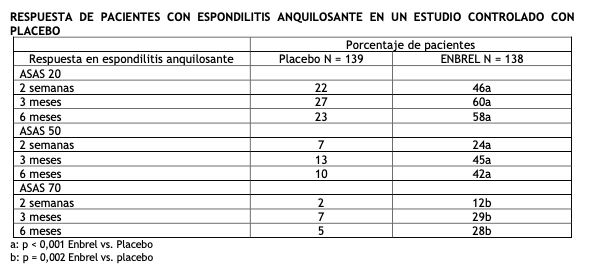
Entre los pacientes con espondilitis anquilosante que recibieron Enbrel, se observaron respuestas clínicas en la primera visita (2 semanas), manteniéndose durante los 6 meses de tratamiento. Se observaron respuestas similares en los pacientes que estaban o no estaban recibiendo tratamiento concomitante en la visita basal. Se obtuvieron resultados similares en los dos estudios más pequeños en espondilitis anquilosante. En un cuarto estudio doble ciego y controlado con placebo, se evaluó la seguridad y la eficacia de 50 mg de Enbrel (dos inyecciones SC de 25 mg) administrados una vez por semana versus 25 mg de Enbrel administrados dos veces por semana en 356 pacientes con espondilitis anquilosante activa. Se observaron perfiles similares de seguridad y de eficacia entre los regímenes de 50 mg una vez por semana y 25 mg dos veces por semana. Pacientes adultos con espondiloartritis axial no radiográfica: La eficacia de Enbrel en pacientes con espondiloartritis axial no radiográfica (SpAax-nr) se evaluó en un estudio aleatorizado, doble ciego, controlado con placebo, de 12 semanas de duración. En el estudio se evaluó a 215 pacientes adultos (población por intención de tratar modificada) con SpAax-nr activa (de entre 18 y 49 años), definida como aquellos pacientes que cumplían los criterios de clasificación de ASAS de la espondiloartritis axial, pero no cumplían los criterios de Nueva York modificados para el diagnóstico de EA. Los pacientes también debían presentar una respuesta inadecuada o intolerancia a dos o más AINEs. En el periodo doble ciego, los pacientes recibieron 50 mg semanales de Enbrel o placebo durante 12 semanas. La variable primaria de eficacia (ASAS 40) se definió como mejoría del 40% en al menos tres de los cuatro parámetros de ASAS y ausencia de deterioro en el parámetro restante. En la visita de inicio y en la semana 12, mediante resonancia magnética se obtuvieron imágenes de la articulación sacroilíaca y la columna vertebral con el fin de evaluar la inflamación. Al periodo doble ciego le siguió un periodo abierto en el que todos los pacientes recibieron 50 mg semanales de Enbrel durante un periodo de hasta 92 semanas adicionales. Comparado con placebo, el tratamiento con Enbrel dio como resultado mejorías estadísticamente significativas en las respuestas ASAS 40, ASAS 20 y ASAS 5/6. También se observó una mejoría significativa en las respuestas ASAS remisión parcial y BASDAI 50. En la tabla siguiente figuran los resultados de la semana 12.
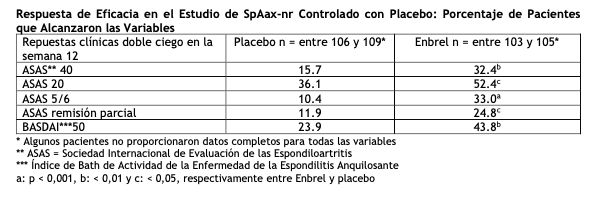
En la semana 12 se produjo una mejoría estadísticamente significativa en la puntuación SPARCC (Consorcio de Investigación de la Espondiloartritis de Canadá) para la articulación sacroilíaca, determinada mediante IRM, en los pacientes que recibían Enbrel. El cambio promedio ajustado desde la visita de inicio fue de 3,8 para los pacientes tratados con Enbrel (n = 95) frente a 0,8 para los pacientes tratados con placebo (n = 105) (p < 0,001). En la semana 104, el cambio promedio desde la visita de inicio en la puntuación SPARCC determinada mediante IRM para los pacientes tratados con Enbrel fue de 4,64 para la articulación sacroilíaca (n=153) y 1,40 para la columna vertebral (n=154). Comparado con placebo, Enbrel mostró una mejoría, desde la visita de inicio hasta la semana 12, estadística y significativamente mayor en la mayoría de las evaluaciones de calidad de vida relacionada con la salud y de la función física, incluyendo el BASFI (Índice Funcional de Bath de la Espondilitis Anquilosante), la puntuación de estado de salud global del cuestionario EuroQol 5D y la puntuación del componente físico del cuestionario SF- 36. Las respuestas clínicas entre los pacientes con SpAax-nr que recibieron Enbrel fueron evidentes en la primera visita (2 semanas) y se mantuvieron a lo largo de los 2 años de tratamiento. La mejoría en la calidad de vida relacionada con la salud y de la función física también se mantuvo a lo largo de los 2 años de tratamiento. Los datos a los 2 años no revelaron nuevos hallazgos sobre la seguridad. En la semana 104,8 los pacientes evolucionaron a una puntuación bilateral de grado 2 por rayos X en columna de acuerdo al sistema de graduación propuesto por los criterios de Nueva York modificados, indicativo de espondiloartropatía axial. Pacientes adultos con psoriasis en placa: Se recomienda el uso de Enbrel en la población de pacientes definida en el ítem Indicaciones. En la población de estudio, los pacientes que "no han respondido a" se definen como los que presentan una respuesta insuficiente (PASI < 50 o PGA menos que bueno), o un empeoramiento de la enfermedad durante el tratamiento, y que han recibido una dosis adecuada durante un periodo de tiempo lo suficientemente largo como para evaluar la respuesta a al menos cada una de las 3 principales terapias sistémicas disponibles. No se ha evaluado la eficacia de Enbrel frente a otras terapias sistémicas en pacientes con psoriasis de moderada a severa (que responden a otras terapias sistémicas) en estudios que comparen directamente Enbrel con otras terapias sistémicas. Se evaluó la seguridad y eficacia de Enbrel en cuatro estudios aleatorios, doble ciego y controlados con placebo en pacientes con psoriasis en placa. La variable principal de eficacia en los cuatro estudios fue la proporción de pacientes en cada grupo de tratamiento que alcanzó un PASI 75 (es decir, por lo menos una mejoría del 75 % en el resultado del Índice de Área y Severidad de la Psoriasis [PASI - Psoriasis Area and Severity Index] desde el valor basal) a las 12 semanas. El Estudio 1 fue un estudio de Fase 2 en pacientes ≥ 18 años con psoriasis en placa activa pero clínicamente estable y ≥ 10 % del área de superficie corporal afectada. Se distribuyeron en forma aleatoria 112 pacientes para recibir dosis de 25 mg de Enbrel (n = 57) o placebo (n = 55) dos veces por semana durante 24 semanas. El Estudio 2 evaluó a 652 pacientes con psoriasis en placa crónica empleando los mismos criterios de inclusión que el Estudio 1, con el agregado de un índice mínimo de área y severidad de la psoriasis (PASI) de 10 en el momento de la selección. Enbrel se administró en dosis de 25 mg una vez por semana, 25 mg dos veces por semana ó 50 mg dos veces por semana durante 6 meses consecutivos. Durante las primeras 12 semanas del período de tratamiento doble ciego, los pacientes recibieron placebo o una de las tres dosis de Enbrel mencionadas. Luego de 12 semanas de tratamiento, los pacientes del grupo de placebo comenzaron el tratamiento ciego con Enbrel (25 mg dos veces por semana); los pacientes en los grupos de tratamiento activo continuaron con la misma dosis a la que habían sido originalmente asignados en forma aleatoria hasta la semana 24. El Estudio 3 evaluó a 583 pacientes con los mismos criterios de inclusión que el Estudio 2. Los pacientes en este estudio recibieron una dosis de 25 mg ó 50 mg de Enbrel o placebo dos veces por semana durante 12 semanas y luego todos recibieron tratamiento abierto con 25 mg de Enbrel dos veces por semana durante otras 24 semanas. El estudio 4 evaluó 142 pacientes y tuvo los mismos criterios de inclusión que los estudios 2 y 3. Los pacientes en este estudio recibieron en la fase abierta una dosis de 50 mg de Enbrel o placebo una vez a la semana, durante 12 semanas; posteriormente todos los pacientes del estudio pasaron a una fase abierta en la que recibieron 50 mg de Enbrel una vez a la semana durante 12 semanas adicionales. En el Estudio 1 se observó una proporción significativamente mayor de pacientes con respuesta PASI 75 en el grupo tratado con Enbrel (30 %) en comparación con el grupo tratado con placebo (2 %) (p < 0,0001) en la semana 12. A las 24 semanas, el 56% de los pacientes tratados con Enbrel había alcanzado el PASI 75 versus el 5 % de los pacientes que recibieron placebo. A continuación se presentan los resultados más importantes de los estudios 2, 3 y 4:
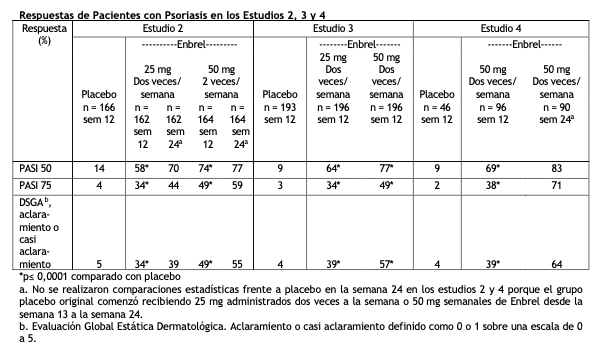
Se observaron respuestas significativas entre los pacientes con psoriasis en placa que recibieron Enbrel en relación al grupo de placebo en el momento de la primera visita (Semana 2), manteniéndose durante las 24 semanas de tratamiento. El Estudio 2 también tuvo un período libre de droga durante el cual se suspendió el tratamiento a los pacientes que alcanzaron una mejoría PASI de por lo menos el 50 % en la semana 24. Se mantuvo observación de los pacientes durante este período por la aparición de rebote (PASI ≥ 150 % del basal) y lapso hasta una recaída (definida como una pérdida de por lo menos la mitad de la mejoría lograda entre la visita basal y la semana 24). Durante el período de supresión del tratamiento, los síntomas de la psoriasis retornaron en forma gradual con un tiempo promedio hasta la recurrencia de la enfermedad de 3 meses. No se observaron brotes de rebote ni eventos adversos serios relacionados con la psoriasis. Se obtuvieron algunos indicios como para avalar un beneficio de la reanudación del tratamiento con Enbrel en pacientes que respondieron inicialmente al mismo. En el Estudio 3, la mayoría de los pacientes (77 %) que inicialmente fueron aleatorizados a 50 mg dos veces por semana reduciéndoseles la dosis de Enbrel a 25 mg dos veces por semana en la semana 12, mantuvieron su respuesta PASI 75 durante las 36 semanas. En los pacientes que recibieron 25 mg dos veces por semana durante todo el estudio, la respuesta PASI 75 continuó mejorando entre las semanas 12 y 36. En el estudio 4, el grupo tratado con Enbrel tuvo una proporción superior de pacientes con PASI 75 en la semana 12 (38%) en comparación con el grupo tratado con placebo (2%) (p < 0,0001). Para pacientes que recibieron 50 mg una vez a la semana a lo largo del estudio, las respuestas de eficacia siguieron mejorando y el 71% alcanzaron el PASI 75 en la semana 24. En los estudios abiertos a largo plazo (hasta 34 semanas) donde se administró ENBREL sin interrupción, se mantuvieron las respuestas clínicas y la seguridad fue similar a la de los estudios a corto plazo. Un análisis de los datos de los estudios clínicos no reveló ninguna característica basal de la enfermedad que ayudara a los médicos a seleccionar la opción de dosificación más apropiada (intermitente o continua). En consecuencia, la elección de la terapia intermitente o continua deberá basarse según criterio médico y las necesidades individuales del paciente. Anticuerpos frente a Enbrel: Se detectaron anticuerpos frente a etanercept en el suero de algunos sujetos tratados con etanercept. Estos anticuerpos eran todos no neutralizantes y generalmente transitorios. No parece que exista relación entre el desarrollo de anticuerpos y la respuesta clínica o los efectos adversos. En los sujetos tratados con dosis aprobadas de etanercept en los estudios clínicos de hasta 12 meses, las tasas acumulativas de anticuerpos anti-etanercept fueron de aproximadamente el 6% de los sujetos con artritis reumatoidea, el 7,5% de los sujetos con artritis psoriásica, el 2% de los sujetos con espondilitis anquilosante, el 7% de los sujetos con psoriasis, 9,7 % de los sujetos con psoriasis pediátrica y el 4,8% de los sujetos con artritis idiopática juvenil. La proporción de sujetos que desarrollaron anticuerpos frente a etanercept en estudios a largo plazo (de hasta 3,5 años) aumenta con el tiempo, según se esperaba. Sin embargo, debido a su naturaleza transitoria, la incidencia de anticuerpos detectados en cada punto de evaluación fue normalmente inferior al 7% en sujetos con artritis reumatoidea y sujetos con psoriasis. En un estudio de psoriasis a largo plazo en el que los pacientes recibieron 50 mg dos veces por semana durante 96 semanas, la incidencia de anticuerpos observada en cada punto de evaluación fue de hasta aproximadamente el 9%. Población pediátrica: Pacientes pediátricos con artritis idiopática juvenil (AIJ): Se evaluó la seguridad y eficacia de etanercept en un estudio dividido en dos partes en 69 niños con artritis idiopática juvenil poliarticular que presentaban distintas formas de comienzo de artritis idiopática juvenil (poliartritis, pauciartritis y de aparición sistémica). Se seleccionaron pacientes de entre 4 y 17 años con artritis idiopática juvenil poliarticular activa de intensidad moderada a severa, refractarios o con intolerancia al metotrexato. Se permitieron dosis estables de un solo antiinflamatorio no esteroide y/o prednisona (≤ 0,2 mg/kg/día ó 10 mg máximo). En la primera parte del estudio, todos los pacientes recibieron dosis de 0,4 mg/kg (máximo 25 mg por dosis) de etanercept por vía subcutánea dos veces por semana. En la segunda parte, los pacientes con respuesta clínica al cabo de 90 días fueron asignados al azar para seguir recibiendo etanercept o para recibir placebo durante 4 meses y fueron evaluados para detección de exacerbaciones de la enfermedad. Las respuestas se evaluaron mediante la Definición de Mejoría de la AIJ, definida como una mejoría ≥ 30 % en por lo menos 3 de los 6 criterios de evaluación para la AIJ y un deterioro ≥ 30 % en no más de 1 de los 6 criterios: recuento de articulaciones activas, limitación de la movilidad, evaluación global por el paciente/padres, evaluación global del médico, evaluación funcional y eritrosedimentación. La exacerbación de la enfermedad se estableció como ≥ 30 % de deterioro en 3 de los 6 criterios para la evaluación de la AIJ y ≥ 30 % de mejoría en no más de 1 de los 6 criterios y un mínimo de 2 articulaciones activas. En la primera parte del estudio, 51 (74 %) de los 69 pacientes presentaron una respuesta clínica favorable e ingresaron a la segunda parte. En esta segunda fase, 6 (24 %) de 25 pacientes que recibían etanercept manifestaron una exacerbación de la enfermedad contra 20 (77 %) de 26 pacientes del grupo de placebo (p = 0,007). El tiempo medio hasta la exacerbación, desde el comienzo de la segunda fase, fue ≥ 116 días en los pacientes tratados con etanercept y de 28 días en los pacientes del grupo de placebo. Cada componente de los criterios para la evaluación de la AIJ empeoró en el brazo de placebo y permaneció estable o mejoró en el brazo que continuó con etanercept. Estos datos indicaron la posibilidad de un mayor índice de exacerbaciones en aquellos pacientes con eritro-sedimentación basal más elevada. De los pacientes con respuesta clínica a los 90 días que ingresaron a la segunda parte del estudio, algunos del grupo de etanercept continuaron mejorando desde el mes 3 hasta el mes 7, mientras que los pacientes que recibieron placebo no mejoraron. En un estudio de extensión de seguridad abierto, 58 pacientes provenientes del estudio anteriormente descrito (de 4 años de edad en el momento de su inclusión en el estudio) continuaron recibiendo Enbrel durante un periodo de hasta 10 años. La tasa de efectos adversos y de infecciones serias no aumentó con la exposición a largo plazo. La seguridad a largo plazo del tratamiento con Enbrel en monoterapia (n=103), Enbrel en combinación con metotrexato (n=294), o metotrexato en monoterapia (n=197) fue evaluada durante un periodo de 3 años a partir de un registro de 594 niños con artritis idiopática juvenil de edades comprendidas entre 2 y 18 años, 39 de los cuales tenían de 2 a 3 años. En general, se notificaron más frecuentemente infecciones en los pacientes tratados con etanercept en comparación con aquellos que estaban en tratamiento con metotrexato en monoterapia (3,8% frente a un 2%), siendo las infecciones asociadas con el uso de etanercept de naturaleza más seria. En otro estudio de fase abierta y de un solo brazo, 60 pacientes con oligoartritis extendida (15 pacientes de edades entre 2 y 4 años, 23 pacientes de edades entre 5 y 11 años y 22 pacientes de edades entre 12 y 17 años), 38 pacientes con artritis relacionada con entesitis (de edades entre 12 y 17 años), y 29 pacientes con artritis psoriásica (de edades entre 12 y 17 años) fueron tratados con Enbrel a dosis de 0,8 mg/kg (hasta un máximo de 50 mg por dosis) una vez a la semana y durante un periodo de 12 semanas. En cada uno de los subtipos de AIJ, la mayoría de los pacientes cumplieron los criterios ACR Pedi 30 y demostraron una mejoraría clínica en las variables secundarias, tales como el número de articulaciones dolorosas y la evaluación global del médico. El perfil de seguridad fue consistente con el observado en otros estudios de AIJ. No se han realizado estudios en pacientes con artritis idiopática juvenil poliarticular para evaluar los efectos de la continuación del tratamiento con Enbrel en pacientes que no responden dentro de los 3 meses de iniciado el tratamiento con Enbrel. Además, tampoco se han realizado estudios para evaluar los efectos de la interrupción del tratamiento o reducción de la dosis recomendada de Enbrel tras su uso a largo plazo en pacientes con AIJ. Pacientes pediátricos con psoriasis en placa: Se evaluó la eficacia de ENBREL en un estudio aleatorizado, doble ciego y controlado con placebo en 211 pacientes pediátricos de 4 a 17 años con psoriasis en placa moderada a severa (según lo definido por un puntaje ≥ 3 en la sPGA, con ≥ 10 % del área de superficie corporal afectada y PASI ≥ 12). Los pacientes seleccionados habían recibido fototerapia o tratamiento sistémico o estaban controlados en forma insatisfactoria con tratamiento tópico. Los pacientes recibieron 0,8 mg/kg (hasta 50 mg) de ENBREL o Placebo una vez por semana durante 12 semanas. En la semana 12, una mayor proporción de pacientes aleatorizados a ENBREL que a placebo presentó respuestas positivas de eficacia (por ej., PASI 75).

Después del período de tratamiento doble ciego de 12 semanas, todos los pacientes que ingresaron al período de tratamiento abierto recibieron 0,8 mg/kg (hasta 50 mg) de ENBREL una vez por semana durante otras 24 semanas. Las respuestas observadas durante el período abierto fueron similares a las observadas en el período doble ciego. Durante un período aleatorizado libre de droga, una proporción significativamente mayor de pacientes realeatorizados a placebo, presentaron recaída (pérdida de respuesta PASI 75) en comparación con los pacientes realeatorizados a ENBREL. Con la continuación del tratamiento, las respuestas se mantuvieron hasta 48 semanas. La seguridad y eficacia de Enbrel 0,8 mg/kg (hasta 50 mg) una vez a la semana, fue evaluada en un estudio de extensión de fase abierta con 181 pacientes pediátricos con psoriasis en placa durante un período de 2 años, así como en el estudio de 48 semanas descrito anteriormente. La experiencia a largo plazo con Enbrel fue generalmente comparable a la del estudio original de 48 semanas, y no reveló ningún hallazgo nuevo de seguridad. Farmacocinètica: Absorción: La absorción del etanercept desde el sitio de la inyección subcutánea es lenta, alcanzando la concentración máxima en aproximadamente 48 horas después de la administración de una dosis única. La biodisponibilidad absoluta es del 76 %. Con dosis administradas dos veces a la semana, se prevé que las concentraciones en el estado de equilibrio estacionario sean aproximadamente dos veces más elevadas que las observadas después de dosis únicas. Después de una dosis subcutánea única de 25 mg de Enbrel, la concentración sérica máxima media observada en voluntarios sanos fue de 1,65 ± 0.66 mg/ml, y el área bajo la curva (ABC) fue de 235 ± 96,6 mg•h/ml. Alcanzado el estado estacionario, las medias de los perfiles de concentración sérica en los pacientes con artritis reumatoidea tratados fueron Cmax de 2,4 mg/l frente a 2,6 mg/l, Cmin de 1,2 mg/l vs 1,4 mg/l y el área bajo la curva (ABC) parcial de 297 mgh/l vs 316 mgh/l para 50 mg de Enbrel una vez a la semana (n=21) vs 25 mg de Enbrel dos veces a la semana (n=16), respectivamente. En un estudio abierto, cruzado, dos brazos de tratamiento, de dosis única, en voluntarios sanos, etanercept administrado como una inyección única de 50 mg/ml resultó ser bioequivalente a dos inyecciones simultáneas de 25 mg/ml. En un análisis farmacocinético poblacional realizado en pacientes con espondilitis anquilosante, las ABCs en estado de estacionario de etanercept fueron de 466 mg•h/ml y 474 mg•h/ml, en el caso de 50 mg de Enbrel administrado una vez a la semana (N=154) y 25 mg de Enbrel administrados dos veces a la semana (N=148), respectivamente. Distribución: Para describir la curva concentración - tiempo de etanercept, se requiere una curva biexponencial. El volumen central de distribución de etanercept es 7,6 l, mientras que el volumen de distribución en el estado estacionario es de 10,4 l. Eliminación: La eliminación de etanercept del organismo es lenta. La vida media de eliminación es de aproximadamente 70 horas. El clearance en pacientes con artritis reumatoidea es de aproximadamente 0,066 l/h, algo inferior al valor de 0,11 l/h observado en voluntarios sanos. Además, la farmacocinética de Enbrel en pacientes con artritis reumatoidea, espondilitis anquilosante y psoriasis en placas es similar. Aparentemente, no existe diferencia farmacocinética entre hombres y mujeres. Linealidad: La proporcionalidad de la dosis no ha sido formalmente evaluada, pero no hay saturación aparente del clearance a lo largo del rango de dosis. Poblaciones Especiales: Pacientes con disfunción renal: Si bien se detecta eliminación de radioactividad en la orina despu
és de la administración de etanercept radiomarcado a pacientes y voluntarios, no se detectó aumento de las concentraciones de etanercept en pacientes con insuficiencia renal aguda. La presencia de disfunción renal no requiere ajustes posológicos. Pacientes con disfunción hepática: En pacientes con insuficiencia hepática aguda no se observó un aumento de las concentraciones de etanercept. La presencia de insuficiencia hepática no requiere un cambio en la dosificación. Pacientes de edad avanzada: El impacto de la edad avanzada en la farmacocinética se ha estudiado en un análisis de las concentraciones séricas de etanercept en esta población. El clearance y volumen estimados, en pacientes entre 65 y 87 años, fueron similares a los de los pacientes menores de 65 años de edad. Población pediátrica: Pacientes pediátricos con artritis idiopática juvenil: En un estudio con Enbrel en artritis idiopática juvenil de curso poliarticular se administró a 69 pacientes (de edades entre 4 y 17 años), 0,4 mg de Enbrel/kg dos veces a la semana durante 3 meses. Los perfiles de concentraciones séricas fueron similares a los encontrados en pacientes adultos con artritis reumatoidea. Los niños de menor edad (4 años de edad) presentaron una reducción en el clearance (el clearance aumentó cuando se normalizó por el peso) comparado con los niños de mayor edad (12 años de edad) y adultos. La simulación de dosis sugiere que mientras los niños mayores (10-17 años de edad) tendrán niveles séricos cercanos a los observados en adultos, los niños menores tendrán niveles apreciablemente más bajos. Pacientes pediátricos con psoriasis en placas: Se administró 0,8 mg/kg (hasta un máximo de dosis de 50 mg por semana) de etanercept una vez a la semana hasta un máximo de 48 semanas, a pacientes pediátricos con psoriasis en placas (de 4 a 17 años). El rango medio de concentraciones séricas en estado de equilibrio fue de 1,6 a 2,1 mcg/ml a las 12, 24 y 48 semanas. Estas concentraciones medias en pacientes pediátricos con psoriasis en placas fueron similares a las concentraciones observadas en pacientes con artritis idiopática juvenil (tratados con 0,4 mg/kg de etanercept dos veces a la semana, hasta un máximo de dosis de 50 mg por semana) Estas concentraciones medias fueron similares a las observadas en pacientes adultos con psoriasis en placa tratados con 25 mg de etanercept dos veces a la semana. Datos preclínicos sobre seguridad: En los estudios toxicológicos con Enbrel, no se observó toxicidad dependiente de la dosis o en el órgano diana. A partir de una batería de estudios in vitro e in vivo se llegó a la conclusión de que Enbrel no era genotóxico. Debido al desarrollo de anticuerpos neutralizantes en roedores, no se realizaron estudios de carcinogenicidad ni valoraciones estándar de la fertilidad y toxicidad postnatal con Enbrel. Enbrel no induce letalidad o signos notables de toxicidad en el ratón o en la rata después de una dosis única subcutánea de 2000 mg/kg o después de una dosis única intravenosa de 1000 mg/kg. Enbrel no muestra toxicidad dosis limitante u órgano específica en el mono cynomolgus después de administraciones subcutáneas, dos veces en semana durante 4 o 26 semanas consecutivas a una dosis (15 mg/kg) que resulta en un área bajo curva (ABC) basada en concentraciones séricas del fármaco que fueron unas 27 veces mayores que las que se obtienen en humanos a la dosis recomendada de 25 mg.
Indicaciones.
Artritis reumatoidea: Enbrel, en combinación con metrotrexato, está indicado para el tratamiento de la artritis reumatoidea activa moderada a severa en adultos, cuando la respuesta a fármacos antirreumáticos que modifican la enfermedad, incluido metotrexato (a no ser que esté contraindicado), ha sido inadecuada. Enbrel puede administrarse como monoterapia en caso de intolerancia a metotrexato o cuando el tratamiento continuo con metotrexato no sea apropiado. Enbrel también está indicado para el tratamiento de la artritis reumatoidea progresiva, activa y severa en adultos que no han sido tratados previamente con metotrexato. Enbrel, solo o en combinación con metotrexato, ha demostrado reducir la tasa de progresión del daño de las articulaciones, medido a través de análisis radiológico, así como mejorar la función física. Artritis idiopática juvenil: Tratamiento de la poliartritis (con factor reumatoideo positivo o negativo) y la oligoartritis extendida en niños a partir de 2 años y adolescentes que han tenido una respuesta inadecuada, o que tienen una intolerancia probada, al metotrexato. Tratamiento de la artritis psoriásica en adolescentes a partir de 12 años que han tenido una respuesta inadecuada, o que tienen una intolerancia probada, al metotrexato. Tratamiento de la artritis relacionada con entesitis en adolescentes a partir de 12 años que han tenido una respuesta inadecuada, o que tienen una intolerancia probada, al tratamiento convencional. Enbrel no ha sido estudiado en niños menores de 2 años. Artritis psoriásica: Tratamiento de la artritis psoriásica activa y progresiva en adultos cuando la respuesta a una terapia previa con fármacos antirreumáticos modificadores de la enfermedad, ha sido inadecuada. Se ha demostrado que Enbrel mejora la función física en pacientes con artritis psoriásica, y que reduce la tasa de progresión del daño de las articulaciones periféricas, medido a través de análisis radiológico, en pacientes con subtipos poliarticulares simétricos de la enfermedad. Espondiloartritis axial: Espondilitis anquilosante (EA): Tratamiento de la espondilitis anquilosante activa severa en adultos que no han tenido una respuesta adecuada a la terapia convencional. Espondiloartritis axial no radiográfica: Tratamiento de la espondiloartritis axial no radiográfica grave en adultos con signos objetivos de inflamación, como elevación de la proteína C-reactiva y/o Imagen por Resonancia Magnética (IRM), que han tenido una respuesta inadecuada a los antiinflamatorios no esteroides (AINEs). Psoriasis en placa: Tratamiento de adultos con psoriasis en placa de moderada a severa que no han respondido o que tienen contraindicada, o no toleran otra terapia sistémica incluyendo ciclosporina, metotrexato o psoraleno y luz ultravioleta A (PUVA). Psoriasis pediátrica en placa: Tratamiento de psoriasis en placa crónica severa en niños a partir de 6 años y adolescentes que no están controlados adecuadamente o son intolerantes a otras terapias sistémicas o fototerapias.
Dosificación.
Artritis reumatoidea: 25 mg de Enbrel administrados dos veces a la semana es la dosis recomendada. Alternativamente, una dosis de 50 mg administrada una vez a la semana ha demostrado ser segura y efectiva (ver Propiedades Farmacodinámicas). Artritis psoriásica, espondilitis anquilosante y espondiloartritis axial no radiográfica: La dosis recomendada de Enbrel es de 25 mg administrados dos veces a la semana o de 50 mg administrados una vez a la semana. Para todas las indicaciones mencionadas anteriormente, los datos disponibles sugieren que la respuesta clínica se consigue, por lo general, dentro de las primeras 12 semanas de tratamiento. La continuación del tratamiento debe ser reconsiderada cuidadosamente si el paciente no ha respondido en este periodo de tiempo. Psoriasis en placas: La dosis recomendada de Enbrel es de 25 mg administrados dos veces a la semana o 50 mg administrados una vez a la semana. Alternativamente, pueden ser administrados 50 mg dos veces a la semana durante un periodo máximo de 12 semanas, seguidos, si es necesario, de una dosis de 25 mg dos veces a la semana o 50 mg una vez a la semana. El tratamiento con Enbrel debe continuar hasta conseguir la remisión, durante un periodo máximo de 24 semanas. La terapia continua más allá de 24 semanas puede ser apropiada para algunos pacientes adultos (ver Propiedades Farmacodinámicas). El tratamiento debe ser discontinuado en pacientes en los que no se observe respuesta después de 12 semanas. Si una repetición del tratamiento con Enbrel está indicada, deben seguirse las mismas pautas sobre la duración del tratamiento. La dosis debe ser 25 mg dos veces a la semana o 50 mg una vez a la semana. Poblaciones especiales: Pacientes con insuficiencia renal y hepática: No se requiere ajuste de la dosis. Personas de edad avanzada: No se requiere ajuste de la dosis. La posología y administración es la misma que la de adultos de 18-64 años de edad. Población pediátrica: Artritis idiopática juvenil: La dosis recomendada es de 0,4 mg/kg (hasta un máximo de 25 mg por dosis) dos veces a la semana, mediante inyección subcutánea, con un intervalo entre dosis de 3-4 días, o de 0,8 mg/kg (hasta un máximo de 50 mg por dosis) una vez a la semana. Se debe considerar la interrupción del tratamiento en pacientes en los que no se observe respuesta después de 4 meses. No se han llevado a cabo estudios clínicos formales en niños de 2 a 3 años. Sin embargo, los escasos datos de seguridad disponibles de un registro de pacientes sugieren que el perfil de seguridad en niños de 2 a 3 años es similar al observado en adultos y en niños a partir de 4 años, cuando se les trata con 0,8 mg/kg a la semana por vía subcutánea (ver Propiedades Farmacodinámicas). Psoriasis pediátrica en placas (a partir de 6 años de edad): La dosis recomendada es de 0,8 mg/kg (hasta un máximo de 50 mg por dosis) una vez a la semana durante un periodo máximo de 24 semanas. El tratamiento debe ser discontinuado en pacientes en los que no se observe respuesta después de 12 semanas. Si está indicada una repetición del tratamiento con Enbrel, deben seguirse las pautas sobre la duración del mismo anteriormente indicadas. La dosis debe ser 0,8 mg/kg (hasta un máximo de 50 mg por dosis) una vez a la semana. Forma de administración: Enbrel es administrado mediante una inyección subcutánea. Al final del prospecto se facilitan instrucciones detalladas para la administración (ver Instrucciones para la preparación y administración de la inyección).
Contraindicaciones.
Hipersensibilidad a etanercept o a alguno de los componentes de la formulación. Sepsis o riesgo de sepsis (ver Advertencias y Precauciones especiales de uso y Reacciones adversas) Enbrel no debe administrarse en pacientes con infecciones activas serias, crónicas o localizadas.
Reacciones adversas.
Resumen del perfil de seguridad: Las reacciones adversas notificadas con mayor frecuencia son reacciones en la zona de inyección (tales como dolor, hinchazón, picor, enrojecimiento y sangrado en el lugar de punción), infecciones (tales como infecciones del tracto respiratorio alto, bronquitis, infecciones vesicales e infecciones cutáneas), reacciones alérgicas, desarrollo de autoanticuerpos, picor y fiebre. Se han notificado también reacciones adversas graves con Enbrel. Los antagonistas de FNT, como Enbrel, afectan al sistema inmune, y su utilización puede afectar a las defensas del organismo frente a infecciones y cáncer. Las infecciones graves afectan a menos de 1 de cada 100 pacientes tratados con Enbrel. Las notificaciones incluyen infecciones mortales y potencialmente mortales y sepsis. También se han notificado varias neoplasias con el uso de Enbrel, incluyendo cánceres de mama, pulmón, piel y ganglios linfáticos (linfoma). Así mismo también se han notificado reacciones hematológicas, neurológicas y autoinmunes graves. Estas incluyen casos raros de pancitopenia, y casos muy raros de anemia aplásica. Con el uso de Enbrel, también se han observado casos raros o muy raros de desmielinización central y periférica, respectivamente. También ha habido notificaciones de lupus, enfermedades relacionadas con lupus y vasculitis. Listado tabulado de reacciones adversas: El siguiente listado de reacciones adversas se basa en la experiencia de los estudios clínicos en adultos y en la experiencia post-comercialización. Dentro de la clasificación por órganos y sistemas, las reacciones adversas están listadas por frecuencia (número de pacientes que se espera experimenten la reacción), utilizando las siguientes categorías: muy frecuentes (≥1/10); frecuentes (≥1/100 a < 1/10); poco frecuentes (≥1/1.000 a < 1/100); raras (≥1/10.000 a < 1/1.000); muy raras ( < 1/10.000); frecuencia no conocida (no puede estimarse a partir de los datos disponibles).
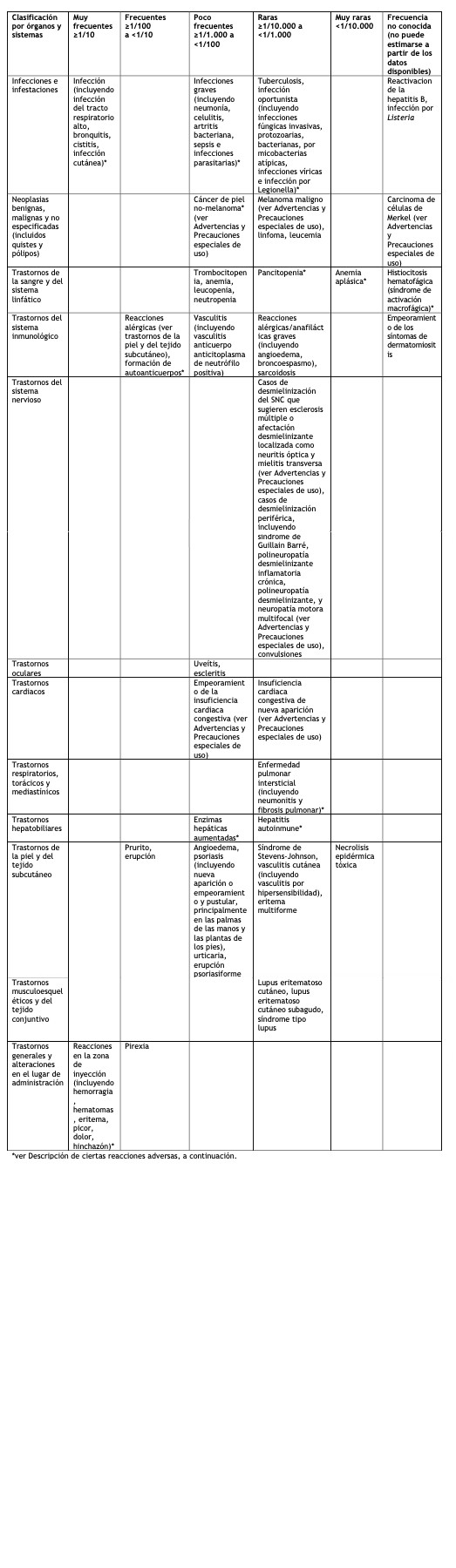
Descripción de ciertas reacciones adversas: Neoplasias y trastornos linfoproliferativos: Se observaron ciento veintinueve (129) nuevas neoplasias de distintos tipos en 4.114 pacientes con artritis reumatoidea tratados con enbrel en estudios clínicos de hasta 6 años de duración aproximadamente, incluyendo 231 pacientes tratados con enbrel en combinación con metotrexato en el estudio de 2 años controlado con comparador activo. Los porcentajes e incidencias en estos estudios clínicos fueron similares a los esperados para la población estudiada. Se notificaron un total de dos casos de neoplasias en los estudios clínicos de aproximadamente 2 años de duración, en los que había 240 pacientes con artritis psoriásica tratados con enbrel. En los estudios clínicos llevados a cabo durante más de dos años con 351 pacientes con espondilitis anquilosante, se notificaron 6 casos de neoplasias en pacientes tratados con enbrel. En un grupo de 2.711 pacientes con psoriasis en placas tratados con enbrel, en estudios doble ciego y abiertos de hasta 2,5 años de duración, se notificaron 30 neoplasias y 43 cánceres de piel no-melanoma En un grupo de 7.416 pacientes tratados con Enbrel en estudios clínicos en artritis reumatoidea, artritis psoriásica, espondilitis anquilosante y psoriasis se notificaron 18 linfomas. Durante el periodo post-comercialización, se han recibido notificaciones de varias neoplasias (incluyendo cáncer de mama y pulmón y linfoma) (ver Advertencias y Precauciones especiales de uso). Reacciones en la zona de inyección: Los pacientes con enfermedades reumatológicas tratados con Enbrel tuvieron una incidencia de reacciones en la zona de inyección significativamente mayor que los pacientes tratados con placebo (36% frente a 9%). Las reacciones en la zona de inyección ocurrieron normalmente en el primer mes. La duración media fue aproximadamente de 3 a 5 días. En los grupos tratados con Enbrel, la mayoría de las reacciones en la zona de inyección no fueron tratadas; de los pacientes a los que se les administró tratamiento, la mayoría recibió preparaciones tópicas, tales como corticosteroides, o antihistamínicos orales. Adicionalmente, algunos pacientes desarrollaron reacciones de recuerdo en la zona de inyección, caracterizadas por una reacción cutánea en la zona de inyección más reciente, así como por la aparición simultánea de reacciones en zonas de inyección previas. Estas reacciones fueron generalmente transitorias y no se repitieron con el tratamiento. En los estudios controlados en pacientes con psoriasis en placas, aproximadamente el 13,6% de los pacientes tratados con Enbrel desarrollaron reacciones en la zona de inyección durante las primeras 12 semanas de tratamiento, frente al 3,4% de los pacientes tratados con placebo. Infecciones graves: En los estudios clínicos controlados con placebo, no se observó aumento alguno en la incidencia de infecciones graves (con resultado de muerte, potencialmente mortales o que requieren hospitalización o la administración de antibióticos por vía intravenosa). Las infecciones graves ocurrieron en un 6,3% de los pacientes con artritis reumatoidea tratados con Enbrel durante un periodo de tiempo de hasta 48 meses. Estas incluyeron abscesos (en diferentes lugares), bacteriemia, bronquitis, bursitis, celulitis, colecistitis, diarrea, diverticulitis, endocarditis (sospecha), gastroenteritis, hepatitis B, herpes zoster, úlcera en piernas, infección bucal, osteomielitis, otitis, peritonitis, neumonía, pielonefritis, sepsis, artritis séptica, sinusitis, infección cutánea, úlcera cutánea, infección del tracto urinario, vasculitis e infección de heridas. En el estudio controlado con comparador activo de 2 años de duración, donde los pacientes eran tratados con Enbrel en monoterapia, con metotrexato en monoterapia o con Enbrel combinado con metotrexato, las tasas de infecciones graves fueron similares entre los grupos de tratamiento. Sin embargo, no se puede excluir que la combinación de Enbrel con metotrexato pudiera estar asociada con un incremento en la tasa de infecciones. En los estudios clínicos controlados con placebo de hasta 24 semanas de duración, en psoriasis en placas, no hubo diferencias en las tasas de infección entre los pacientes tratados con Enbrel y los tratados con placebo. Las infecciones graves ocurridas en pacientes tratados con Enbrel incluyen celulitis, gastroenteritis, neumonía, colecistitis, osteomielitis, gastritis, apendicitis, fascitis por estreptococos, miositis, shock séptico, diverticulitis y abscesos. En los estudios doble ciego y abiertos en artritis psoriásica, se notificó un caso de 1 paciente que presentó una infección grave (neumonía). Durante el uso de Enbrel se han notificado infecciones graves y mortales; los patógenos identificados incluyen bacterias, micobacterias (incluyendo tuberculosis), virus y hongos. Algunas se produjeron a las pocas semanas después de iniciar el tratamiento con Enbrel en pacientes que, además de su artritis reumatoidea, presentaban enfermedades subyacentes (por ejemplo, diabetes, insuficiencia cardiaca congestiva, antecedentes de infecciones activas o crónicas) (ver Advertencias y Precauciones especiales de uso). El tratamiento con Enbrel puede incrementar la mortalidad en pacientes con sepsis demostrada. Se han notificado infecciones oportunistas en asociación con Enbrel, incluyendo infecciones fúngicas invasivas, parasitarias (incluyendo las infecciones protozoarias), víricas (incluyendo herpes zoster) bacterianas (incluyendo las producidas por Listeria y Legionella) y por micobacterias atípicas. En un conjunto de datos de estudios clínicos, la incidencia global de infecciones oportunistas fue del 0,09% para los 15.402 sujetos que recibieron Enbrel. La tasa ajustada por exposición fue de 0,06 acontecimientos por 100 pacientes-año. Durante la experiencia post-comercialización, aproximadamente la mitad de todos los casos clínicos de infecciones oportunistas en todo el mundo fueron infecciones fúngicas invasivas. Las infecciones fúngicas invasivas más comúnmente notificadas fueron por Candida, Pneumocystis, Aspergillus e Histoplasma. Las infecciones fúngicas invasivas explicaron más de la mitad de las muertes de los pacientes que desarrollaron infecciones oportunistas. La mayoría de los casos con desenlace de muerte fueron en pacientes con Pneumocystis pneumoniae, infecciones fúngicas sistémicas no especificadas y aspergilosis (ver Advertencias y Precauciones especiales de uso). Autoanticuerpos: En pacientes adultos, se analizaron muestras de suero en distintos puntos de los estudios para la determinación de autoanticuerpos. De los pacientes con artritis reumatoidea evaluados, el porcentaje de pacientes que desarrollaron nuevos ANA positivos (≥ 1:40) fue superior en los pacientes tratados con Enbrel (11%) que en los tratados con placebo (5%). El porcentaje de pacientes que desarrolló nuevos anticuerpos positivos anti ADN de doble cadena fue también superior por radioinmunoensayo (15% de los pacientes tratados con Enbrel frente al 4% de los pacientes tratados con placebo) y con el estudio Crithidia luciliae (3% de los pacientes tratados con Enbrel frente a ningún paciente de los tratados con placebo). La proporción de pacientes tratados con Enbrel que desarrollaron anticuerpos anticardiolipina aumentó de forma similar en comparación con los pacientes tratados con placebo. No se conoce el impacto del tratamiento a largo plazo con enbrel sobre el desarrollo de enfermedades autoinmunes. Ha habido casos raros de pacientes, incluyendo pacientes con factor reumatoidea positivo, que han desarrollado otros autoanticuerpos junto a un síndrome tipo lupus o a erupciones compatibles clínicamente, y tras la realización de biopsia, con lupus cutáneo subagudo o lupus discoide. Pancitopenia y anemia aplásica: Durante el periodo post-comercialización, se han notificado casos de pancitopenia y anemia aplásica, algunos de los cuales tuvieron desenlace de muerte (ver Advertencias y Precauciones especiales de uso). Enfermedad pulmonar intersticial: En los estudios clínicos controlados de etanercept para todas las indicaciones, la frecuencia (porcentaje de incidencia) de enfermedad pulmonar intersticial en pacientes que estaban recibiendo etanercept sin tratamiento concomitante con metotrexato fue del 0,06% (frecuencia rara). En los estudios clínicos controlados que permitieron el tratamiento concomitante con etanercept y metotrexato, la frecuencia (porcentaje de incidencia) de enfermedad pulmonar intersticial fue del 0,47% (frecuencia poco frecuente). Durante el periodo post-comercialización, se han notificado casos de enfermedad pulmonar intersticial (incluyendo neumonitis y fibrosis pulmonar), algunos de los cuales tuvieron desenlace de muerte. Tratamiento concomitante con anakinra: En los estudios en los que pacientes adultos recibieron tratamiento concomitante con Enbrel y anakinra, se observó una tasa superior de infecciones graves en comparación con los que recibieron sólo Enbrel, y un 2% de los pacientes (3/139) desarrollaron neutropenia (recuento de neutrófilos totales < 1.000/mm3). Durante la fase neutropénica, un paciente desarrolló celulitis que se resolvió tras su hospitalización (ver secciones Advertencias y Precauciones especiales de uso e Interacciones). Enzimas hepáticas aumentadas: En los periodos de doble ciego de los estudios clínicos controlados de etanercept para todas las indicaciones, la frecuencia (porcentaje de incidencia) de acontecimientos adversos de enzimas hepáticas aumentadas en pacientes que estaban recibiendo etanercept sin tratamiento concomitante con metotrexato fue del 0,54% (frecuencia poco frecuente). En los periodos de doble ciego de los estudios clínicos controlados que permitieron el tratamiento concomitante con etanercept y metotrexato, la frecuencia (porcentaje de incidencia) de acontecimientos adversos de enzimas hepáticas aumentadas fue del 4,18% (frecuencia frecuente). Hepatitis autoinmune: En los estudios clínicos controlados de etanercept para todas las indicaciones, la frecuencia (porcentaje de incidencia) de hepatitis autoinmune en pacientes que estaban recibiendo etanercept sin tratamiento concomitante con metotrexato fue del 0,02% (frecuencia rara). En los estudios clínicos controlados que permitieron el tratamiento concomitante con etanercept y metotrexato, la frecuencia (porcentaje de incidencia) de hepatitis autoinmune fue del 0,24% (frecuencia poco frecuente). Población pediátrica: Reacciones adversas en pacientes pediátricos con artritis idiopática juvenil: En general, las reacciones adversas en pacientes pediátricos con artritis idiopática juvenil fueron similares en frecuencia y tipo, a las observadas en pacientes adultos. En los siguientes párrafos se comentan las diferencias con adultos y otras consideraciones especiales. Los tipos de infecciones observados en los estudios clínicos realizados en pacientes de edades comprendidas entre 2 y 18 años, con artritis idiopática juvenil, fueron generalmente de leves a moderados y concordaban con los comúnmente observados en la población pediátrica ambulatoria. Entre las reacciones adversas graves notificadas se incluyen varicela con signos y síntomas de meningitis aséptica que se resolvió sin secuelas (ver Advertencias y Precauciones especiales de uso), apendicitis, gastroenteritis, depresión/trastornos de personalidad, úlcera cutánea, esofagitis/gastritis, shock séptico por estreptococos del grupo A, diabetes mellitus tipo I, e infección en tejidos blandos y en heridas post-operatorias. En un estudio realizado en niños con artritis idiopática juvenil, de edades comprendidas entre 4 y 17 años, 43 de 69 niños (62%) experimentaron una infección mientras recibían Enbrel durante 3 meses de estudio (Parte 1, fase abierta), y la frecuencia y gravedad de las infecciones fue similar en los 58 pacientes que completaron los 12 meses de la fase de extensión abierta. Los tipos y la proporción de acontecimientos adversos en pacientes con artritis idiopática juvenil fueron similares a las observadas en los estudios con Enbrel en pacientes adultos con artritis reumatoidea, siendo la mayoría de carácter leve. Varios acontecimientos adversos se notificaron con más frecuencia en 69 pacientes con artritis idiopática juvenil que recibieron Enbrel durante 3 meses, en comparación con los 349 pacientes adultos con artritis reumatoidea. Estos incluyen cefalea (19% de los pacientes, 1,7 acontecimientos por paciente año), náuseas (9%, 1,0 acontecimientos por paciente año), dolor abdominal (19%, 0,74 acontecimientos por paciente año) y vómitos (13%, 0,74 acontecimientos por paciente año). Se notificaron 4 casos de síndrome de activación macrofágica en estudios clínicos en artritis idiopática juvenil. Durante el periodo post-comercialización, se han notificado casos de enfermedad inflamatoria intestinal y uveítis en pacientes con AIJ en tratamiento con Enbrel, entre los que se incluyen un número muy pequeño de casos que experimentaron una recuperación positiva tras interrumpir el tratamiento (ver Advertencias y Precauciones especiales de uso). Reacciones adversas en pacientes pediátricos con psoriasis en placas.: En un estudio de 48 semanas en 211 niños de edades entre 4 y 17 años, con psoriasis pediátrica en placas, los acontecimientos adversos notificados fueron similares a los observados en estudios anteriores en adultos con psoriasis en placas.estudios Reportes de reacciones adversas sospechosas: Es importante reportar las reacciones adversas luego de la autorización de venta del producto medicinal. Permite continuar monitoreando el balance riesgo/beneficio del producto medicinal. Se les solicita a los profesionales de la salud que reporten cualquier reacción adversa, siguiendo los lineamientos locales del país.
Advertencias.
Infecciones: Se debe evaluar la posibilidad de infección en el paciente antes, durante y después del tratamiento con Enbrel, teniendo en cuenta que la media de la semivida de eliminación de etanercept es aproximadamente 70 horas (rango 7 a 300 horas). Se han notificado infecciones graves, sepsis, tuberculosis, e infecciones oportunistas, incluyendo infecciones fúngicas invasivas, listeriosis y legionelosis con el uso de Enbrel (ver Reacciones Adversas). Estas infecciones se debieron a bacterias, micobacterias, hongos, virus y parásitos (incluyendo protozoos). En algunos casos no se han detectado infecciones fúngicas particulares y otras infecciones oportunistas, dando como resultado el retraso en el tratamiento apropiado y en ocasiones la muerte. En la valoración de los pacientes para determinar la presencia de infecciones, debe considerarse el riesgo para el paciente de padecer infecciones oportunistas relevantes (por ejemplo, exposición a micosis endémicas). Debe monitorizarse estrechamente a los pacientes que desarrollen una nueva infección mientras están en tratamiento con Enbrel. Debe suspenderse la administración de Enbrel si un paciente desarrolla una infección grave. No han sido evaluadas la seguridad y eficacia de Enbrel en pacientes con infecciones crónicas Los médicos deben extremar las precauciones cuando consideren el uso de Enbrel en pacientes con historial de infecciones crónicas o recurrentes o con trastornos subyacentes que pudieran predisponer a los pacientes a infecciones, tales como diabetes avanzada o mal controlada. Tuberculosis: Se han notificado casos de tuberculosis activa, incluyendo tuberculosis miliar, y tuberculosis con localización extra-pulmonar en pacientes en tratamiento con Enbrel. Se debe evaluar a los pacientes para un posible diagnóstico de tuberculosis activa o inactiva ("latente") antes de empezar el tratamiento con Enbrel. Esta evaluación debe incluir una historia médica detallada con una historia personal de tuberculosis o un posible contacto previo con la tuberculosis y previas y/ o actuales terapias inmunosupresivas. Los estudios de detección adecuados, por ejemplo análisis de tuberculina en piel y radiografía de tórax, deben realizarse a todos los pacientes (deben aplicarse las recomendaciones locales). Se recomienda que se registre en la tarjeta de alerta para el paciente la realización de estas pruebas. Se recuerda a los prescriptores del riesgo de un resultado falso negativo en la prueba de tuberculina en piel, especialmente en pacientes que están gravemente enfermos o inmunocomprometidos. No se debe iniciar la terapia con Enbrel si se diagnostica una tuberculosis activa. Si se diagnostica una tuberculosis inactiva ("latente"), debe iniciarse un tratamiento para la tuberculosis latente con una terapia anti-tuberculosis antes del inicio del tratamiento con Enbrel, y de acuerdo a las recomendaciones locales. En esta situación, el balance riesgo/ beneficio de la terapia con Enbrel debe ser considerado cuidadosamente. Se debe informar a todos los pacientes que deben consultar con su médico si aparecen signos o síntomas que sugieran tuberculosis (por ejemplo tos persistente, pérdida de peso, febrícula) durante o después del tratamiento con Enbrel. Reactivación de la hepatitis B: Se ha notificado la reactivación de hepatitis B en pacientes que estuvieron previamente infectados por el virus de la hepatitis B (VHB) y habían recibido tratamiento concomitante con antagonistas del FNT, incluyendo Enbrel. Estas notificaciones incluyen casos de reactivación de hepatitis B en pacientes que eran anticuerpos antiHBc positivos, pero antígeno HBs negativos. Se deberá realizar un análisis al paciente para determinar la presencia de infección por el VHB antes de iniciar tratamiento con Enbrel. En el caso de los pacientes cuyo resultado para la infección por VHB sea positivo, se recomienda consultar a un médico especialista en el tratamiento de la hepatitis B. Debe actuarse con precaución cuando se administre Enbrel a pacientes previamente infectados por el VHB. Se debe monitorizar a estos pacientes durante todo el tratamiento, y durante varias semanas después de finalizarlo, para detectar síntomas y signos de una infección activa por VHB. No se dispone de datos adecuados de pacientes infectados por VHB y tratados con antivirales en combinación con antagonistas FNT. En los pacientes que desarrollen una infección por VHB, se debe interrumpir el tratamiento con Enbrel e iniciarse un tratamiento antiviral efectivo junto con el tratamiento de apoyo apropiado. Empeoramiento de la hepatitis C: Se han notificado casos de empeoramiento de la hepatitis C en pacientes en tratamiento con Enbrel. Se debe utilizar Enbrel con precaución en pacientes con historial de hepatitis C. Tratamiento concomitante con anakinra: La administración concomitante de Enbrel y anakinra se ha asociado con un riesgo incrementado de infecciones graves y neutropenia en comparación con la administración sola de Enbrel. Esta combinación no ha demostrado incremento del beneficio clínico. Por tanto, no se recomienda el uso combinado de Enbrel y anakinra (ver Interacciones y Reacciones Adversas). Tratamiento concomitante con abatacept: En los estudios clínicos, la administración concomitante de abatacept y Enbrel dio como resultado un incremento de la incidencia de las reacciones adversas graves. Esta combinación no ha demostrado un beneficio clínico incrementado; tal uso no se recomienda (ver Interacciones). Reacciones alérgicas: Se han observado con frecuencia reacciones alérgicas asociadas a la administración de Enbrel. Las reacciones alérgicas han incluido angioedema y urticaria: se han producido reacciones graves. Si se produce cualquier reacción alérgica o anafiláctica grave, la terapia con Enbrel debe interrumpirse inmediatamente y comenzar una terapia apropiada. El capuchón de la aguja de la jeringa prellenada contiene látex (goma seca natural), el cual puede causar reacciones de hipersensibilidad, cuando se manipula o se administra Enbrel a personas con una sensibilidad conocida o potencial al látex. Inmunosupresión: Existe la posibilidad de que los antagonistas FNT, incluyendo Enbrel, afecten a las defensas del huésped frente a infecciones y neoplasias, ya que el FNT es un mediador de la inflamación y modula la respuesta inmune celular. En un estudio con 49 pacientes adultos con artritis reumatoidea tratados con Enbrel, no hubo evidencia de depresión de hipersensibilidad de tipo retardado, disminución de los niveles de inmunoglobulinas o cambio en el número de poblaciones de células efectoras. Dos pacientes con artritis idiopática juvenil desarrollaron infección por varicela y signos y síntomas de meningitis aséptica que se resolvieron sin secuelas. Los pacientes con una exposición significativa al virus de la varicela deben interrumpir temporalmente el tratamiento con Enbrel y debe considerarse el tratamiento profiláctico con inmunoglobulina de varicela Zoster. La seguridad y eficacia de Enbrel en pacientes con inmunosupresión no han sido evaluadas. Neoplasias y trastornos linfoproliferativos: Neoplasias sólidas y hematopoyéticas (excluyendo cánceres de piel): Se han notificado varias neoplasias (incluyendo cáncer de mama y pulmón y linfoma) en el periodo de post comercialización (ver Reacciones Adversas). En las partes controladas de los estudios clínicos de los antagonistas del FNT, se han observado más casos de linfomas entre los pacientes que recibieron un antagonista del FNT en comparación con el grupo control. Sin embargo, la incidencia fue rara, y el periodo de seguimiento de los pacientes con placebo fue más corto que el de los pacientes que recibían el tratamiento con el antagonista del FNT. En el periodo post-comercialización, se han notificado casos de leucemia en pacientes tratados con antagonistas del FNT. Existe un mayor riesgo basal de linfomas y leucemia en pacientes con artritis reumatoidea con enfermedad inflamatoria, de larga evolución y de alta actividad, que complica la estimación del riesgo. Sobre la base del conocimiento actual, no se puede excluir un posible riesgo de desarrollo de linfomas, leucemia u otras neoplasias hematopoyéticas o de tumores sólidos en pacientes tratados con un antagonista del FNT. Se debe tener precaución cuando se considera la terapia con antagonistas del FNT para pacientes con una historia de neoplasia o cuando se considera continuar el tratamiento en pacientes que desarrollen una neoplasia. En el periodo de post-comercialización, se han notificado neoplasias, algunas mortales, en niños, adolescentes y adultos jóvenes (hasta 22 años de edad) tratados con antagonistas del FNT (inicio de la terapia ≤ 18 años de edad), incluyendo Enbrel. Aproximadamente la mitad de los casos eran linfomas. Los otros casos representaban una variedad de diferentes neoplasias e incluían neoplasias raras normalmente asociadas con inmunosupresión. No puede excluirse un riesgo de desarrollo de neoplasias en niños y adolescentes tratados con antagonistas del FNT. Cánceres de piel: Se han notificado melanomas y cáncer de piel no melanoma (CPNM) en pacientes tratados con antagonistas del FNT, incluyendo Enbrel. De manera muy infrecuente, se han notificado casos post comercialización de carcinoma de células de Merkel en pacientes tratados con Enbrel. Se recomienda un examen cutáneo periódico de todos los pacientes, especialmente de aquellos con factores de riesgo de cáncer de piel. Combinando los resultados de estudios clínicos controlados, se observaron más casos de NMSC en los pacientes que recibieron Enbrel en comparación con los pacientes control, particularmente en los pacientes con psoriasis. Vacunas: No deben administrarse vacunas vivas simultáneamente con Enbrel. No se dispone de datos sobre la transmisión secundaria de la infección por vacunas vivas en pacientes que reciben Enbrel. En un estudio clínico doble ciego, aleatorizado, controlado con placebo 184 pacientes adultos con artritis psoriásica también recibieron una vacuna polisacárida neumocócica multivalente en la semana 4. En este estudio la mayoría de los pacientes con artritis psoriásica que recibieron Enbrel fueron capaces de generar una respuesta inmune efectiva de células B a la vacuna polisacárida neumocócica, pero los títulos en conjunto fueron moderadamente inferiores y pocos pacientes duplicaron los títulos en comparación con pacientes que no recibieron Enbrel de lo cual se desconoce el significado clínico. Formación de autoanticuerpos: El tratamiento con Enbrel puede producir la formación de anticuerpos autoinmunes (ver Reacciones Adversas). Reacciones hematológicas: En pacientes tratados con Enbrel se han notificado raramente casos de pancitopenia y muy raramente casos de anemia aplásica, algunos con resultado mortal. Se debe tener precaución en pacientes tratados con Enbrel los cuales tengan un historial de discrasias sanguíneas. Todos los pacientes y los padres/cuidadores deben ser advertidos de que si el paciente desarrolla signos y síntomas que sugieren la existencia de discrasias sanguíneas o infecciones (como por ejemplo, fiebre persistente, odinofagia, hematomas, sangrado, palidez) mientras están tratándose con Enbrel deben informar inmediatamente a su médico. Estos pacientes deberán ser estudiados urgentemente incluyendo un recuento de células sanguíneas completo. Si se confirma una discrasia sanguínea, se deberá interrumpir el tratamiento con Enbrel. Trastornos neurológicos: Ha habido, muy ocasionalmente, informes de trastornos desmielinizantes del SNC en pacientes tratados con Enbrel (ver Reacciones Adversas). Además, en raras ocasiones, ha habido informes de polineuropatías desmielinizantes periféricas (incluidos síndrome de Guillain-Barré, polineuropatía desmielinizante inflamatoria crónica, polineuropatía desmielinizante y neuropatía motora multifocal). Aunque no se han desarrollado estudios clínicos para evaluar el tratamiento con Enbrel en pacientes con esclerosis múltiple, los estudios clínicos de otros antagonistas del FNT en pacientes con esclerosis múltiple han mostrado un incremento en la actividad de la enfermedad. Cuando se prescriba Enbrel a pacientes con enfermedad desmielinizante preexistente o de reciente comienzo, o a aquellos que se considere que tienen un riesgo incrementado de desarrollar enfermedad desmielinizante, se recomienda una cuidadosa evaluación del riesgo beneficio, incluyendo una evaluación neurológica. Terapia combinada: En un estudio clínico controlado de dos años de duración en pacientes adultos con artritis reumatoidea, la combinación de Enbrel y metotrexato, no evidenció hallazgos inesperados sobre la seguridad, y el perfil de seguridad de Enbrel cuando se administra con metotrexato fue similar a los perfiles notificados en los estudios de Enbrel y metotrexato solos. Están en marcha estudios a largo plazo para evaluar la seguridad de la combinación. La seguridad a largo plazo cuando Enbrel se administra en combinación con otros fármacos antirreumáticos modificadores de la enfermedad (FARMEs), no ha sido establecida. No se ha estudiado el uso de Enbrel en combinación con otras terapias sistémicas o fototerapia para el tratamiento de la psoriasis. Insuficiencia renal y hepática: Basado en datos farmacocinéticos (ver Propiedades Farmacocinéticas), en pacie
ntes con insuficiencia renal o hepática, no se requiere ajuste de dosis; la experiencia clínica en este tipo de pacientes es limitada. Insuficiencia cardiaca congestiva: Los médicos deben tener precaución cuando se use Enbrel en pacientes que tienen insuficiencia cardiaca congestiva (ICC). Ha habido informes post comercialización sobre empeoramiento de la ICC, con y sin factores de precipitación identificables, en pacientes que están tomando Enbrel. También se han observado casos raros ( < 0,1%) de ICC de novo, incluyendo ICC en pacientes sin enfermedad cardiovascular preexistente conocida. Algunos de estos pacientes tenían menos de 50 años de edad. Dos grandes estudios clínicos en los que se estaba evaluando el uso de Enbrel en el tratamiento de la ICC terminaron antes de tiempo debido a la falta de eficacia. Aunque no es concluyente, los datos de uno de estos estudios sugieren una posible tendencia al empeoramiento de la ICC en aquellos pacientes asignados al tratamiento con Enbrel. Hepatitis alcohólica: En un estudio fase II, aleatorizado, controlado con placebo de 48 pacientes hospitalizados tratados con Enbrel o placebo para hepatitis alcohólica moderada a grave, Enbrel no fue eficaz y la tasa de mortalidad en los pacientes tratados con Enbrel fue significativamente superior tras 6 meses. En consecuencia, Enbrel no debe usarse en pacientes para el tratamiento de la hepatitis alcohólica. Los médicos deben tener cuidado cuando utilicen Enbrel en pacientes que también tienen hepatitis alcohólica moderada a grave. Granulomatosis de Wegener: En un estudio controlado con placebo, en el que 89 pacientes adultos fueron tratados con Enbrel en adición a la terapia estándar (incluyendo ciclofosfamida o metotrexato y glucocorticoides) para una duración media de 25 meses, no se ha demostrado que Enbrel sea un tratamiento eficaz para la granulomatosis de Wegener. La incidencia de neoplasias no cutáneas de diferentes tipos fue significativamente más elevada en pacientes tratados con Enbrel que en pacientes del grupo de control. No se recomienda Enbrel para el tratamiento de la granulomatosis. Hipoglucemia en pacientes tratados para la diabetes: En pacientes que reciben medicación para la diabetes, se ha observado hipoglucemia tras el inicio del tratamiento con Enbrel, necesitándose una reducción de la medicación antidiabética en algunos de estos pacientes. Poblaciones especiales: Personas de edad avanzada: En un estudio fase III en artritis reumatoidea, artritis psoriásica y espondilitis anquilosante, no hubo diferencias globales en reacciones adversas, reacciones adversas graves e infecciones graves en pacientes de 65 años o mayores que han recibido Enbrel en comparación con pacientes más jóvenes. De todas formas, se debe tener precaución cuando se trata a pacientes de edad avanzada y con particular atención con respecto a la ocurrencia de infecciones. Población pediátrica: Vacunas: Se recomienda que, si es posible, los pacientes pediátricos sean vacunados de acuerdo a los calendarios de vacunación previstos, antes de iniciar el tratamiento con Enbrel (ver más arriba el apartado de Vacunas). Enfermedad inflamatoria intestinal (EII) y uveítis en pacientes con artritis idiopática juvenil (AIJ): Se han notificado casos de EII y uveítis en pacientes con AIJ que estaban en tratamiento con Enbrel (ver Reacciones Adversas).
Interacciones.
Tratamiento concomitante con anakinra: Se ha observado que los pacientes adultos en tratamiento con Enbrel y anakinra tienen una tasa superior de infecciones graves en comparación con los pacientes en tratamiento sólo con Enbrel o sólo con anakinra (datos históricos). Además, en un estudio doble ciego, controlado con placebo realizado en pacientes adultos que estaban en tratamiento con metotrexato, se ha observado que en los pacientes en tratamiento con Enbrel y anakinra la tasa de infecciones graves (7%) y neutropenia fue superior a la de los pacientes en tratamiento con Enbrel (ver Advertencias y Precauciones especiales de uso y Reacciones Adversas). La combinación Enbrel y anakinra no ha demostrado un mayor beneficio clínico y por tanto no se recomienda su uso. Tratamiento concomitante con abatacept: En los estudios clínicos, la administración concomitante de abatacept y Enbrel dio como resultado un incremento de la incidencia de las reacciones adversas graves. Esta combinación no ha demostrado un beneficio clínico incrementado; tal uso no se recomienda (ver Advertencias y Precauciones especiales de uso). Tratamiento concomitante con sulfasalazina: En un estudio clínico con pacientes adultos que estaban recibiendo una dosis establecida de sulfasalazina, a la cual se le añadió Enbrel, los pacientes en el grupo de combinación experimentaron una disminución estadísticamente significativa en el recuento medio de glóbulos blancos en comparación con los grupos tratados con Enbrel o sulfasalazina solos. El significado clínico de esta interacción es desconocido. Los médicos deben tener cuidado cuando consideren el tratamiento combinado con sulfasalazina. Sin interacción: En estudios clínicos, no se han observado interacciones cuando Enbrel se administró con glucocorticoides, salicilatos, (excepto sulfasalazina), antiinflamatorios no esteroideos (AINEs), analgésicos o metotrexato. Para recomendaciones de vacunación (ver Advertencias y Precauciones especiales de uso). No se han observado interacciones farmacocinéticas clínicamente significativas entre medicamentos en estudios con metotrexato, digoxina o warfarina. Fertilidad, embarazo y lactancia: Mujeres en edad fértil: Las mujeres en edad fértil deben considerar el uso de métodos anticonceptivos adecuados para evitar el embarazo durante el tratamiento con Enbrel y hasta 3 semanas después de interrumpir el tratamiento. Embarazo: En estudios de desarrollo de toxicidad llevados a cabo en ratas y conejos no se observó evidencia de daño fetal o neonatal en ratas debido a etanercept. Los efectos de etanercept sobre el embarazo se han investigado en dos estudios observacionales de cohortes. En un estudio observacional se observó una mayor tasa de defectos congénitos importantes al comparar los embarazos en los que existió una exposición a etanercept (n=370) durante el primer trimestre, frente a los embarazos en los que no existió exposición a etanercept ni a otros antagonistas del FNT (n=164) (razón de probabilidades ajustado: 2,4; IC del 95%: 1,0-5,5). Los tipos de defectos congénitos importantes fueron consistentes con los que se notificaron con mayor frecuencia en la población general, y no se identificaron patrones de anomalías concretos. No se observaron cambios en las tasas de abortos espontáneos, nacidos muertos o malformaciones leves. En otro estudio observacional de registros médicos de varios países que comparó el riesgo de resultados adversos del embarazo en mujeres tratadas con etanercept durante los primeros 90 días de embarazo (n = 425) con aquellas tratadas con medicamentos no biológicos (n = 3497), no se observó un aumento en el riesgo de defectos congénitos importantes (odds ratio [OR] sin ajustar = 1,22, IC del 95%: 0,79-1,90; OR ajustada = 0,96, IC del 95%: 0,58-1,60 tras el ajuste por país, enfermedad materna, número de partos, edad de la madre y tabaquismo al comienzo del embarazo). Este estudio también mostró que no se incrementaban los riesgos de defectos congénitos menores, parto prematuro, muerte fetal o infecciones en el primer año de vida de los bebés nacidos de mujeres tratadas con etanercept durante el embarazo. Enbrel sólo debe utilizarse durante el embarazo si es claramente necesario.Etanercept atraviesa la placenta y se ha detectado en el suero de niños nacidos de pacientes mujeres tratadas con Enbrel durante el embarazo. Se desconoce la repercusión clínica de este hecho; sin embargo, los lactantes pueden presentar un aumento del riesgo de infección. No se recomienda la administración de vacunas vivas a lactantes durante las 16 semanas siguientes a la última dosis de Enbrel administrada a la madre. Lactancia: Se ha notificado que etanercept se excreta en la leche materna tras la administración subcutánea. En ratas lactantes, tras la administración subcutánea, etanercept se excretó en la leche y se detectó en el suero de las crías. Debido a que, al igual que ocurre con otros muchos medicamentos, las inmunoglobulinas pueden ser excretadas en la leche materna, se debe decidir si es necesario interrumpir la lactancia o interrumpir el tratamiento con Enbrel, tras considerar el beneficio de la lactancia para el niño y el beneficio del tratamiento para la madre. Fertilidad: No se dispone de datos preclínicos sobre la toxicidad peri- y post-natal de etanercept, ni tampoco de los efectos de etanercept sobre la fertilidad y capacidad reproductiva. Efectos sobre la capacidad para conducir y utilizar máquinas: No se han realizado estudios sobre los efectos sobre la capacidad para conducir y utilizar máquinas.
Conservación.
Las jeringas prellenada de Enbrel deberán conservarse en heladera entre 2 °C y 8 °C. No congelar. Mantener las jeringas prellenadas de Enbrel en el estuche para protegerlas de la luz, hasta el momento de uso. No agitar. Después de retirar la jeringa de la heladera, espere aproximadamente 15-30 minutos para que la solución de Enbrel alcance la temperatura ambiente. No la caliente de ninguna otra forma. A continuación, se recomienda el uso inmediato. Ante la eventualidad de una sobredosificación, concurrir al Hospital más cercano o comunicarse con alguno de los Centros de Toxicología del país. Entre otros: Hospital de Pediatría Ricardo Gutiérrez: (011) 4962-6666/2247. Hospital A. Posadas: (011) 4654-6648/4658-7777. Hospital de Pediatría "Dr. Garrahan": (011) 4943-1455.
Sobredosificación.
En los estudios clínicos en pacientes con artritis reumatoide, no se observó toxicidad limitante de la dosis. La dosis más alta evaluada ha sido una dosis de carga inicial intravenosa de 32 mg/m2 seguida de dosis subcutánea de 16 mg/m2 administradas dos veces a la semana. Un paciente con artritis reumatoide se autoadministró por error 62 mg de Enbrel subcutáneo dos veces a la semana durante 3 semanas sin experimentar efectos adversos. No se conoce ningún antídoto para Enbrel. No se conoce ningún antídoto para la sobredosis de etanercept.
Presentación.
Cada estuche de Enbrel 25 mg contiene: 4 jeringas prellenadas de dosis única y 8 torundas (toallitas) impregnadas de alcohol. Cada estuche de Enbrel 50 mg contiene: 4 jeringas prellenadas de dosis única y 8 torundas (toallitas) impregnadas de alcohol.
Revisión.
Octubre 2019. LPD: 25/Feb/2019.

