Actemra®
ROCHE
Tocilizumab.
Agente inmunosupresor, inhibidor de interleucina.
Composición.
Cada ml de concentrado contiene 20 mg de tocilizumab (anticuerpo monoclonal IgG1 recombinante humanizado antirreceptor de interleucina-6 [IL-6] humana, producido en células de ovario de hámster chino mediante tecnología de ADN recombinante). Cada vial de 4 ml contiene 80 mg de tocilizumab, en un excipiente de polisorbato 80: 2 mg, sacarosa 200 mg, fosfato disódico dodecahidrato 6,11 mg, dihidrógeno fosfato de sodio dihidrato 6,70 mg y agua para inyectables c.s.p. 4 ml. Cada vial de 10 ml contiene 200 mg de tocilizumab, en un excipiente de polisorbato 80: 5 mg, sacarosa 500 mg, fosfato disódico dodecahidrato 15,3 mg, dihidrógeno fosfato de sodio dihidrato 16,8 mg y agua para inyectables c.s.p. 10 ml. Cada vial de 20 ml contiene 400 mg de tocilizumab, en un excipiente de polisorbato 80: 10 mg, sacarosa 1.000 mg, fosfato disódico dodecahidrato 30,5 mg, dihidrógeno fosfato de sodio dihidrato 33,5 mg y agua para inyectables c.s.p. 20 ml.
Farmacología.
Código ATC: L04AC07. Grupo farmacoterapéutico: Agentes inmunosupresores, inhibidores de interleucina. Propiedades farmacodinámicas: Mecanismo de acción: Tocilizumab se une específicamente a los receptores de IL-6 tanto solubles como unidos a membranas (IL-6Rs e IL-6Rm). Se ha demostrado que tocilizumab inhibe la señalización mediada por IL-6Rs e IL-6Rm. La IL-6 es una citocina proinflamatoria pleiotrópica producida por diversos tipos celulares, incluidas células T y B, los monocitos y los fibroblastos. La IL-6 participa en diferentes procesos fisiológicos como la activación de los linfocitos T, la inducción de secreción de inmunoglobulina, la inducción de síntesis hepática de proteínas de la fase aguda y la estimulación de la hemopoyesis. Se ha implicado a la IL-6 en la patogenia de enfermedades, tales como afecciones inflamatorias, osteoporosis y neoplasias. Pacientes con Artritis reumatoidea (AR): Efectos farmacodinámicos: En ensayos clínicos con tocilizumab, se observaron reducciones rápidas de la proteína C reactiva (PCR), la velocidad de sedimentación globular (VSG) y el amiloide A sérico (AAS). En forma coherente con el efecto sobre los reactantes de la fase aguda, el tratamiento con tocilizumab se asoció con disminución del recuento de plaquetas dentro del rango normal. Se verificaron aumentos de los niveles de hemoglobina, debidos a la reducción por tocilizumab de los efectos impulsados por la IL-6 sobre la producción de hepcidina para incrementar la disponibilidad del hierro. En pacientes tratados con tocilizumab, se registraron descensos de los niveles de PCR dentro de los valores normales ya a la segunda semana y éstos se mantuvieron mientras duraba el tratamiento. En voluntarios sanos a los que se administró tocilizumab en dosis de 2 a 28 mg/kg, el recuento absoluto de neutrófilos descendió a su nivel más bajo transcurridos de 2 a 5 días después de la administración. Posteriormente los niveles de neutrófilos se recuperaron hasta el valor basal de una manera dosis-dependiente. Los pacientes con artritis reumatoidea demostraron un patrón similar en el recuento absoluto de neutrófilos después de la administración de tocilizumab (véase Reacciones adversas). Eficacia clínica y seguridad: Se ha evaluado la eficacia de tocilizumab para aliviar los signos y síntomas de artritis reumatoidea en cinco ensayos aleatorizados, doble-ciego, multicéntricos. Los ensayos I - V incluyeron a pacientes ≥ 18 años de edad con artritis reumatoidea activa diagnosticada según los criterios del American College of Rheumatology (ACR) y que tenían por lo menos ocho articulaciones doloridas y seis inflamadas al inicio. En el ensayo I, tocilizumab se administró por vía intravenosa cada cuatro semanas como monoterapia y en los estudios II, III y V, por la misma vía cada cuatro semanas en combinación con MTX frente a placebo y MTX. En el estudio IV, tocilizumab se administró por vía intravenosa cada 4 semanas en combinación con otros FAMEs frente a placebo y otros FAMEs. El objetivo primario de los cinco estudios fue la proporción de pacientes que alcanzó respuesta ACR20 a la semana 24. En el ensayo I se evaluaron 673 pacientes que no habían sido tratados con MTX en los seis meses previos a la aleatorización y que no habían suspendido el tratamiento previo con MTX como consecuencia de efectos tóxicos clínicamente importantes o falta de respuesta. La mayoría (67%) no había recibido nunca MTX. Se administraron dosis de 8 mg/kg de tocilizumab cada cuatro semanas como monoterapia. El grupo de comparación recibió MTX semanal (dosis ajustada desde 7,5 mg a un máximo de 20 mg por semana durante un período de ocho semanas). En el ensayo II, un estudio de dos años con análisis planificados en las semanas 24, 52 y 104, se evaluaron 1.196 pacientes con una respuesta clínica inadecuada a MTX. Se administraron dosis de 4 u 8 mg/kg de tocilizumab o placebo cada cuatro semanas como terapia ciega durante 52 semanas en combinación con MTX estable (de 10 mg a 25 mg semanales). Después de 52 semanas todos los pacientes pudieron recibir tratamiento abierto con tocilizumab 8 mg/kg. De los pacientes que completaron el estudio, el 86% de los que inicialmente fueron asignados al grupo placebo + MTX recibió tratamiento abierto con tocilizumab 8 mg/kg en el segundo año. El objetivo primario en la semana 24 fue la proporción de pacientes que alcanzaron respuesta ACR20. Entre las semanas 52 y 104, los objetivos co-primarios fueron la prevención del daño articular y la mejora de la función física. En el ensayo III se evaluaron 623 pacientes con una respuesta clínica inadecuada a MTX. Se administraron dosis de 4 u 8 mg/kg de tocilizumab o placebo cada cuatro semanas, en combinación con MTX estable (de 10 mg a 25 mg semanales). En el ensayo IV se estudiaron 1.220 pacientes con una respuesta inadecuada a un tratamiento reumatológico instaurado, con uno o más FAMEs. Se administraron dosis de 8 mg/kg de tocilizumab o placebo cada cuatro semanas, en combinación con FAMEs estables. El ensayo V incluyó 499 pacientes con una respuesta clínica inadecuada o intolerancia a uno o más tratamientos antagonistas del TNF. Esta terapia se suspendió antes de la aleatorización. Se administraron dosis de 4 u 8 mg/kg de tocilizumab o placebo cada cuatro semanas, en combinación con MTX estable (de 10 mg a 25 mg semanales). El criterio de valoración primario para los estudios III-V fue la proporción de pacientes que alcanzó una respuesta ACR20 a la semana 24. El porcentaje de pacientes que logró respuestas ACR20, 50 y 70 en los estudios I a V se muestra en la Tabla 1. Respuesta clínica: En todos los ensayos, los pacientes tratados con tocilizumab 8 mg/kg tuvieron tasas de respuesta en ACR20, 50 y 70 significativamente mayores a los 6 meses comparados con control (Tabla 1). En el estudio I, se demostró la superioridad de tocilizumab 8 mg/kg frente al comparador activo MTX. El efecto del tratamiento fue similar en los pacientes, independientemente del factor reumatoide, edad, sexo, raza, número de terapias previas o estado de la enfermedad. El tiempo hasta al inicio de la acción fue rápido (ya a la semana 2) y la magnitud de la respuesta siguió mejorando con la duración del tratamiento. En los ensayos de extensión abiertos que están en marcha, I y V, se han registrado respuestas duraderas continuadas durante más de 3 años. En pacientes tratados con tocilizumab 8 mg/kg, se observaron mejorías significativas en todos los componentes individuales de la respuesta ACR, incluidos: recuentos de articulaciones doloridas e inflamadas; evaluación global por los pacientes y los médicos; puntuaciones del índice de discapacidad; evaluación del dolor y PCR en comparación con los pacientes que recibieron placebo más MTX / u otros FAMEs en todos los estudios. Los pacientes de los estudios I-V tenían un nivel medio de actividad de la enfermedad DAS28 de 6,5-6,8 al inicio. Se observó una reducción significativa (mejoría media), del nivel inicial DAS28 de 3,1-3,4 en los tratados con tocilizumab frente a los controles (1,3-2,1). La proporción de pacientes que alcanzó una remisión clínica DAS28 (DAS28 < 2,6), a las 24 semanas, fue significativamente mayor en los que recibieron tocilizumab (28-34%), comparado con los pacientes control (1-12%). En el ensayo II, un 65% logró un DAS28 < de 2,6 a la semana 104, comparado con un 48% que lo alcanzó en la semana 52 y un 33% en la semana 24. En un análisis conjunto de los estudios II, III y IV, la proporción de pacientes que alcanzó una respuesta ACR20, 50 y 70 fue significativamente mayor (59% frente al 50%, 37% frente a 27%, 18% frente a 11%, respectivamente) en el grupo de tocilizumab 8 mg/kg más FAMEs frente al grupo tratado con tocilizumab 4 mg/kg más FAMEs (p < 0,03). En forma similar, la proporción de pacientes que logró remisión en el DAS28 (DAS28 < 2,6) fue significativamente mayor (31% frente al 16%, respectivamente) en aquéllos que recibieron tocilizumab 8 mg/kg más FAMEs que en los tratados con tocilizumab 4 mg/kg más FAMEs (p < 0,0001).
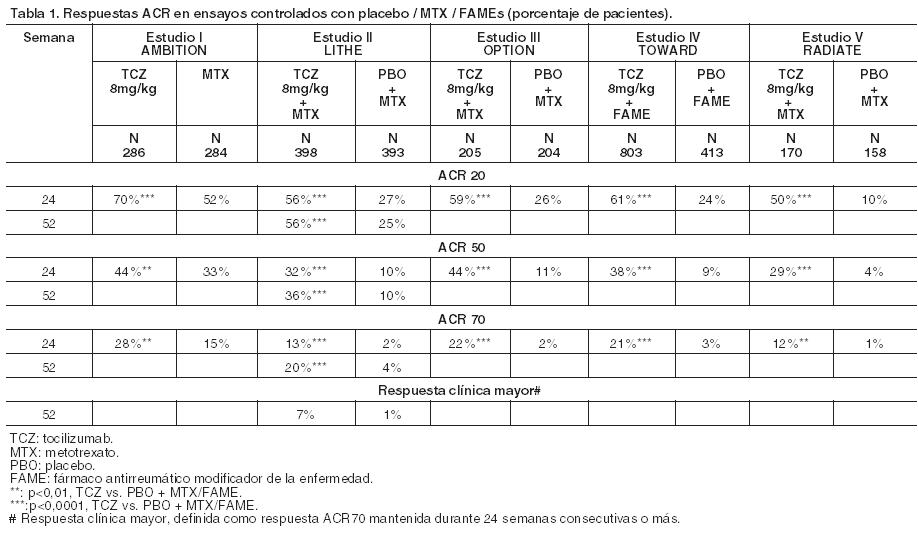
Respuesta clínica mayor: Después de dos años de tratamiento con tocilizumab y metotrexato, el 14% de los pacientes alcanzó una respuesta clínica mayor (mantenimiento de la respuesta ACR70 durante 24 semanas o más). Respuesta radiográfica: En el ensayo II, en pacientes con una respuesta inadecuada a MTX, se evaluó radiográficamente la inhibición del daño articular estructural y se expresó como un cambio en la escala de Sharp modificada y sus componentes, la puntuación de erosión y la del estrechamiento del espacio articular. Se demostró inhibición del daño estructural articular con una progresión radiográfica significativamente menor en los pacientes que recibieron tocilizumab en comparación con el control (Tabla 2). En la extensión abierta del estudio II la inhibición de la progresión del daño estructural en los pacientes tratados con tocilizumab más MTX se mantuvo en el segundo año del tratamiento. En la semana 104 el cambio medio desde la basal en el índice total Sharp-Genant fue significativamente menor en los pacientes del grupo tocilizumab 8 mg/kg más MTX (p < 0,0001) que en los del grupo placebo más MTX.
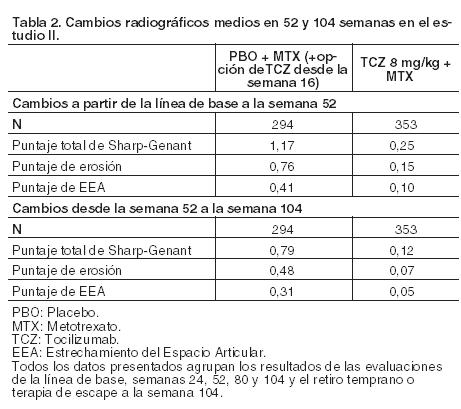
Después de un año de tratamiento con tocilizumab más MTX, el 85% de los pacientes (n = 348) no presentó progresión del daño estructural, definido por un cambio en el índice total de Sharp de cero o menos, comparado con el 67% de aquéllos tratados con placebo más MTX (n = 290) (p ≤0,0001). Estas cifras se mantuvieron coherentes después de dos años de tratamiento (83%; n = 353). El noventa y tres por ciento (93%; n = 271) de los pacientes no manifestó progresión entre las semanas 52 y 104. Resultados relacionados con la salud y la calidad de vida: Los pacientes tratados con tocilizumab comunicaron una mejora en todos los resultados notificados: Cuestionario de evaluación de la salud, Índice de Discapacidad (HAQ-DI), Formulario breve 36 (SF-36) y Evaluación funcional del tratamiento de enfermedades crónicas. Se observaron mejoras estadísticamente significativas en las puntuaciones de HAQ-DI en pacientes tratados con Actemra en comparación con aquellos que recibieron FAMEs. En la semana 24, la proporción de pacientes tratados con 8 mg/kg de tocilizumab que mostraron una mejoría importante en HAQ-DI (definida como una disminución de la puntuación total individual de < 0,25) fue significativamente más elevada que la de los pacientes que recibieron placebo + MTX/FAMES en todos los estudios. Durante el período abierto del estudio II, la mejora de la función física se ha mantenido hasta los 2 años. En el Estudio II, los cambios en PCS, MCS y FACIT-Fatiga a la semana 52 fueron 10,1, 5,4 y 8,4 respectivamente, en el grupo de 8 mg/kg de TCZ + MTX comparado con 5,6, 3,8 y 5,5, en el grupo placebo + MTX, respectivamente. En la semana 52, el cambio medio en HAQ-DI fue de -0,58 en el grupo de tocilizumab 8 mg/kg más MTX comparado con -0,39 del grupo placebo más MTX. El cambio medio en HAQ-DI se mantuvo en la semana 104 en el grupo tocilizumab 8 mg/kg más MTX (-0,61). Niveles de hemoglobina: Se comprobaron mejoras estadísticamente significativas en los niveles de hemoglobina con tocilizumab en comparación con los FAMEs (p < 0,0001) en la semana 24. Los niveles medios de hemoglobina aumentaron en la semana 2 y permanecieron dentro del intervalo normal hasta la semana 24. Un marcado descenso en los niveles promedio de los reactantes de fase aguda PCR, ERS y amiloide sérico A ocurrió rápidamente luego de la administración de tocilizumab. Junto con este efecto sobre los reactantes de fase aguda el tratamiento con tocilizumab se asoció con una reducción en el recuento de plaquetas, pero dentro del rango considerado normal. Tocilizumab versus adalimumab en monoterapia: En el ensayo VI, WA19924, doble-ciego, de 24 semanas, que comparó tocilizumab en monoterapia con adalimumab en monoterapia, se evaluó a 326 pacientes con AR que eran intolerantes a MTX o donde el tratamiento continuado con MTX se consideraba inapropiado (incluyendo respondedores inadecuados a MTX). Los pacientes en el grupo de tocilizumab recibieron una infusión intravenosa (i.v.) de tocilizumab (8 mg/kg) cada 4 semanas y una inyección subcutánea (s.c.) de placebo cada 2 semanas. A los pacientes en el grupo de adalimumab se les administró una inyección subcutánea de adalimumab (40 mg) cada 2 semanas más una infusión intravenosa de placebo cada 4 semanas. Se observó un efecto de tratamiento superior, estadísticamente significativo de tocilizumab sobre adalimumab, en el control de la actividad de la enfermedad, desde el valor basal a la semana 24, para la variable primaria cambio en DAS28 y para todas las variables secundarias (Tabla 3).
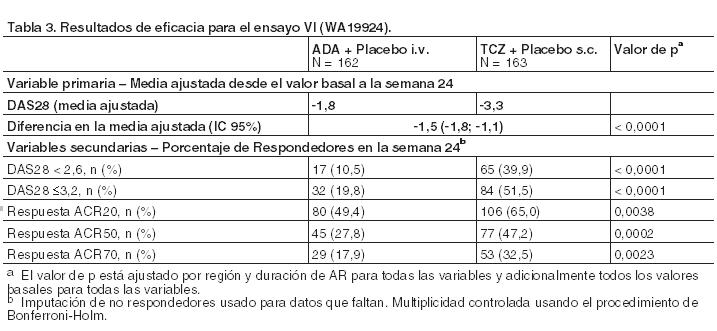
El perfil clínico global de eventos adversos fue similar entre tocilizumab y adalimumab. La proporción de pacientes con reacciones adversas graves fue equilibrada entre los grupos de tratamiento (tocilizumab 11,7% comparado con adalimumab 9,9%). Las reacciones adversas medicamentosas en el grupo de tocilizumab concordaron con el perfil de seguridad conocido de tocilizumab y la frecuencia de las reacciones adversas notificadas fue similar en comparación con la Tabla 8. Se informó en el grupo de tocilizumab una mayor incidencia de infecciones e infestaciones (48% comparado con 42%), sin diferencias en las infecciones graves (3,1%). Ambos tratamientos en estudio indujeron el mismo patrón de cambios en los parámetros de seguridad del laboratorio (disminución en neutrófilos y recuento de plaquetas, aumento en ALT, AST y lípidos); sin embargo, la magnitud de las modificaciones y la frecuencia de fuertes anomalías fueron superiores con tocilizumab en comparación con adalimumab. Cuatro pacientes (2,5%) en el grupo de tocilizumab y 2 (1,2%) en el grupo de adalimumab experimentaron una disminución en el recuento de neutrófilos de Grados 3 o 4 según los Criterios de Toxicidad Común (CTC). Once pacientes (6,8%) en el grupo de tocilizumab y 5 (3,1%) en el de adalimumab tuvieron un incremento de las ALT de Grado 2 o superior según CTC. El aumento medio de LDL desde el valor basal fue 0,64 mmol/litro (25 mg/dl) para pacientes en el grupo de tocilizumab y 0,19 mmol/litro (7 mg/dl) para los del grupo de adalimumab. La seguridad observada en el grupo de tocilizumab concordó con el perfil de seguridad conocido de tocilizumab y no se observaron reacciones adversas al medicamento nuevas o inesperadas (véase Tabla 8). Pacientes sin tratamiento previo con MTX, AR precoz: En el ensayo VII, un estudio de 2 años de duración, el análisis primario previsto en la semana 52, se evaluó a 1.162 pacientes adultos con AR temprana de moderada a grave no tratados previamente con MTX (duración media de la enfermedad ≤6 meses). Aproximadamente el 20% de los pacientes había recibido tratamiento previo con FAMEs distintos de MTX. Este estudio investigó la eficacia en la reducción de los signos y síntomas y la tasa de progresión del daño articular de tocilizumab intravenoso 4 mg/kg u 8 mg/kg en combinación con MTX cada 4 semanas, frente a tocilizumab intravenoso 8 mg/kg en monoterapia y frente a MTX en monoterapia, hasta la semana 104. La variable primaria fue la proporción de pacientes que logró la remisión DAS28 en la semana 24 (DAS28 < 2,6). La variable principal se alcanzó con una proporción significativamente mayor de pacientes en el grupo de tocilizumab 8 mg/kg más MTX y en el de tocilizumab en monoterapia comparado con el grupo de MTX en monoterapia. El grupo de pacientes tratados con tocilizumab 8 mg/kg más MTX también mostró una diferencia estadísticamente significativa en los resultados de las variables secundarias. Se observó una mayor respuesta en todas las variables secundarias para tocilizumab 8 mg/kg en monoterapia comparado con MTX en monoterapia, incluido los resultados radiográficos. En este estudio, se analizó también la remisión ACR/EULAR (Boolean e Index) en las variables exploratorias y las respuestas más altas se registraron en los grupos de tocilizumab. Los resultados del estudio VII se muestran en la Tabla 4.
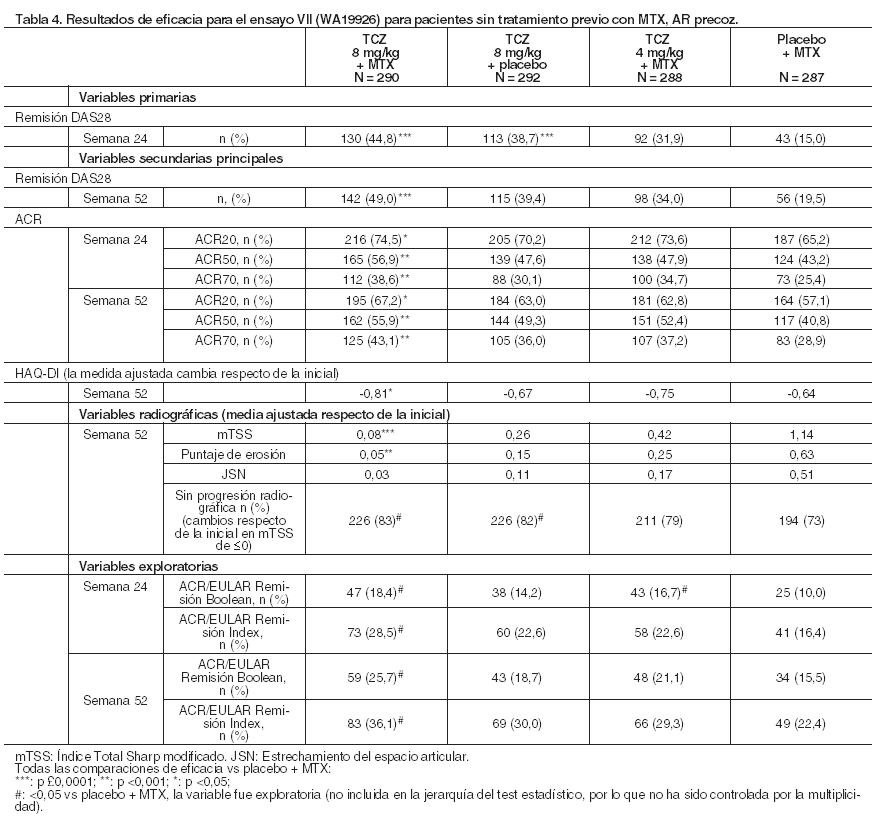
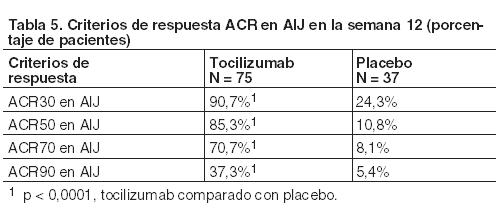
Población pediátrica: Pacientes con Artritis idiopática juvenil sistémica (AIJs): Eficacia clínica: La eficacia de tocilizumab para el tratamiento de AIJs activa fue evaluada en un ensayo de 12 semanas de duración, aleatorizado, doble-ciego, controlado con placebo, con grupos paralelos y de dos brazos. Los pacientes incluidos en el ensayo tenían una duración de la enfermedad activa de al menos 6 meses, pero sin haber experimentado un brote agudo que requiriese una dosis de corticosteroides de más de 0,5 mg/kg de prednisona o equivalente. No se ha investigado la eficacia para el tratamiento del síndrome de activación de los macrófagos. Los pacientes (tratados con o sin metotrexato) fueron aleatorizados (tocilizumab: placebo = 2:1) para recibir tocilizumab en dos dosis, a 75 pacientes se les administró infusiones de tocilizumab cada dos semanas, 8 mg/kg para pacientes ≥30 kg o 12 mg/kg para aquéllos con < 30 kg y 37 fueron asignados al tratamiento con placebo cada dos semanas. Se permitió la disminución de corticosteroides desde la semana 6 para pacientes que mejoraron su respuesta ACR70 de su AIJ. Después de 12 semanas o en el momento de abandonar el estudio, debido a un empeoramiento de la enfermedad, los pacientes fueron tratados en fase de extensión abierta con la dosificación apropiada para su peso. Respuesta clínica: El objetivo primario fue la proporción de pacientes con al menos un 30% de mejoría en el criterio de respuesta ACR en AIJ (ACR30) en la semana 12 y sin fiebre (registro de temperatura no ≥37,5°C en los últimos 7 días). El 85% de los pacientes tratados con tocilizumab (64/75) y el 24% de los que recibieron placebo alcanzaron este objetivo. Estas proporciones fueron significativamente diferentes (p < 0,0001). El porcentaje de pacientes que mejoró la respuesta ACR30, 50, 70, 90 en AIJ se detalla en la Tabla 5. Los criterios de respuesta se mantuvieron durante la fase de extensión abierta.
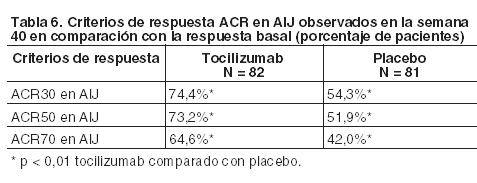
Efectos sistémicos: De los pacientes tratados con tocilizumab, el 85% que había tenido fiebre al inicio debido a su AIJs estaba sin fiebre (ningún registro de temperatura ≥37,5°C en los últimos 14 días) en la semana 12 en comparación con un 21% de los tratados con placebo (p < 0,0001); y 64% de los pacientes tratados con tocilizumab, que había tenido rash al inicio debido a su AIJs estaba sin rash en la semana 12 frente a un 11% de los que recibieron placebo (p = 0,0008). Se registró una reducción estadísticamente muy significativa del dolor para los pacientes tratados con tocilizumab en la semana 12 en comparación con los que recibieron placebo. Para aquellos a los que se administró tocilizumab, el cambio medio ajustado en la escala del dolor VAS, después de 12 semanas de tratamiento con tocilizumab, fue de 41 puntos en una escala de 0 a 100, comparado con una reducción de un 1 para pacientes tratados con placebo (p < 0,0001). Los criterios de respuesta se mantienen en la fase de extensión abierta en curso. Disminución en corticosteroides: A los pacientes que mejoraron la respuesta ACR70 en la AIJ se les permitió reducir la dosis de corticosteroides. Diecisiete pacientes tratados con tocilizumab (24%) frente a 1 paciente que recibió placebo (3%) redujeron su dosis de corticosteroides en por lo menos un 20% sin experimentar un brote (ACR30 en su AIJ) o la aparición de síntomas sistémicos hasta la semana 12 (p = 0,028). La disminución de los corticosteroides continuó, con 44 pacientes libres de corticosteroides orales en la semana 44, mientras mantenían las respuestas ACR en su AIJ. Resultados relacionados con la salud y la calidad de vida: En la semana 12, la proporción de pacientes tratados con tocilizumab que manifestó una mejora mínima clínicamente importante en el Cuestionario de Evaluación de Salud Infantil - Índice de Discapacidad (definida como una disminución del puntaje total ≥0,13) fue significativamente mayor que en los tratados con placebo, 77% comparado con 19% (p < 0,0001). Los criterios de respuesta se mantienen en la fase de extensión abierta en curso. Parámetros de laboratorio: Cincuenta de 75 pacientes (67%) tratados con tocilizumab tuvieron un valor de hemoglobina menor al límite inferior de normalidad (LIN) al inicio. Cuarenta de estos pacientes (80%) con hemoglobina reducida tuvieron un aumento de este parámetro dentro de los límites normales en la semana 12, en comparación con sólo 2 de 29 (7%) tratados con placebo, que tenían hemoglobina menor a LIN al comienzo del estudio (p < 0,0001). Cuarenta y cuatro de los pacientes tratados con tocilizumab (88%) que tenían hemoglobina reducida al inicio tuvieron un incremento en su hemoglobina de ≥ 10g/l en la semana 6 en comparación con un paciente tratado con placebo (3%) (p < 0,0001). La proporción de pacientes tratados con tocilizumab que tenía trombocitosis al inicio, con un recuento normal de plaquetas en la semana 12 fue significativamente superior que la de los que recibieron placebo, 90% frente a 4% (p < 0,0001). Una marcada disminución en los niveles medios de reactantes de fase aguda, PCR, tasa ESR, y amiloide A sérico ocurre rápidamente después de la administración de tocilizumab. Pacientes con Artritis idiopática juvenil poliarticular (AIJp): Eficacia clínica: Se ha evaluado la eficacia de tocilizumab en el ensayo WA19977 que consta de tres partes, incluyendo una extensión abierta en niños con AIJp activa. La Parte I consistió en un período de introducción de tratamiento activo con tocilizumab de 16 semanas de duración (n = 188), seguido por la Parte II, una fase de retirada de 24 semanas de duración, doble-ciego y controlado con placebo (n = 163); y una Parte III, un lapso abierto de 64 semanas. En la Parte I, los pacientes elegibles ≥30 kg recibieron 8 mg/kg de tocilizumab intravenoso cada 4 semanas, durante 4 dosis. Los que pesaban menos de 30 kg fueron aleatorizados 1:1 para recibir tocilizumab 8 mg/kg o 10 mg/kg intravenoso cada 4 semanas, durante 4 dosis. Los pacientes que completaron la Parte I del ensayo y alcanzaron por lo menos una respuesta ACR30 en AIJ en la semana 16 en comparación con la respuesta basal, fueron elegibles para adherirse en el período de retirada ciego (Parte II) del ensayo. En la Parte II, los pacientes fueron aleatorizados a tocilizumab (misma dosis recibida en la Parte I) o placebo en proporción 1:1, se estratificó por uso concurrente de metotrexato y corticosteroides. Los pacientes continuaron en la Parte II del ensayo hasta la semana 40, o hasta que la respuesta ACR30 en AIJ desmejoró (con respecto a la semana 16), y calificaron para recibir la terapia de retirada con tocilizumab (misma dosis recibida en la Parte I). Respuesta clínica: La variable primaria de eficacia fue la proporción de pacientes con respuesta ACR30 en AIJ desmejorada en la semana 40 con respecto a la semana 16. El 48% (48,1%, 39/81) de los pacientes tratados con placebo empeoró comparado con el 25,6% (21/82) de los que recibieron tocilizumab. Estos porcentajes demostraron diferencias estadísticamente significativas (p = 0,0024). Como conclusión de la Parte I, las respuestas ACR30, 50, 70 y 90 en AIJ fueron 89,4%, 83,0%, 62,2% y 26,1%, respectivamente. Durante la fase de retirada (Parte II), el porcentaje de pacientes que alcanzó las respuestas ACR30, 50 y 70 en AIJ en la semana 40 en relación con la respuesta basal, se detalla en la Tabla 6. En este análisis estadístico, los pacientes que empeoraron (y cambiaron a tocilizumab) durante la Parte II o que abandonaron, se clasificaron como no respondedores. El análisis adicional de respuestas ACR en AIJ, considerando los datos observados en la semana 40, independientemente del estado de deterioro, demostró que en la semana 40, el 95,1% de los pacientes que había recibido terapia continuada de tocilizumab, había alcanzado la respuesta ACR30 en AIJ o superior.
El número de articulaciones activas se redujo significativamente con respecto al valor basal en pacientes que recibieron tocilizumab en comparación con placebo (cambios promedios ajustados de -14,3 frente a -11,4, p = 0,0435). La evaluación realizada por el médico de la actividad global de la enfermedad, según lo medido en una escala de 0-100 mm, demostró una reducción mayor de la actividad de la enfermedad con tocilizumab en comparación con placebo (cambios promedios ajustados de -45,2 mm frente a -35,2 mm, p = 0,0031). El cambio promedio ajustado en la escala del dolor VAS, después de 40 semanas de tratamiento con tocilizumab, fue de 32,4 mm en una escala de 0-100 mm, comparado con una reducción de 22,3 mm para los pacientes tratados con placebo (estadísticamente muy significativa, p = 0,0076). Las respuestas ACR fueron numéricamente inferiores en pacientes con tratamiento biológico previo, como se detalla en la Tabla 7.
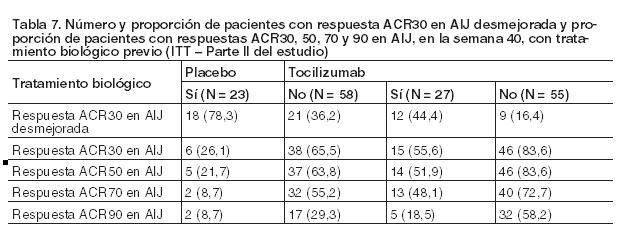
Los pacientes aleatorizados a tocilizumab tuvieron menos respuestas ACR30 en AIJ desmejoradas y un aumento general de las respuestas ACR que aquéllos que recibieron placebo, independientemente de los antecedentes de tratamiento biológico previo. La Agencia Europea de Medicamentos ha eximido al titular de la obligación de presentar los resultados de los estudios realizados con Actemra en todos los subgrupos de población pediátrica con artritis reumatoidea, y ha aplazado la obligación de presentar las conclusiones de los estudios con Actemra en todos los subgrupos de población pediátrica con artritis idiopática juvenil (véase Dosificación, para más información sobre uso pediátrico). Propiedades farmacocinéticas: Pacientes con Artritis reumatoidea (AR): Absorción: Se determinó la farmacocinética de tocilizumab usando un análisis de farmacocinética poblacional en una base de datos compuesta por 3.552 pacientes con artritis reumatoidea tratados con una infusión de una hora de 4 u 8 mg/kg de tocilizumab cada 4 semanas durante 24 semanas o con 162 mg de tocilizumab administrados por vía subcutánea una vez por semana o cada dos semanas durante 24 semanas. Los siguientes parámetros son válidos para una dosis de 8 mg/kg de tocilizumab administrados cada 4 semanas: los valores medios previstos (± DE) en equilibrio fueron de área bajo la curva (ABC) = 38.000 ± 13.000 h•mg/ml, concentración mínima (Cmín) = 15,9 ± 13,1 mg/ml y concentración máxima (Cmáx) = 182 ± 50,4 mg/ml de tocilizumab. Los cocientes de acumulación para ABC y Cmáx fueron pequeños, de 1,32 y 1,09, respectivamente. Este cociente de acumulación fue mayor para la Cmín (2,49), lo que era esperado de acuerdo con la contribución del clearance no lineal en concentraciones menores. Se alcanzó el equilibrio después de la primera administración para la Cmáx y después de 8 y 20 semanas para el ABC y la Cmín, respectivamente. El ABC, la Cmín y la Cmáx de tocilizumab aumentaron con el incremento del peso corporal. Para un peso corporal ≥100 kg, los valores medios previstos (±DE), en equilibrio de ABC, Cmin y Cmáx de tocilizumab fueron de 50.000 ± 16.800 mg•h/ml, 24,4 ± 17,5 mg/ml, y 226 ± 50,3 mg/ml, respectivamente, los cuales son mayores que los valores de exposición media de los pacientes (es decir, cualquier peso corporal) indicados anteriormente. La curva dosis-respuesta para tocilizumab se aplana a mayor exposición, resultando en una menor ganancia de eficacia por cada incremento en la concentración de tocilizumab, de manera que no se demostró mayor eficacia clínicamente significativa en pacientes tratados con > 800 mg de tocilizumab. Por lo tanto, no se recomiendan dosis de tocilizumab superiores a 800 mg en infusión en pacientes que pesen ≥ de 100 kg (véase Dosificación). Los siguientes parámetros son válidos para una dosis de 4 mg/kg de tocilizumab administrada cada 4 semanas. Los valores medios pronosticados (± DE) en estado de equilibrio de ABC (área bajo la curva), concentración mínima (Cmín) y concentración máxima (Cmáx) de tocilizumab fueron de 13.000 ± 5.800.mg.h/ml, 1,49 ± 2,13 mg/ml y 88,3 ±41,4 mg/ml, respectivamente. El cociente de acumulación fue mayor para la Cmín (1,96). Se alcanzó el equilibrio después de la primera administración para la Cmáx y para el ABC respectivamente, y después de 16 semanas para la Cmín. Distribución: En pacientes con artritis reumatoidea, el volumen central de distribución fue de 3,72 litros, el volumen periférico de distribución fue de 3,35 litros, lo que da un volumen de distribución en equilibrio de 7,07 litros. Eliminación: Después de la administración intravenosa, tocilizumab presenta una eliminación bifásica de la circulación. El clearance total de tocilizumab fue dependiente de la concentración y es la suma del clearance lineal y el no lineal. El clearance lineal se estimó como parámetro en el análisis de farmacocinética poblacional y fue de 9,5 ml/hora. El clearance no lineal dependiente de la concentración desempeña una función importante en concentraciones bajas de tocilizumab. Una vez saturada la vía de clearance no lineal, en concentraciones mayores de tocilizumab, la eliminación viene determinada fundamentalmente por el clearance lineal. La vida media (t½) de tocilizumab fue dependiente de la concentración. En equilibrio, después de una dosis de 8 mg/kg cada 4 semanas, la t1/2 eficaz se redujo con concentraciones descendentes dentro de un intervalo posológico de 18 días a 6 días. Linealidad: Los parámetros farmacocinéticos de tocilizumab no cambiaron con el tiempo. Se observó un aumento mayor que el proporcional al incremento de la dosis en el área bajo la curva (ABC) y la concentración mínima (Cmín) con las dosis de 4 y 8 mg/kg, cada 4 semanas. La concentración máxima (Cmáx) aumentó en forma proporcional a la dosis. En equilibrio, el ABC y la Cmín previstos fueron 3,2 y 30 veces mayores con 8 mg/kg que con 4 mg/kg, respectivamente. Poblaciones especiales: Insuficiencia renal: No se ha realizado ningún estudio formal del efecto de la insuficiencia renal sobre la farmacocinética de tocilizumab. La mayoría de los pacientes del análisis de farmacocinética poblacional tenía una función renal normal o insuficiencia renal leve. Esta (clearance de creatinina basado en Cockroft-Gault < 80 ml/min y ≥50 ml/min) no tuvo impacto sobre la farmacocinética de tocilizumab. No se requiere ajuste de la dosis en pacientes con insuficiencia renal leve. Insuficiencia hepática: No se ha efectuado ningún estudio formal del efecto de la insuficiencia hepática sobre la farmacocinética de tocilizumab. Edad, sexo y etnia: Los análisis de farmacocinética poblacional en pacientes con artritis reumatoidea demostraron que la edad, el sexo y la raza no afectaron la farmacocinética de tocilizumab. No se requiere ajuste de dosis para estos factores demográficos. Pacientes con Artritis idiopática juvenil sistémica (AIJs): La farmacocinética de tocilizumab se determinó mediante un análisis farmacocinético poblacional incluida en una base de datos compuesta de 75 pacientes con AIJs tratados con 8 mg/kg (con peso corporal ≥30 kg) o 12 mg/kg (con peso corporal < 30 kg), administrado cada 2 semanas. Los valores medios previstos (± DE) ABC2semanas Cmáx y Cmín de tocilizumab fueron 32.200 ± 9.960 mg•hr/ml, 245 ± 57,2 mg/ml y 57,5 ± 23,3 mg/ml, respectivamente. La proporción acumulada para la Cmín (semana 12/ semana 2) fue 3,2 ± 1,3. La Cmín de tocilizumab se estabilizó después de la semana 12. La media prevista para los valores de exposición a tocilizumab fue similar en los dos grupos de peso corporal. En pacientes con AIJs, el volumen de distribución central fue de 35 ml/kg y el de distribución periférico fue de 60 ml/kg, resultando en un volumen de distribución en equilibrio de 95 ml/kg, 2,54 litros. El clearance lineal estimado como parámetro en el análisis farmacocinético poblacional, fue de 0,142 ml/hr/kg. La vida media de tocilizumab en pacientes con AIJs es de hasta 23 días para las dos categorías de peso (8mg/kg para pesos ≥30 kg o 12 mg/kg para pesos < 30 kg) en la semana 12. Pacientes con Artritis idiopática juvenil poliarticular (AIJp): Se determinó la farmacocinética de tocilizumab usando un análisis de farmacocinética poblacional en una base de datos compuesta por 188 pacientes con AIJp. Los siguientes parámetros son válidos para una dosis de 8 mg/kg de tocilizumab (pacientes con un peso corporal ≥30 kg) administrada cada 4 semanas. Los valores medios previstos (DE) ABC4 semanas Cmáx y Cmín de tocilizumab fueron 29.500±8.660 mgh/ml, 182±37 mg/ml y 7,49±8,20 mg/ml, respectivamente. Los siguientes parámetros son válidos para una dosis de 10 mg/kg de tocilizumab (pacientes con un peso corporal < 30 kg) administrado cada 4 semanas. Los valores medios previstos (DE) ABC4 semanas Cmáx y Cmín de tocilizumab fueron 23.200±6.100 mg•h/ml, 175±32 mg/ml y 2,35±3,59 mg/ml, respectivamente. Los cocientes de acumulación fueron 1,05 y 1,16 para ABC4 semanas y 1,43 y 2,22 para Cmín para dosis de 10 mg/kg (peso corporal < 30 kg) y de 8 mg/kg (peso corporal ≥30 kg), respectivamente. No se observó acumulación para Cmáx. En pacientes con AIJp, el volumen central de distribución fue de 50 ml/kg, el volumen periférico de distribución de 53 ml/kg, resultando en un volumen de distribución en equilibrio de 103 ml/kg. El clearance lineal se estimó como parámetro en el análisis de farmacocinética poblacional y fue de 0,146 ml/h/kg. La vida media de tocilizumab en pacientes con AIJp es de hasta 16 días para las dos categorías de peso (8 mg/kg para pesos ≥30 kg o 10 mg/kg para pesos < 30 kg) durante un intervalo de dosis en estado estacionario. Datos preclínicos sobre seguridad: Los datos no clínicos no revelan un riesgo especial para los seres humanos de acuerdo con estudios convencionales sobre farmacología de seguridad, toxicidad de dosis repetidas y genotoxicidad. No se realizaron estudios de carcinogenia, dado que los anticuerpos monoclonales IgGl no se consideran potencialmente carcinogénicos. Los datos no clínicos disponibles demostraron el efecto de IL-6 a la progresión maligna y la resistencia a la apoptosis de diversos tipos de cáncer. Esta información no sugiere un riesgo relevante para la iniciación y la progresión del cáncer bajo tratamiento con tocilizumab. Además, no se observaron lesiones proliferativas en un estudio crónico, de 6 meses, de toxicidad en monos cynomolgus o en ratones con deficiencia de IL-6. Los datos no clínicos disponibles no indican un efecto sobre la fertilidad bajo el tratamiento con tocilizumab. No se observaron efectos sobre los órganos endócrinos activos y del aparato reproductor en un estudio de toxicidad crónica en monos cynomolgus y el rendimiento reproductor no se vio afectado en ratones deficitarios en IL-6. Se comprobó que tocilizumab administrado en monos cynomolgus durante la gestación precoz no tiene efecto lesivo directo o indirecto sobre el embarazo o el desarrollo embrionario-fetal. Sin embargo, se registró un leve aumento de los abortos/las muertes embrionarias-fetales con una alta exposición sistémica ( > 100 x la exposición humana) en el grupo de dosis alta de 50 mg/kg/día en comparación con placebo y otros grupos de dosis bajas. La incidencia de aborto estaba dentro de los antecedentes históricos en monos cynomolgus en cautiverio y los casos individuales de abortos/muerte embriofetal no demostraron ninguna relación constante con la dosificación de tocilizumab o con la duración de la misma. Aunque la IL-6 no parece ser una citocina crítica para el crecimiento fetal o el control inmunológico de la interfaz materno/fetal, no puede excluirse una relación de este hallazgo con tocilizumab. Se ha observado la transferencia de un análogo murino de tocilizumab en la leche de ratones lactantes. El tratamiento con un análogo murino no ha supuesto toxicidad en ratones jóvenes. En particular, no se han registrado alteraciones en el crecimiento esquelético, la función inmune y la maduración sexual.
Indicaciones.
Artritis reumatoidea (AR): Actemra está indicado, en combinación con metotrexato (MTX), para: El tratamiento de artritis reumatoidea (AR) grave, activa y progresiva en adultos no tratados previamente con MTX. El tratamiento de AR activa de moderada a grave en pacientes adultos con respuesta inadecuada o intolerancia a un tratamiento previo con uno o más fármacos antirreumáticos modificadores de la enfermedad (FAMEs) o con antagonistas del factor de necrosis tumoral (TNF). En estos pacientes Actemra puede ser administrado como monoterapia en caso de intolerancia a MTX o cuando el tratamiento continuado con MTX es inadecuado. Actemra ha demostrado reducir la tasa de progresión del daño articular medido a través de análisis radiológico y mejorar la función física, cuando se administra en combinación con metotrexato. Artritis idiopática juvenil sistémica (AIJs): Actemra está indicado para el tratamiento de artritis idiopática juvenil sistémica (AIJs) activa en pacientes desde 2 años de edad a mayores, que no han respondido adecuadamente a terapias anteriores con AINEs y corticoides sistémicos. Actemra puede ser administrado como monoterapia (en caso de intolerancia a metotrexato o cuando el tratamiento con metotrexato no es adecuado) o en combinación con metotrexato. Artritis idiopática juvenil poliarticular (AIJp): Actemra está indicado, en combinación con metotrexato (MTX), para el tratamiento de artritis idiopática
juvenil poliarticular (AIJp; factor reumatoide positivo o negativo y oligoartritis extendida) en pacientes desde 2 años de edad a mayores, que no han respondido adecuadamente al tratamiento previo con MTX. Actemra puede administrarse como monoterapia en caso de intolerancia al MTX o cuando el tratamiento continuado con MTX no sea apropiado.
Dosificación.
El reemplazo de cualquier otro agente biológico requiere el consentimiento del médico prescriptor. La terapia debe ser iniciada por profesionales sanitarios con experiencia en el diagnóstico y el tratamiento de artritis reumatoidea, de artritis idiopática juvenil sistémica (AIJs) o de artritis idiopática juvenil poliarticular (AIJp). Todos los pacientes tratados con Actemra deben recibir la Tarjeta de Alerta del Paciente de Actemra intravenoso. Pacientes con Artritis reumatoidea (AR): Posología: La posología recomendada es de 8 mg/kg de peso corporal, administrados como infusión intravenosa una vez cada cuatro semanas. Para pacientes cuyo peso corporal sea superior a 100 kg, no se recomiendan dosis que excedan de 800 mg (véase Farmacología - Propiedades farmacocinéticas). No se han evaluado dosis superiores a 1,2 g en estudios clínicos (véase Farmacología - Propiedades farmacodinámicas). Recomendaciones y ajustes de dosis si los valores de laboratorio están fuera de los parámetros normales (véase Precauciones): Enzimas hepáticas fuera de los valores normales:
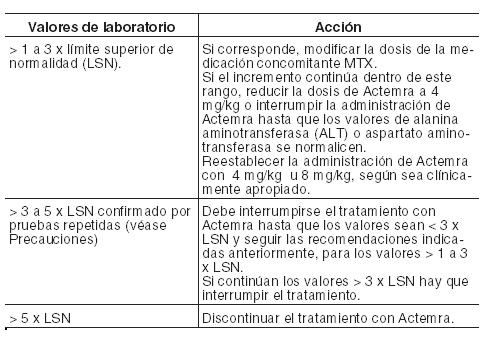
Bajo recuento absoluto de neutrófilos (RAN): No se recomienda iniciar el tratamiento, en pacientes que no han sido tratados previamente con Actemra, si el recuento absoluto de neutrófilos está por debajo de 2 x 109/l.
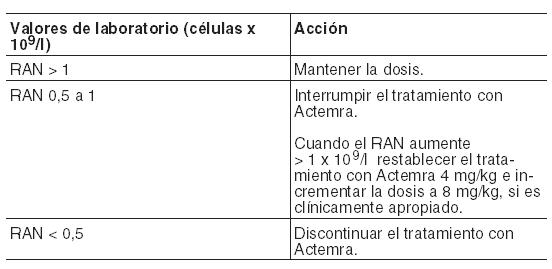
Bajo recuento de plaquetas:

Poblaciones especiales: Población pediátrica: Pacientes con Artritis idiopática juvenil sistémica (AIJs): La dosis recomendada en pacientes mayores de 2 años es de 8 mg/kg una vez cada dos semanas en pacientes con un peso mayor o igual a 30 kg o 12 mg/kg una vez cada dos semanas en aquéllos cuyo peso sea menor de 30 kg. La dosis debe ser calculada sobre la base del peso del paciente en cada administración. Un cambio en la dosis únicamente se debe justificar por una modificación sustancial en el peso del paciente. No se han establecido la seguridad y eficacia de Actemra en niños menores de 2 años, ya que no se dispone de datos. En pacientes con AIJs se recomienda interrumpir la dosis de tocilizumab si los valores de laboratorio están fuera de los parámetros normales, véase Tabla siguiente. Si corresponde, la dosis concomitante de metotrexato y/o de otra medicación puede ser modificada o suspendida, y la dosis de tocilizumab interrumpida hasta que la situación clínica haya sido evaluada. Como en los pacientes con AIJs hay diversas comorbilidades que pueden afectar a los valores de laboratorio, si éstos están fuera de los parámetros normales la decisión de suspender tocilizumab debe estar basada en la evaluación individual del médico para cada paciente. Recomendaciones y ajustes de dosis si los valores de laboratorio están fuera de los parámetros normales (véase Precauciones): Enzimas hepáticas fuera de los valores normales:
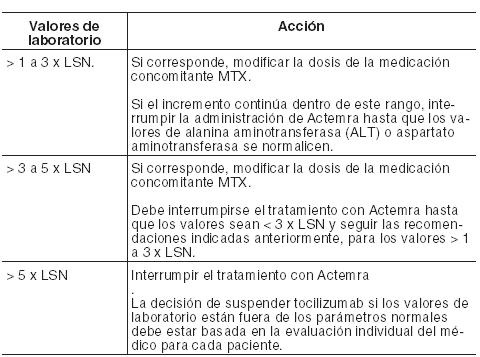
Bajo recuento absoluto de neutrófilos (RAN):
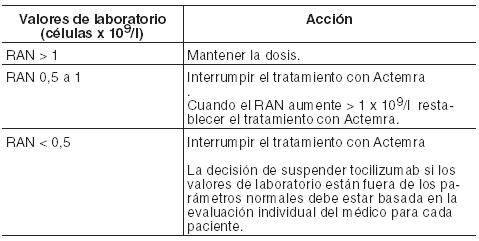
Bajo recuento de plaquetas:

En pacientes con AIJs no se ha estudiado el efecto de las reducciones de dosis de tocilizumab si los valores de laboratorio están fuera de los parámetros normales. Los datos disponibles indican que la mejoría clínica se observa a las 6 semanas de iniciar el tratamiento con Actemra. Se debe reconsiderar cuidadosamente continuar con el mismo, si el paciente no ha mostrado mejoría en este período de tiempo. Pacientes con Artritis idiopática juvenil poliarticular (AIJp): La posología recomendada en pacientes mayores de 2 años es de 8 mg/kg una vez cada 4 semanas en pacientes con un peso superior o igual a 30 kg o de 10 mg/kg una vez cada 4 semanas en aquéllos con un peso menor de 30 kg. La dosis debe ser calculada sobre la base del peso corporal del paciente en cada administración. Un cambio en la dosis únicamente se debe justificar por una modificación sustancial en el peso del paciente con el tiempo. No se ha establecido la seguridad y eficacia de Actemra en niños menores de 2 años de edad, ya que no se dispone de datos. En pacientes con AIJp se recomienda interrumpir la dosis de tocilizumab si los valores de laboratorio están fuera de los parámetros normales, véase Tabla siguiente. Si corresponde, la dosis concomitante de metotrexato y/o de otra medicación puede ser modificada o suspendida, y la dosis de tocilizumab interrumpida hasta que la situación clínica haya sido evaluada. Como en los pacientes con AIJp hay diversas comorbilidades que pueden afectar a los valores de laboratorio, si éstos están fuera de los parámetros normales la decisión de suspender tocilizumab debe estar basada en la evaluación individual del médico para cada paciente. Recomendaciones y ajustes de dosis si los valores de laboratorio están fuera de los parámetros normales (véase Precauciones): Enzimas hepáticas fuera de los valores normales:
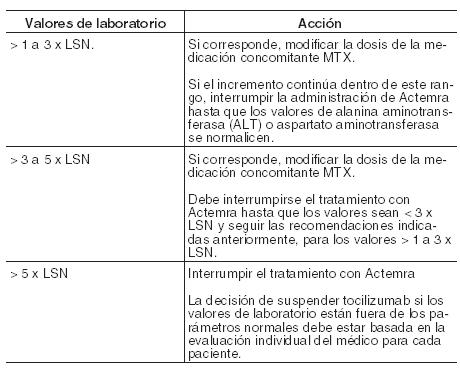
Bajo recuento absoluto de neutrófilos (RAN):
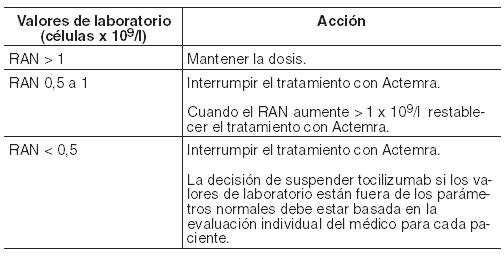
Bajo recuento de plaquetas:
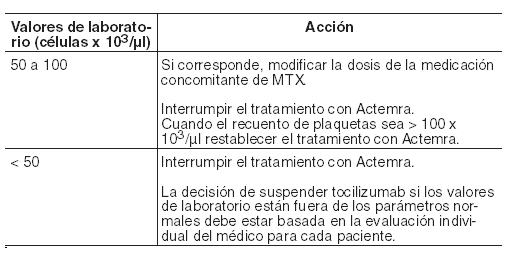
En pacientes con AIJp no se ha estudiado el efecto de las reducciones de dosis de tocilizumab si los valores de laboratorio están fuera de los parámetros normales. Los datos disponibles indican que la mejoría clínica se observa a las 12 semanas de iniciar el tratamiento con Actemra. Se debe reconsiderar cuidadosamente continuar con el mismo, si el paciente no ha mostrado mejoría en este período de tiempo. Pacientes de edad avanzada: No se requiere el ajuste de dosis en pacientes de 65 años de edad y mayores. Pacientes con insuficiencia renal: No se requiere ajuste de la dosis en pacientes con insuficiencia renal leve. Actemra no ha sido estudiado en pacientes con insuficiencia renal de moderada a grave (véase Farmacología - Propiedades farmacocinéticas). La función renal debe ser estrechamente vigilada en esta población. Pacientes con insuficiencia hepática: No se ha estudiado Actemra en pacientes con insuficiencia hepática. Por lo tanto, no pueden hacerse recomendaciones sobre la dosis. Forma de administración: Actemra debe ser administrado después de su dilución, como infusión intravenosa durante una hora, en pacientes con artritis reumatoidea (AR), con artritis idiopática juvenil sistémica (AIJs) y con artritis idiopática juvenil poliarticular (AIJp). Actemra se suministra en viales de uso único. No administrar en bolo. Instrucciones para la dilución previa a la administración: Los medicamentos de uso parenteral deben comprobarse visualmente antes de su administración para detectar la posible existencia de partículas o decoloración. Sólo deben diluirse las soluciones que sean transparentes a opalescentes, incoloras a amarillo pálido y carentes de partículas visibles. Pacientes con Artritis reumatoidea (AR): Retire de una bolsa de infusión de 100 ml un volumen de solución para inyección estéril y apirógena de cloruro sódico 9 mg/ml (0,9%) igual que el volumen de concentrado de Actemra necesario para la dosis del paciente, en condiciones asépticas. La cantidad necesaria de concentrado de Actemra (0,4 ml/kg) debe ser retirada del vial y colocada en los 100 ml de la bolsa de infusión. El volumen final debe ser de 100 ml. Para mezclar la solución, invierta suavemente la bolsa de infusión para evitar la formación de espuma. Uso en la población pediátrica: Pacientes con Artritis idiopática juvenil sistémica (AIJs) y Artritis idiopática juvenil poliarticular (AIJp) con peso ≥30 kg: Retire de una bolsa de infusión de 100 ml un volumen de solución para inyección estéril y apirógena de cloruro sódico 9 mg/ml (0,9%) igual que el volumen de concentrado de Actemra necesario para la dosis del paciente, en condiciones asépticas. La cantidad necesaria de concentrado de Actemra (0,4 ml/kg) debe ser retirada del vial y colocada en los 100 ml de la bolsa de infusión. El volumen final debe ser de 100 ml. Para mezclar la solución, invierta suavemente la bolsa de infusión para evitar la formación de espuma. Pacientes con Artritis idiopática juvenil sistémica (AIJs) con peso < 30 kg: Retire de una bolsa de infusión de 50 ml un volumen de solución para inyección estéril y apirógena de cloruro sódico 9 mg/ml (0,9%) igual que el volumen de concentrado de Actemra necesario para la dosis del paciente, en condiciones asépticas. La cantidad necesaria de concentrado de Actemra (0,6 ml/kg) debe ser retirada del vial y colocada en los 50 ml de la bolsa de infusión. El volumen final debe ser de 50 ml. Para mezclar la solución, invierta suavemente la bolsa de infusión para evitar la formación de espuma. Pacientes con Artritis idiopática juvenil poliarticular (AIJp) con peso < 30 kg: Retire de una bolsa de infusión de 50 ml un volumen de solución para inyección estéril y apirógena de cloruro sódico 9 mg/ml (0,9%) igual que el volumen de concentrado de Actemra necesario para la dosis del paciente, en condiciones asépticas. La cantidad necesaria de concentrado de Actemra (0,5 ml/kg) debe ser retirada del vial y colocada en los 50 ml de la bolsa de infusión. El volumen final debe ser de 50 ml. Para mezclar la solución, invierta suavemente la bolsa de infusión para evitar la formación de espuma.
Contraindicaciones.
Hipersensibilidad al principio activo o a cualquiera de sus excipientes. Infecciones graves y activas (véase Precauciones).
Reacciones adversas.
Pacientes con Artritis reumatoidea (AR): Resumen del perfil de seguridad: Las reacciones adversas medicamentosas notificadas con más frecuencia (que se produjeron en ≥5% de los pacientes tratados con tocilizumab en monoterapia o en combinación con FAMEs) fueron infecciones en el tracto respiratorio superior, nasofaringitis, cefalea, hipertensión y elevación de la ALT. Las reacciones adversas más graves fueron infecciones graves, complicaciones de la diverticulitis y reacciones de hipersensibilidad. Pacientes con Artritis reumatoidea (AR): La seguridad de Actemra ha sido estudiada en 4 ensayos controlados con placebo (estudios II, III, IV y V), un estudio con MTX como control (estudio I) y sus fases de extensión (véase Farmacología - Propiedades farmacodinámicas). El período controlado doble-ciego fue de 6 meses en cuatro estudios (I, III, IV y V) y de hasta 2 años en el estudio II. En los estudios controlados, doble-ciego, 774 pacientes recibieron 4 mg/kg de tocilizumab en combinación con MTX, 1.870 8 mg/kg de tocilizumab asociado con MTX/u otros FAMEs y 288 8 mg/kg de tocilizumab en monoterapia. La población expuesta a largo plazo incluye a todos los pacientes que recibieron por lo menos una dosis de tocilizumab en los estudios controlados y doble-ciego o en las fases abiertas de los estudios de extensión. De los 4.009 pacientes expuestos, 3.577 fueron tratados durante por lo menos 6 meses, 3.296 durante por lo menos 1 año, 2.806 durante por lo menos 2 años y 1.222 durante 3 años. Las reacciones adversas medicamentosas enumeradas en la Tabla 8 se presentan según la clasificación por órganos y sistemas y frecuencias. Las frecuencias se definen de la siguiente manera: muy frecuentes (≥1/10); frecuentes (≥1/100 a < 1/10), poco frecuentes (≥1/1000 a < 1/100), raras ( > 1/10.000 a < 1/1.000) o muy raras ( < 1/10.000). Las reacciones adversas se enumeran en orden decreciente de gravedad dentro de cada intervalo de frecuencia.
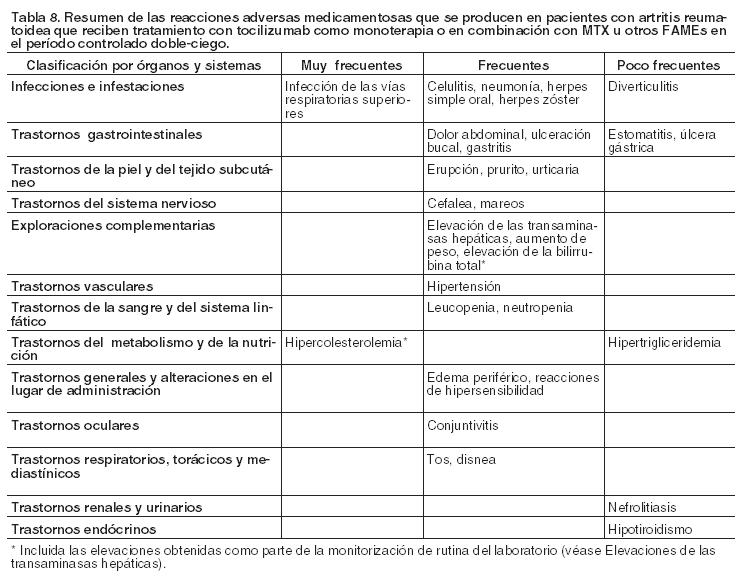
Infecciones: En los estudios controlados de 6 meses, la tasa de todas las infecciones notificadas con el tratamiento de tocilizumab 8 mg/kg más FAMEs fue de 127 eventos por 100 pacientes-años comparada con 112 eventos por 100 pacientes-años en el grupo de placebo más FAMEs. En la población expuesta a largo plazo, la tasa global de infecciones con Actemra fue de 108 eventos por 100 pacientes-años de exposición. En los ensayos clínicos controlados de 6 meses, la tasa de todas las infecciones graves comunicadas con tocilizumab 8 mg/kg más FAMEs fue de 5,3 eventos por 100 pacientes-años de exposición comparada con 3,9 eventos por 100 pacientes-años de exposición en el grupo de placebo más FAMEs. En el estudio de monoterapia, la tasa de infecciones graves fue de 3,6 eventos por 100 pacientes-años de exposición en el grupo de tocilizumab y de 1,5 eventos por 100 pacientes-años de exposición en el grupo de MTX. En la población expuesta a largo plazo, la tasa global de infecciones (bacterianas, víricas y fúngicas) fue de 4,7 eventos por 100 pacientes-años de exposición. Entre las infecciones graves notificadas, algunas mortales, se incluyeron tuberculosis activa, que se puede presentar con enfermedad intrapulmonar o extrapulmonar, infecciones pulmonares invasivas, incluidas candidiasis, aspergilosis, coccidioidomicosis y neumocistis jirovecii, neumonía, celulitis, herpes zóster, gastroenteritis, diverticulitis, sepsis y artritis bacteriana. También se han informado casos de infecciones oportunistas. Enfermedad pulmonar intersticial: El deterioro de la función pulmonar puede aumentar el riesgo de desarrollo de infecciones. Durante la comercialización se han comunicado casos de enfermedad pulmonar intersticial (incluyendo neumonía y fibrosis pulmonar), alguno de los cuales fue mortal. Perforación gastrointestinal: Durante 6 meses de ensayos clínicos controlados, la tasa global de perforaciones gastrointestinales fue de 0,26 eventos por 100 pacientes-año en tratamiento con tocilizumab. En la población expuesta a largo plazo la tasa global de perforaciones gastrointestinales fue de 0,28 eventos por 100 pacientes-años. Los informes de perforación gastrointestinal con tocilizumab fueron comunicados inicialmente como complicaciones de diverticulitis, tales como, peritonitis purulenta generalizada, perforación gastrointestinal inferior, fístulas y abscesos. Reacciones a la infusión: En los estudios controlados de 6 meses se registraron eventos adversos asociados con la infusión (reacciones seleccionadas que se producen durante o dentro de las 24 horas después de la infusión) en el 6,9% de los pacientes en el grupo de tocilizumab 8 mg/kg más FAMEs y en 5,1% de los del grupo placebo más FAMEs. Los eventos notificados durante la infusión fueron fundamentalmente episodios de hipertensión; los acontecimientos informados en el plazo de 24 horas desde la terminación de una infusión fueron cefalea y reacciones cutáneas (erupción, urticaria). Estos eventos no fueron limitantes para el tratamiento. La tasa de reacciones anafilácticas (que se produjeron en un total de 8/4.009 pacientes, 0,2%) fue varias veces más elevada con la dosis de 4 mg/kg que con la de 8 mg/kg. Se notificaron reacciones de hipersensibilidad clínicamente significativas asociadas con tocilizumab y que precisaron suspensión del tratamiento en un total de 56 de 4.009 pacientes (1,4%) tratados con tocilizumab durante los estudios clínicos controlados y abiertos. Estas reacciones se observaron generalmente de la segunda a la quinta infusión de tocilizumab (véase Precauciones). Se ha comunicado una reacción anafiláctica mortal durante el tratamiento con tocilizumab en la etapa poscomercialización (véase Precauciones). Inmunogenicidad: En ensayos clínicos controlados de 6 meses se ha estudiado un total de 2.876 pacientes en cuanto a anticuerpos anti-tocilizumab. Cuarenta y seis pacientes (1,6%) desarrollaron anticuerpos anti-tocilizumab, de los cuales 6 tuvieron una reacción de hipersensibilidad asociada y médicamente significativa, que en cinco de los casos condujo a la retirada. Treinta pacientes (1,1%) desarrollaron anticuerpos neutralizadores. Anomalías hematológicas: Neutrófilos: En los ensayos clínicos controlados de 6 meses se produjeron descensos de los recuentos de neutrófilos por debajo de 1 x 109/l en el 3,4% de los pacientes tratados con tocilizumab 8 mg/kg más FAMEs en comparación con < 0,1% de aquellos a los que se administró placebo más FAMEs. Aproximadamente la mitad de los pacientes que desarrollaron RAN < 1 x 109/l lo hicieron en el plazo de 8 semanas después de comenzar el tratamiento. Se notificaron descensos por debajo de 0,5 x 109 /l en el 0,3% de los pacientes que recibieron tocilizumab 8 mg/kg más FAMEs. Se han informado casos de infecciones con neutropenia. Durante el período controlado doble-ciego y en el lapso de exposición a largo plazo, el patrón y la incidencia de descensos en los recuentos de neutrófilos coincidieron con lo observado en los 6 meses de ensayos clínicos controlados. Plaquetas: En los ensayos clínicos controlados de 6 meses se produjeron disminuciones de los recuentos de plaquetas por debajo de 100 x 103/ml en el 1,7% de los pacientes tratados con tocilizumab 8 mg/kg más FAMEs en comparación con < 1% de aquellos que recibieron placebo más FAMEs. Estos descensos se produjeron sin episodios hemorrágicos asociados. Durante el período controlado doble-ciego y en el lapso de exposición a largo plazo, el patrón y la incidencia de descensos en los recuentos de plaquetas coincidieron con lo observado en los 6 meses de ensayos clínicos controlados. Se han comunicado casos muy poco frecuentes de pancitopenia durante la etapa poscomercialización. Elevaciones de las transaminasas hepáticas: Durante los ensayos clínicos controlados de 6 meses se observaron elevaciones transitorias de ALT/AST > 3 x LSN en el 2,1% de los pacientes con tocilizumab 8 mg/kg en comparación con el 4,9% de aquellos tratados con MTX y en el 6,5% de los que recibieron 8 mg/kg de tocilizumab más FAMEs en comparación con el 1,5% de los tratados con placebo más FAMEs. La adición de fármacos potencialmente hepatotóxicos (por ejemplo, MTX) a la monoterapia con tocilizumab ocasionó un aumento de la frecuencia de estas elevaciones. Se observaron incrementos de ALT/AST > 5 x LSN en el 0,7% de los pacientes en monoterapia con tocilizumab y en el 1,4% de los tratados con tocilizumab más FAMEs, la mayoría de los cuales abandonaron en forma permanente el tratamiento con tocilizumab. Estas elevaciones no se asociaron con un ascenso clínicamente relevante de la bilirrubina directa, ni con pruebas clínicas de hepatitis o insuficiencia hepática. Durante un período controlado doble-ciego la incidencia de niveles de bilirrubina indirecta por encima del límite superior normal, obtenidos como un parámetro de rutina de laboratorio, es de 6,2% en pacientes tratados con 8 mg/kg de tocilizumab + FAMEs. Un total de 5,8% de pacientes experimentó un incremento de los niveles de bilirrubina indirecta de > 1 a 2 x LSN y 0,4% una elevación de > 2 x LSN. Durante el período controlado doble-ciego y en el lapso de exposición a largo plazo, el patrón y la incidencia de aumento en ALT/AST coincidieron con lo observado en los 6 meses de ensayos clínicos controlados. Parámetros lipídicos: Durante seis meses de ensayos clínicos controlados se han notificado en forma frecuente incrementos en los parámetros lipídicos, tales como: colesterol total, triglicéridos, colesterol LDL, y/o colesterol HDL. Se observó, con monitorización de rutina, en el laboratorio, que aproximadamente el 24% de los pacientes que recibieron tocilizumab en los ensayos clínicos experimentó una elevación sostenida del colesterol total ≥6,2 mmol/l y un 15% un aumento sostenido de los valores de LDL ≥4,1 mmol/l. Las elevaciones en los parámetros lipídicos respondieron al tratamiento con agentes hipolipidemiantes. Durante el período controlado doble-ciego y en el lapso de exposición a largo plazo, el patrón y la incidencia de aumento en los parámetros lipídicos coincidieron con lo observado en los 6 meses de ensayos clínicos controlados. Neoplasias malignas: Los datos clínicos son insuficientes para evaluar la posible incidencia de tumores malignos después de la exposición a tocilizumab. Se encuentran en proceso evaluaciones de seguridad a largo plazo. Reacciones cutáneas: Se han notificado muy raramente casos de Síndrome de Stevens-Johnson ocurridos durante la etapa de poscomercialización. Pacientes sin tratamiento previo con MTX, AR precoz: Resumen del perfil de seguridad: En el estudio VII (WA19926) se evaluaron 1.162 pacientes sin tratamiento previo con MTX y un agente biológico con AR precoz, moderada o grave. El perfil general de seguridad observado en los grupos de tratamiento con tocilizumab fue compatible con el perfil de seguridad conocido de tocilizumab (Tabla 8) (véase Farmacología; Propiedades farmacodinámicas). Anomalías hematológicas: Elevaciones de las transaminasas hepáticas: En el estudio VII los pacientes adultos con AR precoz, activa, moderada a grave sin tratamiento previo con MTX (duración media de la enfermedad ≤ 6 meses) experimentaron más elevaciones transitorias de ALT > 3 x LSN en comparación con toda la población de control. Esto fue observado en pacientes tratados con tocilizumab y en aquéllos que recibieron MTX en monoterapia. Población pediátrica: En la Tabla 9 se indica la seguridad de tocilizumab en la población pediátrica con artritis idiopática juvenil sistémica y artritis idiopática juvenil poliarticular. En general, en los pacientes con artritis idiopática juvenil sistémica y artritis idiopática juvenil poliarticular, las reacciones adversas medicamentosas fueron de una clase similar a las observadas en los que padecían artritis reumatoidea (véase Reacciones adversas). Las reacciones adversas medicamentosas en pacientes con artritis idiopática juvenil sistémica y artritis idiopática juvenil poliarticular tratados con tocilizumab se enumeran a continuación en la Tabla 9; las mismas se presentan según la clasificación por órganos y sistemas, y frecuencias. Las frecuencias se definen de la siguiente manera: muy frecuentes (≥ 1/10); frecuentes (≥ 1/100 a < 1/10) o poco frecuentes (≥ 1/1.000 a < 1/100).
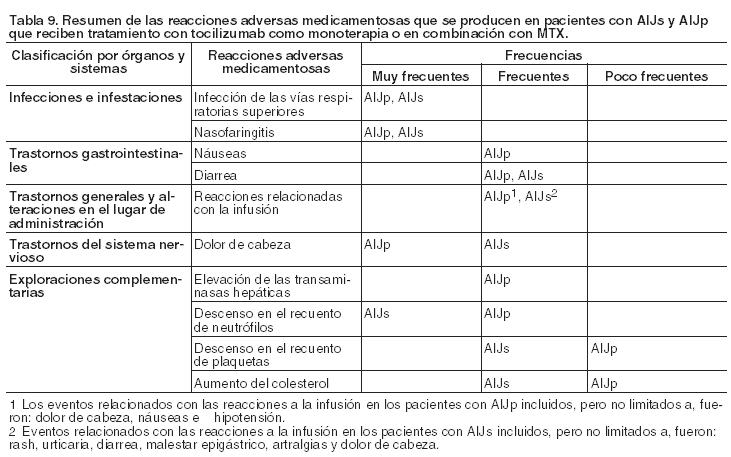
Pacientes con Artritis idiopática juvenil poliarticular (AIJp): La seguridad de tocilizumab en AIJp se ha estudiado en 188 pacientes de 2 a 17 años de edad. El total que recibió tocilizumab fue de 184,4 pacientes-año. La frecuencia de reacciones adversas medicamentosas en aquéllos con artritis idiopática juvenil poliarticular puede verse en la Tabla 9. Los tipos de reacciones adversas medicamentosas en pacientes con artritis idiopática juvenil poliarticular fueron similares a los observados en los que padecían artritis reumatoidea y artritis idiopática juvenil sistémica, véase Reacciones adversas. Comparado con la población adulta con artritis reumatoidea, se informaron con más frecuencia en artritis idiopática juvenil poliarticular, los eventos de nasofaringitis, dolor de cabeza, náuseas y disminución en el recuento de neutrófilos. Sin embargo, manifestaciones como aumento del colesterol, fueron notificados menos frecuentemente en la población con artritis idiopática juvenil poliarticular que en los adultos con artritis reumatoidea. Infecciones: La tasa de infecciones en la población total expuesta a tocilizumab fue de 163,7 por 100 pacientes-años. Los acontecimientos más comunes observados fueron nasofaringitis e infecciones del tracto respiratorio superior. La tasa de infecciones graves fue numéricamente más alta en pacientes con peso < 30 kg, tratados con 10 mg/kg de tocilizumab (12,2 por 100 pacientes-años) comparada con aquéllos con peso ≥30 kg, tratados con 8 mg/kg de tocilizumab (4,0 por 100 pacientes-años). La incidencia de infecciones que conducen a interrupciones de la dosis fue también numéricamente superior en pacientes con peso < 30 kg, tratados con 10 mg/kg de tocilizumab (21,4%) comparado con aquéllos con peso ≥30 kg, que recibieron 8 mg/kg de tocilizumab (7,6%). Reacciones a la infusión: En pacientes con artritis idiopática juvenil poliarticular, las reacciones relacionadas con la infusión se definen como todos los eventos ocurridos durante o en las 24 horas siguientes a la infusión. En la población total expuesta a tocilizumab, 11 pacientes (5,9%) experimentaron reacciones a la infusión durante la administración y 38 (20,2%) sufrieron un evento dentro de las 24 horas siguientes a la infusión. Los efectos más comunes ocurridos durante la administración fueron dolor de cabeza, náuseas e hipotensión y dentro de las 24 horas siguientes a la misma mareos e hipotensión. En general, las reacciones adversas al medicamento observadas durante o en las 24 horas siguientes a la infusión fueron similares en naturaleza a aquellas observadas en pacientes con artritis reumatoidea y con artritis idiopática juvenil sistémica (véase Reacciones adversas). No se han notificado reacciones de hipersensibilidad clínicamente significativas asociadas con tocilizumab que requiriesen interrupción del tratamiento. Inmunogenicidad: Un paciente del grupo de peso < 30 kg y 10 mg/kg desarrolló anticuerpos anti-tocilizumab positivos sin presentar reacción de hipersensibilidad y por esta causa posteriormente fue retirado del ensayo. Anomalías hematológicas: Neutrófilos: Durante la monitorización rutinaria en los valores de laboratorio en toda la población expuesta a tocilizumab, se observó una disminución en el recuento de neutrófilos por debajo de 1 x 109/litro en el 3,7% de los pacientes. Plaquetas: Durante la monitorización rutinaria de los valores de laboratorio en toda la población expuesta a tocilizumab, el 1% de los pacientes tuvo una disminución en el recuento de plaquetas a ≤ 50 x 103/ml, sin episodios de sangrado asociados. Elevación en las transaminasas hepáticas: Durante la monitorización rutinaria en los valores de laboratorio en toda la población expuesta a tocilizumab una elevación en ALT o AST ≥3 x LSN ocurrió en el 3,7% y en menos del 1% de los pacientes, respectivamente. Parámetros lipídicos: Durante la monitorización rutinaria en los valores de laboratorio en toda la población expuesta a tocilizumab, el incremento de colesterol total > 1,5 x LSN hasta 2 x LSN se observó en un paciente (0,5%) y también en otro (0,5%) el aumento en LDL > 1,5 x LSN hasta 2 x LSN. Pacientes con Artritis idiopática juvenil sistémica (AIJs): La seguridad de tocilizumab en artritis idiopática juvenil sistémica se ha estudiado en 112 pacientes de 2 a 17 años. En las 12 semanas de la fase controlada, doble-ciego, 75 pacientes recibieron tocilizumab (8mg/kg o 12 mg/kg en función de su peso corporal). Después de 12 semanas o en el momento de cambiar a tocilizumab, debido al empeoramiento de la enfermedad, los pacientes fueron tratados en la fase de extensión abierta en marcha. En general, las reacciones adversas en pacientes con artritis idiopática juvenil sistémica fueron de una clase similar a las observadas en aquéllos con artritis reumatoidea (véase Reacciones adversas). La frecuencia de reacciones adversas en pacientes con artritis idiopática juvenil sistémica está incluida en la Tabla 9. Comparado con la población adulta con artritis reumatoidea, se notificaron con más frecuencia en pacientes con artritis idiopática juvenil sistémica: nasofaringitis, disminución en el recuento de neutrófilos, aumento de las transaminasas hepáticas y diarrea. Sin embargo, eventos como incremento del colesterol, fueron informados con menor frecuencia en la población con artritis idiopática juvenil sistémica que en los adultos con artritis reumatoidea. Infecciones: En las 12 semanas de la fase controlada, la tasa de todas las infecciones del grupo tocilizumab fue 344,7 por 100 pacientes años y 287,0 por 100 pacientes años en el de placebo. En la fase abierta de extensión en marcha (parte II), la tasa global de infecciones continúa siendo similar (306,6 por 100 pacientes años). En las 12 semanas de la fase controlada, la tasa de infecciones graves en el grupo de tocilizumab fue de 11,5 por 100 pacientes años. En un año de la fase abierta de extensión en marcha la tasa global de infecciones graves continúa estable (11,3 por 100 pacientes años). Las infecciones graves fueron similares a las observadas en pacientes con artritis reumatoidea, incluyendo varicela y otitis media. Reacciones a la infusión: Las reacciones relacionadas con la infusión están definidas como los eventos ocurridos durante o en las 24 horas siguientes a la misma. En las 12 semanas de la fase controlada el 4% de los pacientes tratados con tocilizumab tuvo eventos durante la infusión. A un paciente se le interrumpió el tratamiento en el ensayo por presentar angioedema, considerado grave y amenazante para la vida. En las 12 semanas de la fase controlada del estudio, el 16% de los pacientes del grupo de tocilizumab y el 5,4% de aquéllos del grupo placebo experimentaron eventos en las 24 horas siguientes a la infusión. En el grupo de tocilizumab se manifestaron, pero no se limitaron a, los siguientes eventos: rash, urticaria, diarrea, malestar epigástrico, artralgia, y dolor de cabeza. La urticaria fue considerada una reacción grave. Se notificaron reacciones de hipersensibilidad clínicamente significativas asociadas con tocilizumab y que requirieron interrupción del tratamiento en 1 de cada 112 pacientes ( < 1%) tratados con tocilizumab durante la fase controlada y hasta la inclusión en la fase abierta del ensayo clínico. Inmunogenicidad: En todos los 112 pacientes se analizaron los anticuerpos anti-tocilizumab al inicio. Dos pacientes desarrollaron anticuerpos anti-tocilizumab positivos, uno de ellos tuvo una reacción de hipersensibilidad que obligó a retirarlo del ensayo. La incidencia de formación de anticuerpos anti-tocilizumab podría ser subestimada debido a interferencia de tocilizumab con el método analítico y a las altas concentraciones de producto observadas en niños en comparación con adultos. Anomalías hematológicas: Neutrófilos: Durante la monitorización en los valores de laboratorio en las 12 semanas de la fase controlada, descendió el recuento de neutrófilos por debajo del 1 x 109/l en un 7% de los pacientes del grupo de tocilizumab y no disminuyó en el grupo placebo. En la fase abierta de extensión en marcha, se redujo el recuento de neutrófilos por debajo de 1 x 109/l en un 15% de los pacientes del grupo de tocilizumab. Plaquetas: Durante la monitorización en los valores de laboratorio en las 12 semanas de la fase controlada, el 3% de los pacientes del grupo de placebo y el 1% del grupo de tocilizumab tuvieron un descenso del recuento de plaquetas hasta ≤100 x 103/ml. En la fase abierta de extensión en marcha, el descenso del recuento de plaquetas por debajo de 100 x 103/ml, se produjo en el 3% de los pacientes en el grupo de tocilizumab, sin episodios de sangrado asociados. Elevación en las transaminasas hepáticas: Durante la monitorización en los valores de laboratorio en las 12 semanas de la fase controlada, el aumento en ALT o AST ≥3 x LSN fue de un 5% y un 3%, respectivamente, en el grupo de tocilizumab y un 0% en el de placebo. En la fase abierta de extensión en marcha, el aumento de ALT o AST ≥3 x LSN fue en un 12% y un 4%, respectivamente, en el grupo de tocilizumab. Inmunoglobulina G: Los niveles de inmunoglobulina G disminuyen durante la terapia. Un descenso a límites inferiores a la normalidad se manifestó en 15 pacientes en algún momento del ensayo. Parámetros lipídicos: Durante la monitorización en los valores de laboratorio en las 12 semanas de la fase controlada, el aumento de colesterol total > 1,5 x LSN hasta 2 x LSN se produjo en el 1,5% del grupo de tocilizumab y el 0% en el de placebo. El incremento en LDL > 1,5 x LSN hasta 2 x LSN se registró en un 1,9% de los pacientes del grupo de tocilizumab y en el 0% en el de placebo. En la fase abierta de extensión en marcha, el patrón y la incidencia en la elevación en los parámetros lipídicos permanecen constantes, con datos similares a los obtenidos en la fase de las 12 semanas. Comunicación de reportes de reacciones adversas: Es importante comunicar las presuntas reacciones adversas después de la autorización del medicamento. Esto permite la monitorización continua de la relación riesgo/beneficio. Se solicita a los profesionales de la salud informar de cualquier sospecha de eventos adversos asociados con el uso de Actemra® al Área de Farmacovigilancia de Roche al siguiente teléfono 0800-77-ROCHE (76243). En forma alternativa, esta información puede ser reportada ante ANMAT. Ante cualquier inconveniente con el producto, el paciente puede llenar la ficha que está en la Página Web de la ANMAT: http://www.anmat.gov.ar/farmacovigilancia/Notificar.asp o llamar a ANMAT responde al 0800-333-1234.
Precauciones.
Trazabilidad: A fin de mejorar la trazabilidad de los medicamentos biológicos, el nombre comercial del producto administrado debe estar claramente registrado (o mencionado) en la historia clínica del paciente. Infecciones: Se han notificado infecciones graves y en algunos casos mortales en pacientes que reciben agentes inmunosupresores, incluido Actemra (véase Reacciones adversas). No debe iniciarse el tratamiento con Actemra en pacientes con infecciones activas (véase Contraindicaciones). Se debe interrumpir la administración de Actemra si un paciente desarrolla una infección grave, hasta que la misma esté controlada (véase Reacciones adversas). Los profesionales sanitarios deben tener precaución cuando consideren su empleo en pacientes con antecedentes de infecciones recurrentes o crónicas o con procesos subyacentes (por ejemplo, diverticulitis, diabetes y enfermedad pulmonar intersticial) que puedan predisponerlos a infecciones. Se recomienda vigilar la detección oportuna de infecciones graves en pacientes que reciben tratamientos biológicos para la artritis reumatoidea de moderada a grave, artritis idiopática juvenil sistémica o artritis idiopática juvenil poliarticular, ya que los signos y síntomas de la inflamación aguda pueden reducirse, debido a la supresión de la reacción de fase aguda. Los efectos de tocilizumab sobre la proteína C reactiva (PCR), neutrófilos y los signos y síntomas de la infección deben ser considerados al evaluar a un paciente con una infección potencial. Se deben dar instrucciones precisas a los pacientes (incluyendo a los niños pequeños con artritis idiopática juvenil sistémica o artritis idiopática juvenil poliarticular que pueden ser menos capaces de comunicar sus síntomas) y a los padres o cuidadores de los pacientes con artritis idiopática juvenil sistémica o artritis idiopática juvenil poliarticular, para que se contacten inmediatamente con su profesional sanitario cuando aparezca cualquier síntoma que sugiera infección y asegurar, de esa manera, una evaluación rápida y un tratamiento adecuado de la misma. Tuberculosis: Tal como se recomienda en pacientes con artritis reumatoidea, artritis idiopática juvenil sistémica y artritis idiopática juvenil poliarticular, que reciben otros tratamientos biológicos, se sugiere a los pacientes a ser tratados con Actemra realizar pruebas para la detección de infección por tuberculosis latente antes de la administración de Actemra. Los pacientes con tuberculosis latente deben recibir tratamiento estándar con antimicobacteriano antes de comenzar con Actemra. Los profesionales sanitarios deben recordar el riesgo que existe de falsos negativos al realizar la prueba cutánea de la tuberculina y la detección del gamma interferón, especialmente en pacientes que están gravemente enfermos o inmunosuprimidos. Se debe dar instrucciones a los pacientes para que acudan al médico si se presentan signos y síntomas (por ejemplo, tos persistente, debilidad/pérdida de peso, fiebre baja) que puedan sugerir una infección por tuberculosis, ya sea que se produzcan durante o después del tratamiento con Actemra. Reactivación viral: Se ha notificado reactivación viral (por ejemplo, virus de la hepatitis B) en pacientes con artritis reumatoidea que estaban en tratamiento con terapias biológicas. En los ensayos clínicos con tocilizumab, se excluyeron los pacientes con pruebas positivas para hepatitis. Complicaciones de la diverticulitis: Se han informado casos poco frecuentes de perforaciones diverticulares como complicaciones de una diverticulitis. En pacientes con artritis reumatoidea Actemra debe utilizarse con precaución en aquellos con antecedentes de ulceración intestinal o diverticulitis (véase Reacciones adversas). Los que presenten síntomas potencialmente indicativos de diverticulitis complicada, como dolor abdominal, hemorragia y/o cambio inexplicado en los hábitos intestinales con fiebre, deben ser evaluados rápidamente para la identificación precoz de diverticulitis, que puede asociarse con perforación gastrointestinal. Reacciones de hipersensibilidad: Se han comunicado reacciones de hipersensibilidad graves asociadas con la infusión de Actemra (véase Reacciones adversas). Estas reacciones pueden ser más graves y potencialmente mortales en pacientes que ya las hayan experimentado durante infusiones previas, incluso si han recibido premedicación con esteroides y antihistamínicos. Debe estar disponible un tratamiento adecuado para su uso inmediato en el caso de que se produjera una reacción anafiláctica durante el tratamiento de Actemra. Si se manifiesta una reacción anafiláctica u otra hipersensibilidad grave/reacción grave relacionada con la infusión, el tratamiento de Actemra debe interrumpirse inmediatamente y ser suspendido en forma definitiva. Enfermedad hepática activa e insuficiencia hepática: El tratamiento con Actemra, especialmente cuando se administra simultáneamente con MTX, puede estar asociado con elevaciones de las transaminasas hepáticas. Por lo tanto, debe tenerse precaución al considerar esta alternativa terapéutica en pacientes con enfermedad hepática activa o insuficiencia hepática (véanse Dosificación y Reacciones adversas). Elevaciones de las transaminasas hepáticas: En ensayos clínicos, se han comunicado frecuentemente elevaciones leves y moderadas transitorias o intermitentes de las transaminasas hepáticas con el tratamiento con Actemra, sin progresión a lesión hepática (véase Reacciones adversas). Se observó un aumento de la frecuencia de estas elevaciones cuando se usaron fármacos potencialmente hepatotóxicos (por ejemplo, metotrexato) en combinación con Actemra. Se debe considerar realizar otras pruebas hepáticas, incluida bilirrubina, cuando esté clínicamente indicado. Debe tenerse precaución al considerar el inicio de Actemra en pacientes con elevación de las transaminasas (ALT) o (AST) > 1,5 x LSN. No se recomienda el tratamiento en aquéllos con ALT o AST > 5 x LSN al comienzo. En pacientes con artritis reumatoidea se deben vigilar los valores de ALT y AST entre 4 y 8 semanas los 6 primeros meses de tratamiento y a partir de entonces cada 12 semanas. Para las modificaciones de las dosis basadas en las tr
ansaminasas, véase Dosificación. En elevaciones de ALT o AST > 3-5 LSN, confirmadas por pruebas repetidas, debe interrumpirse el tratamiento con Actemra. En pacientes con artritis idiopática juvenil sistémica y artritis idiopática juvenil poliarticular se deben vigilar los niveles de ALT y AST en el momento de la segunda infusión y posteriormente de acuerdo con las buenas prácticas clínicas (véase Dosificación). Efectos hematológicos: Se han producido descensos de los recuentos de neutrófilos y plaquetas después del tratamiento con tocilizumab 8 mg/kg en combinación con metotrexato (véase Reacciones adversas). El riesgo de neutropenia puede aumentar en pacientes que han sido previamente tratados con antagonistas del TNF. No se recomienda comenzar el tratamiento, en pacientes que no han sido tratados previamente con Actemra, si el recuento absoluto de neutrófilos está por debajo de 2 x 109/l. Debe tenerse precaución al considerar el inicio de Actemra en pacientes con un recuento bajo de plaquetas (es decir, por debajo de 100 x 103/ml). No se recomienda continuar el tratamiento en pacientes que desarrollen un recuento absoluto de neutrófilos < 0,5 x 109/l o un recuento de plaquetas < 50 x 103/ml. La neutropenia grave se puede asociar con un aumento del riesgo de infecciones graves, aunque no se ha observado una clara asociación entre el descenso de neutrófilos y la aparición de infecciones graves en los ensayos clínicos realizados con Actemra hasta la fecha. En pacientes con artritis reumatoidea el recuento de neutrófilos y plaquetas debe vigilarse de 4 a 8 semanas después del comienzo del tratamiento y posteriormente, siguiendo las recomendaciones de la práctica clínica habitual. Para las modificaciones de la dosis basadas en RAN y recuento de plaquetas, véase Dosificación. En pacientes con artritis idiopática juvenil sistémica y artritis idiopática juvenil poliarticular el recuento de neutrófilos y plaquetas debe ser vigilado en el momento de la segunda infusión y posteriormente siguiendo las recomendaciones de las buenas prácticas clínicas (véase Dosificación). Parámetros lipídicos: En los pacientes tratados con tocilizumab se han comprobado aumentos de parámetros lipídicos incluido colesterol total, lipoproteínas de baja densidad (LDL), lipoproteínas de alta densidad (HDL), y triglicéridos (véase Reacciones adversas). En la mayoría de los pacientes no se registró elevación del índice aterogénico, y el incremento del colesterol total respondió al tratamiento con agentes hipolipemiantes. En pacientes con artritis idiopática juvenil sistémica, artritis idiopática juvenil poliarticular y artritis reumatoidea de 4 a 8 semanas después del inicio del tratamiento con Actemra, debe realizarse una evaluación de los parámetros lipídicos. Los pacientes deben tratarse de acuerdo con las directivas clínicas locales para el manejo de la hiperlipidemia. Trastornos neurológicos: Los médicos deben estar atentos a síntomas potencialmente indicativos de trastornos desmielinizantes centrales de nueva aparición. Actualmente, se desconocen las posibilidades de que se produzca una desmielinización central con tocilizumab. Neoplasias malignas: El riesgo de neoplasias malignas se incrementa en pacientes con artritis reumatoidea. Los fármacos inmunomoduladores pueden aumentar el riesgo de tumores malignos. Inmunizaciones: No deben administrarse vacunas vivas o vivas atenuadas simultáneamente con Actemra, porque no se ha establecido la seguridad clínica. En un estudio abierto, aleatorizado, pacientes adultos con AR tratados con Actemra y metotrexato lograron una respuesta eficaz a la vacuna neumocócica polisacárida 23 valente y a la vacuna de toxoide tetánico, que fue comparable a la respuesta observada en pacientes tratados con metotrexato solo. Se recomienda que todos los pacientes, especialmente los de artritis idiopática juvenil sistémica y artritis idiopática juvenil poliarticular, estén al día con su vacunación de acuerdo con los actuales calendarios de vacunación antes de comenzar el tratamiento con Actemra. El intervalo entre la iniciación de Actemra y la administración de vacunas vivas se realizará en concordancia con las guías actuales de vacunación, en lo referente a la interacción de tocilizumab con agentes inmunosupresores. Riesgo cardiovascular: Los pacientes con artritis reumatoidea tienen mayor posibilidad de presentar trastornos cardiovasculares y deben tratarse sus factores de riesgo (por ejemplo, hipertensión, hiperlipidemia) como parte de la asistencia habitual. Combinación con agentes antagonistas del TNF: No hay experiencia en el uso de Actemra con antagonistas del TNF u otros tratamientos biológicos para artritis reumatoidea, ni para artritis idiopática juvenil sistémica o artritis idiopática juvenil poliarticular. No se recomienda el uso de Actemra con otros agentes biológicos. Sodio: Este medicamento contiene 1,17 mmol (o 26,55 mg) de sodio en una dosis máxima de 1.200 mg, lo que deberá tenerse en cuenta en el tratamiento de pacientes con dietas pobres en sodio. Dosis menores de 1.025 mg de este producto contienen menos de 1 mmol de sodio (23 mg), por lo que se considera esencialmente exento de sodio. Población pediátrica: Pacientes con Artritis idiopática juvenil sistémica (AIJs): El síndrome de activación de macrófagos (SAM) es un trastorno grave y potencialmente mortal que puede desarrollarse en pacientes con artritis idiopática juvenil sistémica (AIJs). En los ensayos clínicos con tocilizumab no se han estudiado pacientes durante un episodio de activación de SAM. Efectos sobre la capacidad para conducir y utilizar máquinas: La influencia de Actemra sobre la capacidad para conducir y utilizar máquinas es pequeña (véase Reacciones adversas, Mareos). Fertilidad, embarazo y lactancia: Mujeres en edad fértil: Las mujeres en edad fértil deben utilizar métodos anticonceptivos eficaces durante y hasta 3 meses después del tratamiento. Embarazo: No hay datos suficientes acerca del uso de tocilizumab en mujeres embarazadas. Un estudio en animales ha mostrado un aumento del riesgo de aborto espontáneo/muerte embriofetal con una dosis alta (véase Farmacología - Datos preclínicos sobre seguridad). Se desconoce el riesgo potencial en los seres humanos. Actemra no se debe administrar durante el embarazo, salvo que sea claramente necesario. Lactancia: Se desconoce si tocilizumab se excreta en la leche materna humana. Si bien las inmunoglobulinas endógenas del isotipo IgG son excretadas en la leche materna, una absorción sistémica de tocilizumab por amamantamiento es poco probable debido a la rápida degradación de dichas proteínas en el sistema digestivo. La excreción de tocilizumab en leche no ha sido estudiada en animales. Debe tomarse una decisión acerca de continuar/suspender el amamantamiento o continuar/suspender el tratamiento con Actemra, teniendo en cuenta el beneficio de la lactancia materna para el niño y las ventajas del medicamento para la mujer. Fertilidad: Los datos no clínicos disponibles no sugieren un efecto sobre la fertilidad bajo tratamiento con tocilizumab.
Interacciones.
Los estudios de interacciones se han realizado sólo en adultos. La administración simultánea de una dosis única de 10 mg/kg de tocilizumab con 10 - 25 mg de metotrexato una vez por semana no tuvo efecto clínicamente significativo en la exposición al MTX. Los análisis farmacocinéticos poblacionales no revelaron ningún efecto en el clearance de tocilizumab con MTX, antiinflamatorios no esteroideos (AINEs) o corticosteroides. Tocilizumab no ha sido estudiado en combinación con otros FAMEs biológicos. La expresión de las enzimas CYP450 hepáticas se suprime por las citocinas, como la IL-6, que estimulan la inflamación crónica. Así pues, la expresión de CYP450 puede revertirse cuando se introduce un tratamiento potente inhibidor de las citocinas, como tocilizumab. Los estudios in vitro con hepatocitos humanos cultivados demostraron que la IL-6 produjo una reducción de la expresión de enzimas CYP1A2, CYP2C9, CYP2C19 y CYP3A4. Tocilizumab regulariza la expresión de las mismas. Una semana después de la administración de una dosis única de tocilizumab, en un estudio realizado en pacientes con artritis reumatoidea, los niveles de simvastatina (CYP3A4) disminuyeron en un 57%, a valores similares o ligeramente superiores a los observados en sujetos sanos. Cuando se comienza o se detiene el tratamiento con tocilizumab, debe vigilarse a los pacientes que toman medicamentos que se ajustan individualmente y se metabolizan mediante CYP450 3A4, 1A2 o 2C9 (por ejemplo, atorvastatina, antagonistas del canal del calcio, teofilina, warfarina, fenprocumon, fenitoína, ciclosporina o benzodiazepinas), porque puede ser necesario un aumento de dosis para mantener el efecto terapéutico. Dada la larga vida media de eliminación (t½), el efecto de tocilizumab sobre la actividad de la enzima CYP450 podría persistir durante varias semanas después de suspender el tratamiento.
Incompatibilidades.
Este medicamento no debe mezclarse con otros, excepto los mencionados en Dosificación, Forma de administración, Instrucciones para la dilución previa a la administración.
Conservación.
Los viales deben conservarse en heladera entre 2°C a 8°C. No congelar. Conservar el vial en el embalaje exterior para proteger su contenido de la luz. Para las condiciones de conservación del medicamento diluido, véase Período de validez. Período de validez: Producto diluido: Después de la dilución, la solución preparada para infusión es física y químicamente estable en solución para inyección de cloruro sódico 9 mg/ml (0,9%) a 30°C durante 24 horas. Desde el punto de vista microbiológico, la solución preparada para infusión debe usarse inmediatamente. Caso contrario, los tiempos de conservación en uso y las condiciones antes del mismo son responsabilidad del usuario y no deberían superar las 24 horas a 2°C a 8°C, a menos que la dilución haya tenido lugar en condiciones asépticas controladas y validadas. Actemra se suministra como concentrado estéril que no contiene conservantes. Precauciones especiales de eliminación y otras manipulaciones: La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él, se realizará de acuerdo con la normativa local. Este medicamento no debe ser utilizado después de la fecha de vencimiento indicada en el envase. Este medicamento debe ser usado exclusivamente bajo prescripción y vigilancia médica y no puede repetirse sin nueva receta médica. Mantenga los medicamentos fuera del alcance de los niños.
Sobredosificación.
Existen escasos datos disponibles acerca de la sobredosis con Actemra. Se notificó un caso de sobredosis accidental en el que un paciente con mieloma múltiple recibió una dosis única de 40 mg/kg por vía intravenosa. No se observaron reacciones adversas. No se registraron reacciones adversas graves en voluntarios sanos que recibieron una dosis única de hasta 28 mg/kg por vía intravenosa, aunque se observó neutropenia limitante de la dosis. Población pediátrica: No se observó ningún caso de sobredosis en la población pediátrica. Ante la eventualidad de una sobredosificación, concurrir al Hospital más cercano o comunicarse con los Centros de Toxicología: Hospital de Pediatría Dr. Ricardo Gutiérrez: 4962-6666/2247; Policlínico Dr. G. A. Posadas: 4654-6648; 4658-7777; Hospital General de Niños Dr. Pedro de Elizalde: 4300-2115; 4363-2100/2200 Interno 6217.
Presentación.
Naturaleza y contenido del envase: Actemra se suministra en vial de vidrio tipo I (USP), con un tapón de goma butilo, que contiene 4 ml, 10 ml o 20 ml. Vial de 4 ml con 80 mg (20mg/ml): envases con 1 y 4. Vial de 10 ml con 200 mg (20mg/ml): envases con 1 y 4. Vial de 20 ml con 400 mg (20mg/ml): envases con 1 y 4.
Revisión.
Agosto 2016. RI+EMA+Shpe.

